食用菌中二氧化硫残留量检测方法探索
鲁瑞丽
(中检集团中原农产品检测(河南) 有限公司,河南 郑州 450000)
在现代食品加工过程中,常采用硫磺熏蒸和适量食品添加剂亚硫酸盐漂白/杀虫和防腐处理,其中的主要成分二氧化硫,会破坏食品本身的营养成分。此外,食用二氧化硫残留量过高的食品会导致食用者产生咽喉疼痛、恶心、呕吐等肠胃反应,并对肝脏也有一定的损害;因此,在食品安全国家标准 食品添加剂使用标准(GB 2760—2014)[1]中对于食用菌、坚果、饼干、食糖等食品的二氧化硫最大残留量都有相关的规定。例如,水果干类最大使用量不超过0.1 g/kg,干制的食用菌和藻类限量0.05 g/kg,白糖及白糖制品限量0.1 g/kg 等。近年来,国内外对于食品中二氧化硫检测方法有很多研究,主要包括滴定法(蒸馏-间接碘量法)、分光光度法,离子色谱法、电化学法、酶法等。日本食品卫生协会方法为蒸馏- 碱滴定法[2]、韩国食品药品安全部采用Monier-Williams 改良法[3]、英法等国也是选用的蒸馏碱滴定法[4]。我国现行有效的食品中二氧化硫检测的方法为GB 5009.34—2016[5],该标准于2017 年替代了GB/T 5009.34—2003,删 除 了GB/T 5009.34—2003[6]中紫外分光光度法。但是,由于该方法操作简单,便于批量操作,仍有一定的研究价值。根据GB 5009.34—2016 中蒸馏法测定食用菌中二氧化硫时,发现由于食用菌中一些化合物的干扰,在滴定的过程中容易产生假阳性,并且滴定终点不稳定,在出现浅紫色后颜色很快褪去;平行测定时,相对偏差达到10%以上。因此,在查阅一些文献后,选用蒸馏-直接滴定法、蒸馏-碱滴定法、紫外分光光度法进行比较,发现蒸馏-间接滴定法测定食用菌回收率达到94%以上,多次平行测定的精密度能够达到1%,这一发现对实验室在食用菌中二氧化硫的检测方面获得可重复、准确的数据有着重大意义。
1 材料与方法
1.1 仪器与试剂
试剂:纯氮气、过氧化氢溶液(9~10 g/L)、盐酸溶液(64 g/L)、溴酚蓝指示剂溶液、氢氧化钠标准溶液(0.01 mol/L)、碘标准溶液(0.01 mol/L)、淀粉指示剂(5 g/L)、二氧化硫标准溶液(1 mg/mL)、四氯汞钠吸收液、氨基磺酸铵溶液(2 g/L)、甲醛溶液(2 g/L)、亚铁氰化钾溶液(106 g/L)、乙酸锌(220 g/L)、盐酸副玫瑰苯胺(2%)。
仪器:全玻璃蒸馏器、250 mL 碘量瓶、酸式滴定管、碱式滴定管、紫外分光光度计等。
1.2 试验方法
1.2.1 蒸馏法
将称好的样品置于圆底蒸馏烧瓶中,加入250 mL水,装上冷凝装置,冷凝管下端插入碘量瓶中25 mL乙酸铅吸收液中,然后在蒸馏瓶中加入10 mL 盐酸(1+1),立即盖塞,加热蒸馏,当蒸馏液200 mL 左右时,使冷凝管下端离开液面,再蒸馏1 min。同时做空白试验。
1.2.2 紫外分光光度法
称取食用菌试样于100 mL 容量瓶中,加入20 mL 四氯汞钠吸收液,浸泡过夜,先加入亚铁氰化钾2.5 mL,摇匀,然后加入乙酸锌溶液2.5 mL,最后用水稀释至100 mL 刻度,静置30 min 后,过滤备用。同时做空白试验。吸取1 mL 上述处理液于25 mL带塞比色管中;另取0,0.20,0.40,0.60,0.80,1.00,1.50,2.00 mg/mL 二氧化硫标准使用液,分别置于25 mL 带塞比色管中。于试样及标准管中各加入四氯汞钠吸收液至10 mL,然后再依次加入1 mL 氨基磺酸铵溶液、1 mL 甲醛溶液和1 mL 盐酸副玫瑰苯胺溶液,摇匀,放置20 min。用1 cm 比色皿,以零管为参比,于波长550 nm 处测定吸光度。
1.2.3 蒸馏-碱滴定法
取2 g 样品放入蒸馏瓶中,先将样品酸化后,再在氮气(控制氮气流速0.5 mL/min) 流中加热蒸馏,并随氮气流通过过氧化氢稀溶液而被吸收氧化成硫酸,最后用标准氢氧化钠溶液滴定至终点。
2 结果与分析
通过采用3 种方法对同一样品香菇中二氧化硫残留量进行测定,蒸馏法测定时结果不稳定,相对偏差高达20.7%,不满足标准中相对偏差≤5%。造成这一现象的主要原因是,香菇中本身含有的某种物质对滴定终点进行干扰,致使在重复测定时滴定终点无法判断。紫外分光光度法与蒸馏-碱滴定法所测香菇中二氧化硫残留量重复性较好,精密度≤2%,并且2 种方法所得样品的二氧化硫残留量相对偏差1.6%。
不同方法测定香菇中二氧化硫结果见表1。
然而在进行紫外分光光度法测定食用菌中二氧化硫残留量时发现一个严重问题:低浓度二氧化硫标准溶液极不稳定,容易被氧化。
二氧化硫标准溶液吸光度随时间变化见表2。
由表2 可知,二氧化硫标准溶液的吸光度随时间变化减小,低质量浓度二氧化硫标准溶液变化较快,高质量浓度二氧化硫标准溶液相对稳定一些;这使低含量样品在测定时结果偏高。建议在每次试验前,对标准溶液进行标定。
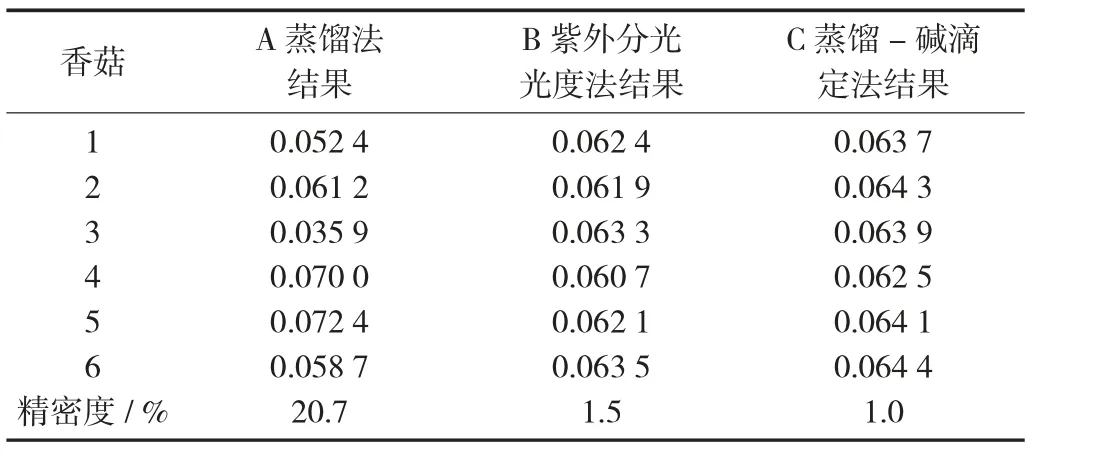
表1 不同方法测定香菇中二氧化硫结果 /g·kg-1

表2 二氧化硫标准溶液吸光度随时间变化
同时也发现该方法在分析葡萄酒等色素含量较高的食品时,色素会影响显色反应,导致假阳性,致使结果不准确;另外,该方法所使用的盐酸副玫瑰苯胺溶液,按照标准(GB/T 5009.34—2003) 中给定的配置方法,较难获得,并且显色剂对于显色反应至关重要。最终选用购置试剂公司成品盐酸副玫瑰苯胺很大程度上解决了这一难题。
为进一步验证蒸馏-碱滴定法所测食用菌中二氧化硫残留量数据的准确性,进行了加标回收试验。不同品种食用菌所测二氧化硫回收率均达到90%以上。
蒸馏-碱滴定法测定食用菌中二氧化硫结果见表3。
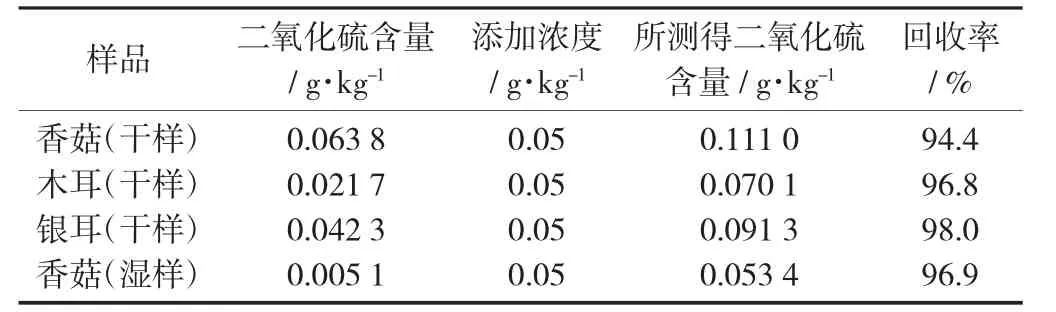
表3 蒸馏-碱滴定法测定食用菌中二氧化硫结果
3 结论
试验表明,直接蒸馏法测定食用菌中二氧化硫由于样品中某种物质产生干扰,无法确定滴定终点,结果重复性较差;采用紫外分光光度法时,结果重复性较好,但由于低浓度标准溶液不稳定,在测定之前需要对标准溶液进行标定,操作繁琐;蒸馏-碱滴定法所得结果稳定,重复性达到1.0%,并且对不同样品基质适用性良好,加标回收率94%以上。

