六硝酸合钕酸苄基三甲基铵的合成与晶体结构*
龙水红,黄慧彬,张世勇,周中高,卢莹冰,谢永荣
(赣南师范大学化学化工学院,江西省高等学校功能材料化学重点实验室,江西 赣州 341000)
稀土元素(除钪、钇外)具有独特的4f层电子结构,能与氧、碳、氮、卤素、硫、氢和磷等原子的配体形成结构多样化的配合物,体现出优越的光、电、磁性质[1-6],因此稀土配合物功能材料也一直成为化学、物理、材料学等领域的研究热点.为了进一步挖掘稀土材料的多功能应用,近年来报道了一些含有机铵离子和稀土离子组分的有机-无机杂化相变材料,并引起了研究者的广泛兴趣.如Anthony K.Cheetham等报道了2例三维有机-无机杂化稀土复钙钛矿型相变配合物(CH3NH3)2KGdCl6和(CH3NH3)2KYCl6[7].张毅和叶恒云教授报道了二维杂化稀土复钙钛矿型相变配合物,一个新的二维稀土双钙钛矿铁电体家族A4MIMIII(NO3)8,其中A为有机阳离子,MI为碱性金属或铵离子,MIII为稀土离子,这些相变配合物具有高温铁电和光致发光的性能,通过改变稀土离子,可以实现可变光致发光[8].唐云志教授等报道了2例铁电体[(CH3CH2CH2CH2)4N]3[Ln(NO3)4(SCN)2](Ln=Nd,Pr),其具有高的居里温度,大的自发极化值、二阶非线性光学和强荧光性能,拓展了稀土材料的多功能应用[9].
稀土离子是硬酸,从软硬酸碱理论来看,稀土离子更易于与氧原子(硬碱)配位,因此稀土离子能与硝酸根中的氧原子配位形成稳定的配位阴离子[Ln(NO3)6]3-或[Ln(NO3)5]2-.前期我们报道了基于稀土-硝酸配位离子与四丙铵、三丙铵、三丁铵有机铵离子合成的相变配合物[10-11],为进一步深化拓展研究,在本文中,我们选择大体积的苄基三甲基铵离子与硝酸钕反应,合成得到一例新型配合物[(C6H5CH2)N(CH3)3]3[Nd(NO3)6](1),并分析了其晶体结构及热稳定性.
1 实验部分
1.1 试剂和仪器
本论文所使用试剂均为商业上购置,未作进一步纯化处理.红外光谱在Nicolet Magna 750红外光谱仪上测量(KBr压片),测量范围400-4 000 cm-1.热重分析在TA Q50上进行,氮气气氛,加热速率10 ℃/min.元素分析在Elementar Vario-EL元素分析仪上测量.
1.2 配合物1的合成
称取Nd(NO3)3·6H2O(0.5 mmol)、C6H5CH2N(CH3)3OH(1.5 mmol)和浓硝酸(1.5 mmol)放入10 mL的透明螺口玻璃瓶中,加入5 mL有机混合溶剂(乙酸乙酯 ∶乙 醇体积比为1∶1)溶解,搅拌均匀,旋紧瓶盖,再将透明螺口玻璃瓶放入202-0型数显电热恒温干燥箱内,缓慢升温至50 ℃,保持温度加热30 min.随后取出玻璃瓶,开盖静置于室温下.冷却静置挥发3 d,得到淡紫色块状晶体.以Nd计算产率约为30%.红外光谱数据为(KBr压片,cm-1):3 030(m),1 438(vs),1 384(vs),1 317(vs),1 219(m),1 039(s),888(m),814(s),697(m),726(s).元素分析的计算值为C30H48N9O18Nd1(1):C,37.26;H,5.00;N,13.04;实测值为C,37.18;H,4.75;N,13.19%.
1.3 晶体结构的测定
选取尺寸大小合适、透明、无刮痕的配合物1块状单晶,在室温下用布鲁克单晶衍射仪ApexII收集衍射数据.在3.017°<θ<27.592°范围内以ω扫描方式共收集40 722个衍射点,其中参加精修的衍射数目为9 710个,I>2σ(I)的可观测衍射数目为9 130个.对衍射数据经Lorentz校正还原后,再用SADABS程序进行吸收校正[12].晶体结构解析使用SHELXL-97软件[13],分子结构及晶体堆积图由DIAMOND2.1软件绘制[14].配合物1的主要晶体结构参数、重要的键长数据分别列于表1和表2.

表1 配合物1的晶体学参数
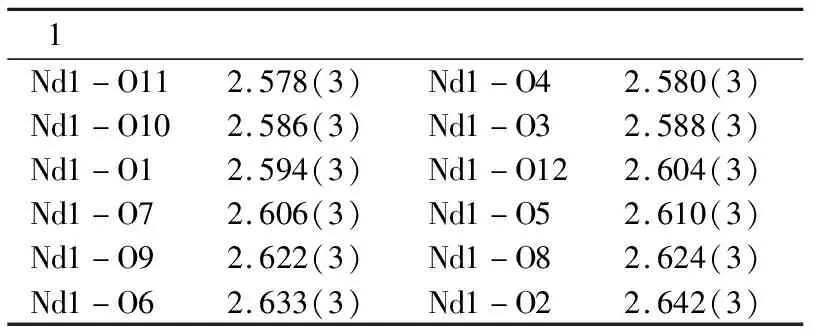
表2 配合物1的主要键长数据(Å)
2 结果与讨论
2.1 配合物1的晶体结构
通过对配合物1的结构分析发现晶体属于三斜晶系,P-1(No.2)空间群,配合物1是由[Nd(NO3)6]3-阴离子和[(CH3)3N(C6H5CH2)]+阳离子组成的典型阴阳离子共晶化合物.配合物1的不对称单元包含1个晶体学独立的[Nd(NO3)6]3-阴离子和3个晶体学独立的[(CH3)3N(C6H5CH2)]+阳离子(见图1),配合物1的中心离子Nd1为十二配位、二十面体构型,其与来自六个NO3-阴离子的十二个O原子配位,每个NO3-阴离子都以二齿方式与Nd1离子配位.Nd-O键长为2.578(3)-2.642(3)Å,均在正常范围内,与文献报道的其它钕配合物的Nd-O键长相当[15].
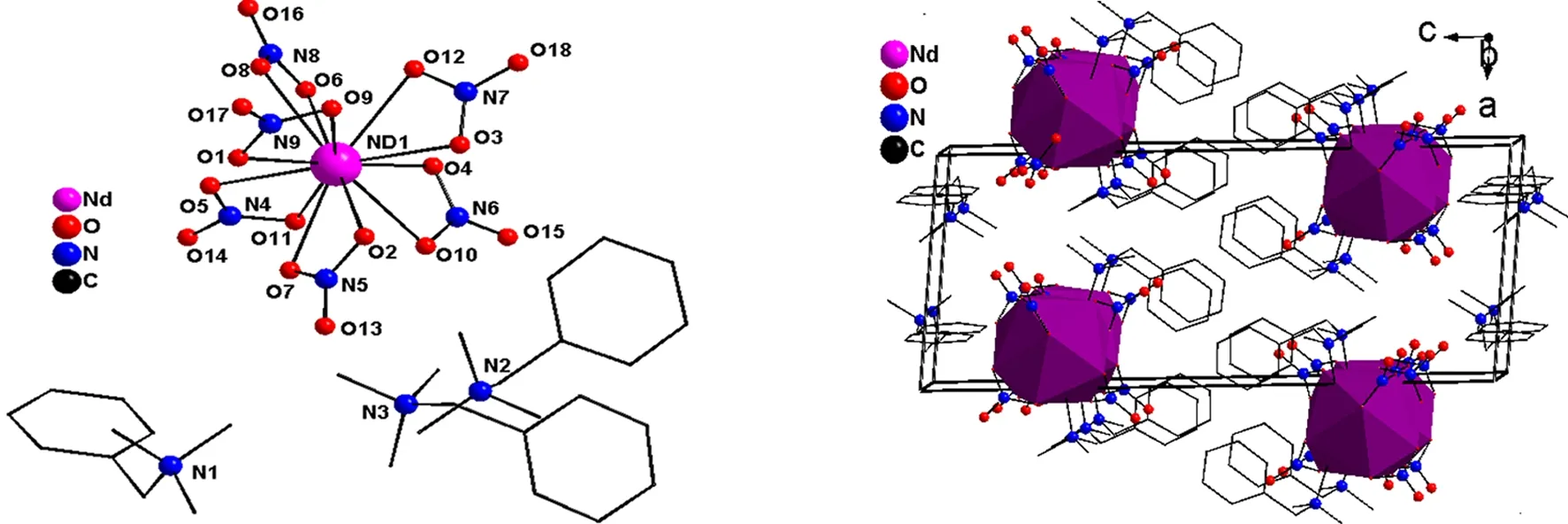
图1 配合物1的结构单元图 图2 配合物1沿b轴方向的三维结构图
由于配合物1中没有水分子,不存在经典的氢键,大体积的[Nd(NO3)6]3-阴离子和电荷平衡[(CH3)3N(C6H5CH2)]+阳离子之间通过非共价库仑力以及范德华力形成三维超分子结构(见图2).
拓扑分析显示配合物1中每个[Nd(NO3)6]3-阴离子被6个[(CH3)3N(C6H5CH2)]+阳离子包围,如Nd1分别被2个[(CH3)3N1(C6H5CH2)]+阳离子、2个[(CH3)3N2(C6H5CH2)]+阳离子和2个[(CH3)3N3(C6H5CH2)]+阳离子包围.其中Nd…N之间的距离也是各不相同,如Nd1…N1,Nd1…N2,Nd1…N3之间的距离分别为5.814 8/6.279 3,5.749 2/6.102 7,5.801 0/5.907 4Å(见图3).
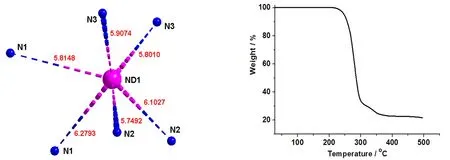
图3 配合物1中[Nd(NO3)6]3-与 图4 配合物1的热重曲线[(CH3)3N(C6H5CH2)]+之间Nd…N的距离(小于6.3Å)
2.2 配合物1的热稳定性
对配合物1在25-500 ℃温度区间进行热重测试,其热重曲线如图4所示,配合物1在空气中保持恒重到220 ℃,随后开始失重,随着温度的上升而逐步分解为硝酸钕,最后成为氧化钕,至350 ℃后,失重率达到74.78%,当温度达到500 ℃时,剩余21.74%,500 ℃以上没有继续做表征.根据热重分析曲线可得出:配合物1的分解温度范围为220-500 ℃;在220 ℃内有很好的热稳定性.
3 结论
本实验研究以Nd(NO3)3·6H2O、C6H5CH2N(CH3)3OH和浓硝酸为反应试剂,溶入有机混合溶剂(乙酸乙酯:无水乙醇体积比为1∶1),通过溶液缓慢挥发法得到配合物1。单晶衍射数据和晶体结构分析表明:配合物1结晶于P-1(No.2)空间群,晶胞参数为a=9.779(1)Å,b=10.857(1)Å,c=22.412(3)Å,α=78.064(3)°,β=81.766(3)°,γ=65.596(3)°,V=2115.5(5)Å3,Z=2.中心离子Nd为十二配位构型,来自6个NO3-的12个O原子以二齿的配位方式与Nd1离子配位,大体积的[Nd(NO3)6]3-阴离子和电荷平衡[(CH3)3N(C6H5CH2)]+阳离子之间通过非共价库仑力以及范德华力形成三维超分子结构.热重测试显示配合物1在220 ℃以内有良好热稳定性.

