新penA镶嵌等位基因致淋病奈瑟菌头孢菌素耐药的分子机制*
向 波 向 辉 熊 文 刘龙亚 印道春 王永杰 向 敏 符自清
吉首大学第一附属医院(湘西土家族苗族自治州人民医院) 1 检验科 2 肿瘤科 3 肾内科 4 泌尿一科 5 皮肤科 ,湖南省吉首市 416000
自20世纪40年代,青霉素广泛用作治疗淋病的一线药物以来,科研工作者陆续发现对氨基糖苷类、β内酰胺类、四环素类、氟喹诺酮类和广谱头孢菌素类耐药淋病奈瑟菌(Neisseria gonorrhoeae,NG)[1]。更严重的是,NG泛耐药(Extensively drug resistant, XDR)现象已经出现,2018年英国和澳大利分别发现了本国首例XDR的NG菌株[2-3]。伴随耐药现象的是每年全球上亿例淋病的高发病率。我国医疗和疾病控制系统对NG检测力度仍远远不及发达国家,尽管中国于1987年建立了淋球菌耐药检测系统(GASP),但是绝大部分医院没有开展NG培养和药敏试验,因此国内淋病疫情可能只是“冰山一角”。国内仅江浙以及两广地区一些科研院所进行小范围科研工作,报道了少量头孢菌素低敏和阿奇霉素耐药的NG菌株[4-5]。在抗生素选择性压力下,具有强大耐药特质的NG必将出现头孢菌素耐药菌株,也将会给我国医务工作者和卫生管理者带来严峻挑战。故加强监控淋病一线治疗药物头孢曲松耐药NG菌株流行状况,进一步阐明NG对头孢菌素耐药机理是淋病防治工作的重点之一。本课题组前期研究发现1例头孢菌素耐药菌株wls18099,进一步检测了与NG耐药密切的penA、mtrR、penB和ponA基因相关信息[6-9],进行了penA基因转化试验,并研究了其耐药分子机理和分子流行病学特点。
1 资料与方法
1.1 耐药菌株及药敏实验 2018年9月,我们从武陵山区1名48岁有双性接触史的男性淋病患者尿道脓液中分离出1株头孢克肟和头孢曲松耐药菌株(wls18099)。该患者无出国经历,口服200mg/bid头孢克肟4周,治疗失败。治疗期间无任何性接触,但其性伴侣的性接触史未知。之后,用单剂量160mg庆大霉素注射治疗成功。1个月后,NG培养和NG-PCR复检阴性。NG微生物学鉴定及药敏实验,参照第28版CLSI M100。
1.2 NG-MAST分型、耐药基因扩增及生物信息学分析 使用上海生工试剂盒(货号B518255)提取NG基因组DNA。分子流行病学分析采用NG-MAST分型,引物:por,CAAGAAGACCTCGGCAA和CCGACAACCACTTGGT;tbpB,CGTTGTCGGCAGCG-CGAAAAC和TTCATCGGTGCGCTCGCCTTG。扩增:95℃ 4min,95℃ 30s,por 58℃/tbpB 69℃各30s, 72℃ 1min,25个循环,72℃10min。penA、mtrR、penB和ponA 4种与NG密切相关的重要耐药基因PCR引物参照Liao M和Lee SG的数据[10-11]。PCR扩增:引物0.5μl,模板0.5μl,酶0.5μl,镁1.5mmol/L,dNTPs 200μmol/L;94℃4min,94℃40s,penA 58℃/mtrR 50℃/penB 46℃/ponA 56℃各40s,72℃50s,35个循环,最后72℃ 6min。扩增仪为ABI7500。电泳检查产物,提取凝胶中DNA,送上海生工测序。使用BioEdit7.1.9比对这4种耐药相关基因在wls18099和野生型菌株M32091之间的差异。
1.3 penA基因转化分析 通过比对后,将wls18099菌株中存在差异的基因,进行转化实验[12]。受体菌株为两种标准菌株WHO M(MIC头孢克肟≤0.016μg/ml、MIC头孢曲松0.016μg/ml)、WHO L(MIC头孢克肟0.25μg/ml、MIC头孢曲松0.125μg/ml)以及一种临床分离头孢菌素敏感菌株wls11020(MIC头孢克肟0.008μg/ml、MIC头孢曲松0.016μg/ml)。设立重复实验,并测定转化后WHO M’、WHO L’和wls11020’菌株中penA、ponA、mtrR和penB序列,以排除转化引起新的变异。最后测定3种转化株对头孢克肟和头孢曲松的最小抑菌浓度(MIC头孢克肟和MIC头孢曲松)。
2 结果
2.1 wls18099耐药菌株分子生物学信息 wls18099耐药菌株NG-MAST分型,属于ST14155。该菌株mtrR、penB和ponA基因序列与野生型菌株M32091比对,未发现新突变。我们在该菌株penA基因中,发现一种类似penA ⅩⅩⅩⅣ基因型的新镶嵌等位基因型。其包含bp1507A/C与1508A/C颠换,并导致青霉素结合蛋白氨基酸序列K503P错义突变(赖氨酸→脯氨酸),暂命名为penA wls ⅩⅩⅩⅣ/K503P,见图1。

图1 头孢菌素耐药wls18099菌株和头孢曲松敏感野生型M32091菌株间penA基因编码蛋白PBP2氨基酸序列差异
2.2 转化实验前后3种菌株MIC值变化及4种基因特点 wls18099菌株对头孢克肟和头孢曲松耐药。WHO M、WHO L和wls11020转化wls18099菌株penA基因后头孢菌素类MIC值较转化前上升4~62倍,详见表1。WHO M、WHO L、wls11020和wls18099菌株por、tbpB、penA、ponA、mtrR和penB基因特点,详见表2。转化后WHO M’、WHO L’和wls11020’菌株除penA wls ⅩⅩⅩⅣ/K503P位点改变,其余3种基因序列未产生新的变异。
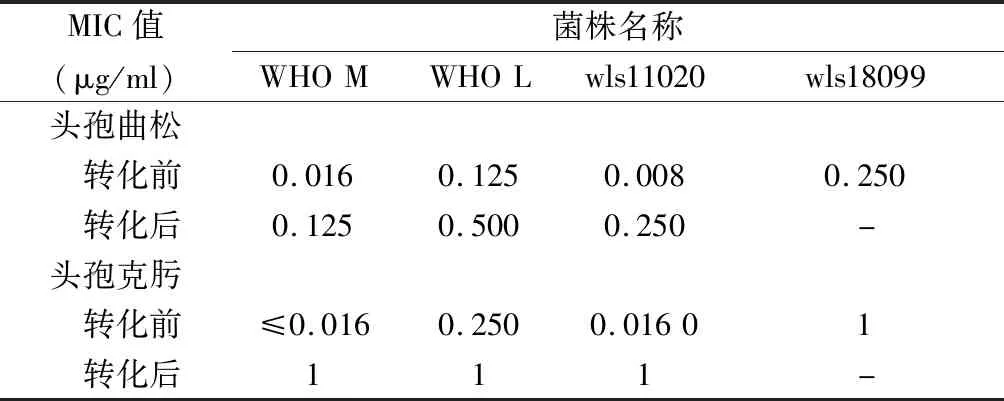
表1 3种菌株转化penAwls ⅩⅩⅩⅣ/K503P等位基因前后MIC值
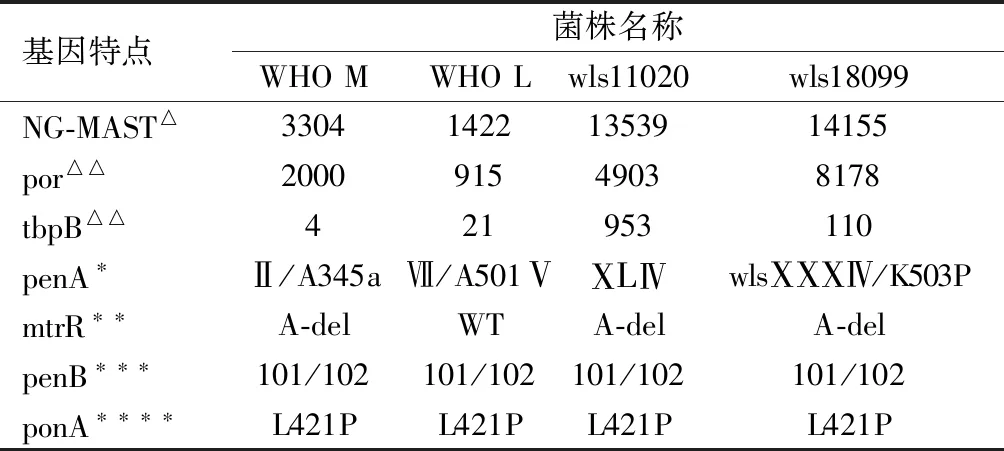
表2 WHOM、WHOL、wls11020和wls18099菌株基因特点
3 讨论
wls18099是湖南省首例头孢菌曲松耐药淋病奈瑟菌(Neisseria gonorrhoeae,NG),我们采用多抗原序列分型(NG-MAST),探讨了其分子流行病学特征。wls18099菌株与日本兵库县发现的KG12051菌株NG-MAST分型分别为ST14155和ST14150型,por基因型分别为ST8178型和ST8173型,二者tbpB基因型均为ST110型。生物信息学比对发现,二者por基因碱基序列差异<100bp,二者同属于G1407基因群,两株菌同源性极高[13]。尽管该基因群NG是欧洲和亚洲流行的头孢曲松耐药NG之一,但是2015年中国首先报道的该群菌株对头孢曲松均敏感(MIC 0.008~0.06μg/ml)[13-15]。从上述报道的时间先后可以推测出我们发现的头孢曲松耐药菌株wls18099来源于国外的G1407基因群。众所周知,拥有强大的基因重组和潜在的高度耐药变异能力是NG的重要特性。很明显,该群NG通过近几年在国内传播,可能获得了头孢菌素类耐药抗性的基因改变,导致其对头孢菌素类敏感性由敏感转化为耐药。
NG对广谱头孢菌素(Extended spectrum cephalosporins,ESCs)产生耐药主要与penA、mtrR、penB和ponA等基因突变相关。本课题组通过对wls18099耐药株4种基因测序,发现penA基因出现一种特殊wls ⅩⅩⅩⅣ/K503P镶嵌突变,未在其余3种基因中检出新突变。2015年国内报道的4例G1407群NG菌株中,有3例头孢曲松敏感菌株的penA基因型为ⅩⅩⅩⅣ型[15]。我们发现的头孢曲松耐药菌株wls18099与前述3例头孢曲松敏感NG菌株差异在于,penA基因编码蛋白PBP2发生了新的K503P改变。这提示我们,penA wls ⅩⅩⅩⅣ/K503P等位基因型可能是导致wls18099菌株与其他头孢菌素敏感NG菌株在药敏表型上差异的主要原因。我们在国内首次报道了这种新的penA镶嵌等位基因,这也是本研究最重要的发现。
目前,已经先后发现49种penA等位基因型,其中Ⅹ、ⅩⅩⅥ、ⅩⅩⅦ和ⅩⅩⅩ等都属于镶嵌基因型[11,16]。penA镶嵌等位基因型具有较高的复杂性和多变性,其中涉及突变位点达到50余个。上述已知类型的镶嵌等位基因型与耐药有一定联系,但无严格对应关系[15]。因为,不同NG菌株耐药表型的差异不仅仅是蛋白质一级序列的问题,还可能与编码蛋白的基因组甲基化、基因诱导调控等表观遗传调控等协同因素相关。近年来,针对penA镶嵌等位基因型的研究逐渐由Ⅹ转向 ⅩⅩⅩⅣ型[7]。2018年Ryan L应用whole-genome sequencing技术,在9例头孢菌素低敏菌株中检测出6例含有penA ⅩⅩⅩⅣ等位基因[17]。2018年,Washington在美国佐治亚州1名23岁士兵的尿道拭子中检出了头孢克肟耐药菌株G093携带penA ⅩⅩⅩⅣ镶嵌型等位基因型[8]。科研工作者们先后在旧金山、台湾和加拿大发现 ⅩⅩⅩⅣ型[18],但是其对头孢曲松和头孢克肟仅仅表现为敏感性降低,MIC分别为0.06~0.125μg/ml和0.125~0.25μg/ml。本研究特殊之处在于,同样包含penA ⅩⅩⅩⅣ基因型的wls18099具有更高水平的耐药现象,头孢曲松和头孢克肟MIC分别为0.25μg/ml和1μg/ml。上述差异可能与wls18099菌株同时具有penA ⅩⅩⅩⅣ等位基因和一个未见报道的PBP2蛋白A503P氨基酸错义突变有关。赖氨酸A与脯氨酸P结构和生理功能相差较大,我们据此假设,penA ⅩⅩⅩⅣ镶嵌基因和PBP2蛋白A503P变异具有协同作用,共同导致wls18099菌株产生耐药表型。
我们对penA wls ⅩⅩⅩⅣ/K503P镶嵌型等位基因认识还远远不够。因此,我们在头孢菌素耐药wls18099菌株与2种标准菌株和1种头孢菌素敏感菌株间分别进行了penA基因水平转化实验,初步阐明了其对PBP2抗头孢菌素类抗生素的活性。转化实验采用的受体菌株为WHO M、WHO L标准菌株以及临床分离头孢菌素敏感菌株wls11020。结果显示,3种菌株转化wls18099菌株penA wls ⅩⅩⅩⅣ/K503P镶嵌型等位基因后,均显示出对头孢克肟和头孢曲松耐药特征,且MIC值是转化前的4~62倍。通过对上述3种受体菌株中其他主要耐药基因测序(ponA、mtrR和penB),明确了penA基因转化试验没有造成这3种基因序列产生新的变异,排除了这3种NG耐药相关基因突变而引起耐药性改变的干扰。这提示,wls18099耐药菌株携带的penA ⅩⅩⅩⅣ/K503P镶嵌基因型很可能是导致该菌株对头孢菌素类抗生素稳定地产生耐药性的重要独立因素。
综上所述,我们于2018年首次在国内分离出1例伴有K503P错义突变的penA wls ⅩⅩⅩⅣ/K503P镶嵌等位基因型的头孢菌素类耐药NG株wls18099。尽管penA ⅩⅩⅩⅣ镶嵌基因型不是引起NG耐药的唯一因素,但是本课题组通过penA基因转化试验证实,前者在PBP2蛋白K503P改变的协同下,产生稳定耐药性。在后续研究中,我们将继续监测penA wls ⅩⅩⅩⅣ/K503P等位基因型,在湖南和周边省份的播散情况,以控制头孢菌素耐药的wls18099菌株播散。

