氢离子阻断CCL5-CXCL4异构体通过减弱白细胞募集和内皮增生改善心肌梗死后心功能的机制
詹莉 代菁 刘超
(1武汉市第八医院心血管内科,湖北 武汉 430010;2江汉大学附属医院 武汉市第六医院心电图室;3天津市胸科医院心血管病研究所)
心肌梗死(MI)是发达国家最常见的死亡原因之一,因此寻找新的预防和治疗MI策略是首要任务。冠状动脉粥样硬化是血管阻塞后急剧缺乏血液供应导致心肌细胞死亡并引起许多炎症因子的显著上调。通过再灌注疗法有效治疗急性MI促进血流恢复至缺血心肌。低浓度氢气或氢离子或氢气饱和生理盐水对多种疾病具有神奇的保护作用,包括心肌缺血再灌注损伤。炎症反应在再灌注期间继续损伤心脏组织,这可能导致进一步不可逆的心肌细胞死亡。炎症反应也可用于制备心肌组织和修复驻留细胞〔1〕。最近显示嗜中性粒细胞将巨噬细胞极化为修复表型,表明嗜中性粒细胞(白细胞的一种)在MI相关炎症中的作用〔2~5〕。
趋化因子是与特异性G蛋白耦联受体(GPCR)结合并发挥不同功能的小细胞因子,趋化因子能调节白细胞的活化并协调它们对炎症部位的运输〔6〕。趋化因子(CCL)5和血小板因子(CXCL)4储存在血小板的分泌性α-颗粒中,是有效的中性粒细胞和单核细胞引诱剂〔7,8〕。此外,这些趋化因子显示出嗜异性相互作用,CCL5-CXCL4异构体募集单核细胞和中性粒细胞方面特别有效〔9~12〕。由于CCL5的实验性抑制在心肌再灌注期间显示出心脏保护作用〔13~15〕,假设阻断CCL5-CXCL4相互作用将在MI的早期阶段具有治疗益处,可能对MI具有治疗效果。本研究评估了氢离子处理对心肌缺血再灌注小鼠模型中心肌组织和心脏功能的影响。
1 资料与方法
1.1实验动物 雄性C57BL/6J小鼠,10周龄,重约25 g,购自湖南斯莱克景达实验动物有限公司。饲养于空调室内,光照周期为12 h 20℃±2℃和50%~60%湿度,饮用水均经过灭菌处理。
1.2心肌缺血模型 实验所用动物用5%异氟烷麻醉,在呼吸机支持下通过做中线颈部切口暴露左颈总动脉、颈内动脉和颈外动脉,用尼龙缝合线缝合颈总动脉,并将缝合线推进至颈动脉分叉处约9 mm处,以闭塞大脑中动脉(MCA),心肌缺血60 min建立心肌缺血再灌注模型。在假手术组中,进行了相同的手术,但没有将缝合线插入MCA。共有30只小鼠随机分组,包括10只假手术小鼠和20只心肌缺血小鼠,用于整个实验。所有实验程序由广东省医学实验动物中心批准,并且根据动物使用和护理指南进行实验。
1.3实验处理 将 20只心肌缺血小鼠随机分为对照组与氢离子组,每组10只,对照组和假手术组采用预先用氧平衡(体积分数95%O2+5%CO2)的37℃空白灌流液(K-R液)灌注,氢离子组采用预先用氧平衡(体积分数95%O2+5%CO2)的37℃ K-R液+氢离子灌注(0.6 mmol/L pH7.3)。实验完毕后取材,伊文蓝染色观察两组大鼠心肌组织的心肌病理学改变,测定心肌组织中白细胞和内皮细胞数量。
1.4研究方法
1.4.1RNA提取和逆转录聚合酶链反应(RT-PCR)分析 使用TRIzol试剂(Invitrogen)分离总RNA。使用Prime-Script RT试剂盒(日本TaKaRa公司)合成逆转录的互补DNA。常规PCR用于使用特异性正向引物测定miRNA表达,并且使用小核RNA互补的通用反向引物作为内部对照。CCL5和CXCL4的PCR引物设计:CCL5:上游引物TCAGGTCATCACTATCGGCAAT,下游引物AAAGAAAGGGTGTAAAACGCA;CXCL4:上游引物CCCATCTATGAGGGTTACGC,下游引物TTTAATGTCACGCACGATTTC ;β-actin:上游引物AACAGTCCGCCTAGA AGCAC,下游引物CGTTGACATCCG TAA AGACC,PCR循环通过在95℃下初始变性进行5 min,然后在95℃ 30 s,58℃ 30 s,72℃ 1 min条件下完成35个循环,最后72℃ 1 min。
1.4.2CCL5/CXCL4表达量的检测 为了检测氢离子处理后心肌缺血小鼠中CCL5-CXCL4异构体的表达水平,在灌注后10 h收获样品,在冷裂解缓冲液(10 mmol/L 4-2-羟乙基-1-哌嗪-乙磺酸〔pH 7.9〕,1.5 mmol/L MgCl2,10 mmol/L KCl,1 mmol/L二硫苏糖醇)和蛋白酶抑制剂混合物(德国RocheDiagnostics GmbH公司)中轻轻匀浆,然后离心,收集上清液并用于分析。使用二辛可宁酸(美国Pierce公司)测量蛋白质浓度。将蛋白质(36 μg)加载到每个泳道中,用4%~15%聚丙烯酰胺凝胶(Bio-Rad公司)分离,并电转移至聚偏二氟乙烯膜(美国MILLIPORE公司)。用含有0.1%吐温20的磷酸盐缓冲液(PBS)中的5%脱脂奶粉封闭膜1 h,并与1∶250抗小鼠CCL5抗体(美国R&D Systems Inc公司)一起温育过夜。用PBS中的0.1%吐温洗涤3次,然后在室温下与1∶1 000二抗(美国Cell Signaling Technology公司)一起温育2 h,并用0.1%Tween的PBS溶液洗涤3次。用ECL试剂(瑞典Amersham Biosciences公司)检测信号。β-肌动蛋白用作内部对照。用Image J软件进行条带的光密度分析。
1.4.3流式细胞仪统计白细胞和内皮细胞数目 在灌注后10 h用过量的异氟烷对小鼠实施安乐死,并用50 ml冷PBS灌注。使用3 ml缓冲液(含有1%胎牛血清的PBS)与3 ml 90%细胞分离液〔通用电气(中国)有限公司〕混合在冰上收集他们的心肌细胞,细胞悬浮后加入1 ml 70%细胞分离液,然后将样品在4℃下以1 500 r/min离心30 min,收集白细胞并用缓冲液洗涤,然后将细胞重新悬浮用于统计。
1.4.4伊文氏蓝/四唑染色法 为了评估梗死面积的大小,从对照组和氢离子组(每组10只)中分别切下心脏并用PBS洗涤,灌注200 μl伊文蓝。在-20℃下冷冻1 h后,将心脏切成5个切片,并在四氮唑溶液中于37℃孵育10 min,然后在10%甲醛中温育10 min。将切片固定在显微镜载玻片之间用于照相和测量。使用Image J测量包含蓝色正常区域,红色受伤但仍存活区域和白色梗死区域的总脑室面积。缺血区(AAR)计算为总染色区域和蓝染区域之间的差异,并表示为总脑室的百分比梗死面积计算为白色未染色区域。
1.4.5超声心动图 在小动物超声成像仪(日本富士VisualSonics公司)上进行二维和M模式超声心动图测量。两种程序均在心肌缺血再灌注后进行。用含1.5%异氟烷的面罩麻醉小鼠,并置于温热垫上的仰卧位。记录和分析射血分数,心输出量,左心室舒张末期(LVEDD),左心室收缩末期(LVESD)直径,心率和心脏重量。
1.5统计学方法 采用SPSS20.0软件进行独立样本t检验、χ2检验。
2 结 果
2.1CCL5和CXCL4 mRNA的表达 与对照组(0.37±0.01、0.31±0.01)比较,氢离子组CCL5和CXCL4的表达量显著降低(0.29±0.01、0.25±0.02;χ2=9.170、7.852,P=0.008、0.015),说明氢离子能够阻断CCL5和CXCL4的表达。见图1。
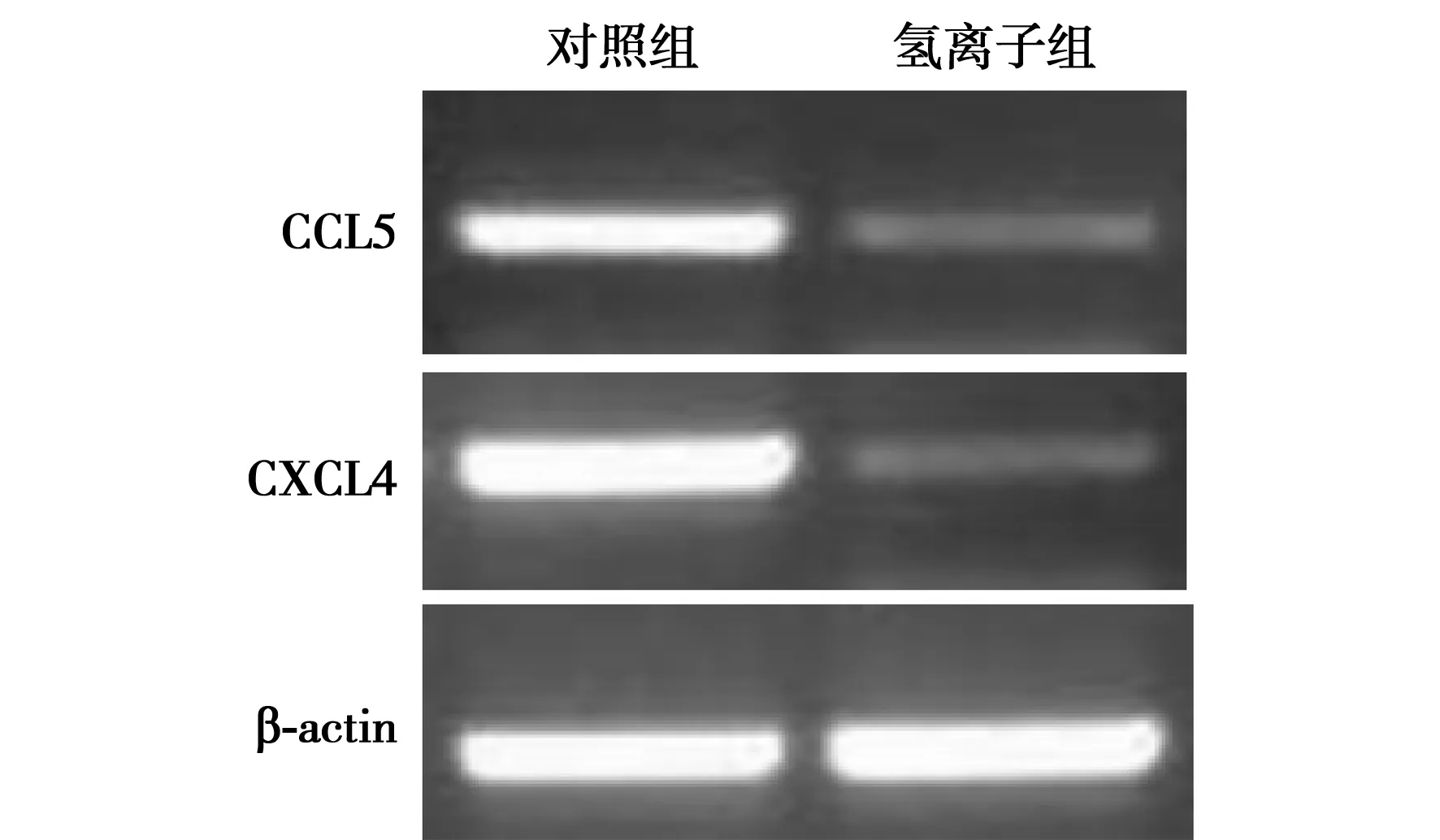
图1 RT-PCR检测mRNA表达
2.2CXCL4-CCL5异构体的表达量 氢离子组CXCL4-CCL5表达量(0.29±0.01)显著低于对照组(0.37±0.013,t=9.17,P=0.008),说明氢离子能够降低CXCL4-CCL5异构体的表达,阻止CXCL4-CCL5异二聚体的形成。见图2。

图2 CXCL4-CCL5异构体蛋白表达
2.3白细胞和内皮细胞数目 与对照组〔(19.47±2.13)×104、(33.26±89.74)〕相比,氢离子组中白细胞和内皮细胞的数目均显著下降〔(9.01±2.03)×104、(28.74±85.35);P<0.05〕,说明白细胞和内皮细胞参与氢离子阻止CXCL4-CCL5异二聚体的形成过程。
2.4氢离子对心肌细胞存活和梗死面积的影响 伊文氏蓝染色显示氢离子组与对照组相比梗死面积明显减小,心肌细胞存活区域显著增多(P<0.01),见表1、图3。说明氢离子对心肌缺血有保护作用。

图3 心肌细胞

表1 各组实验动物心肌细胞存活和梗死面积比较
2.5氢离子对MI后心功能的影响 与对照组相比,氢离子组射血分数和心输出量显著增加,心率和心脏重量变化差异无统计学意义,左心室舒张(LVEDD)和收缩(LVESD)末期内径显著减小,用氢离子治疗的心脏没有扩张,说明了氢离子对MI后的心功能有积极的作用。见表2。
表2 超声心动图评估不同处理组心脏功能
3 讨 论
MI发生后,心肌每天从循环系统招募数十万白细胞,骨髓造血系统也迅速启动造血生成,同时交感神经也会刺激造血祖细胞迁移至脾脏,产生骨髓外造血,分化出大量白细胞,进一步促进炎症的产生,加重心室重构,造成巨大危害。因此,研究MI发生后对白细胞生成的影响,对抑制MI后炎症加重有重要的临床意义。
本研究证明了氢离子能够特异性阻断CCL5-CXCL4相互作用,用于治疗心肌缺血/再灌注损伤。由于MI后炎症减少,给予氢离子显著减少了梗死面积。用氢离子治疗后,中性粒细胞和单核细胞浸润到受影响的心肌区域减少,这对梗死结果和心脏功能产生积极影响。循环单核细胞在MI后以不同的波形渗入受影响的组织,经典的Ly6Chi CCR2+单核细胞负责清除死细胞和Ly6Chi CCR2-单核细胞用于组织修复,此外,在健康的稳态条件下,心脏组织中充满了常驻巨噬细胞。在心脏,肝脏和脑中组织驻留巨噬细胞起源于胚胎卵黄囊衍生的前体。在稳态条件下,发现心脏主要由驻留的卵黄囊衍生的巨噬细胞Ly6Clow CCR2-细胞填充,其通过局部增殖自我维持,但各个趋化因子对常驻巨噬细胞的作用尚不明确。本研究观察到用氢离子处理后心脏单核细胞含量降低。我们无法区分常驻细胞和浸润细胞,因为Ly6Clow CCR2-单核细胞在急性缺氧事件后发生在梗死区域。由于梗死区域通过心脏的特殊分布(缺血/再灌注损伤的特征),氢离子治疗后梗死面积的显著减少允许远端心肌补偿丢失的组织,从而保持区域收缩性和心脏功能。心肌具有复杂的细胞结构,除了心肌细胞外,还包括成纤维细胞和整合在毛细血管中的内皮细胞。在缺氧期间,内皮细胞重新组织并开始由MI后直接释放的血管生成因子控制的血管生成,而成纤维细胞开始增殖〔16〕。然而,如本研究中的发现所示,心肌细胞正在经历凋亡或甚至坏死。
在所有趋化因子中,趋化因子CCL5在心血管疾病中起特殊作用。CCL5介导单核细胞和T淋巴细胞通过内皮的阻滞和迁移。动脉粥样硬化病变的进展是通过减少梗死后的趋化因子寡聚化〔17〕和心肌损伤,通过减少受影响心肌细胞中白细胞浸润,趋化因子表达和细胞凋亡〔13〕。该结果表明,氢离子对异构体形成的抑制减少了心肌损伤,中性粒细胞和单核细胞浸润到受影响的组织中的程度与CCL5拮抗剂或阻断抗体完全抑制相似〔15〕。CXCL4在血小板聚集期间从活化血小板的α-颗粒释放,并且可以通过与肝素样分子结合来调节血液凝固。CXCL4已被公认为巨核细胞生成和血管生成的生理抑制剂,而不是经典的白细胞募集趋化因子。尽管如此,CXCL4可能会促进炎症,尤其是心血管疾病。例如,CXCL4的遗传缺失减少了小鼠的动脉粥样硬化斑块和新内膜形成〔18〕。研究表明,CXCL4可作为平滑肌细胞的促炎和促有丝分裂因子,促进血管损伤后的重塑〔12〕。在急性冠状动脉综合征期间,患者血清CXCL4水平升高,与心肌损伤的严重程度相关。在机制水平上,CXCL4对CCL5功能的增强似乎主要由CCR1介导,这与CCR1在心肌缺血/再灌注损伤中的作用一致〔8〕。因此,CXCL4似乎在CCL5介导的CCR1激活中起辅助作用,这一功能可能对CCL5的体内活性至关重要。最近的研究也支持这一观点,该研究在炎症性疾病的小鼠模型中实施了氢离子。例如,氢离子显示抑制腹主动脉瘤的形成和进展,减少主动脉直径增大,保留内侧弹性蛋白纤维和平滑肌细胞,并减弱壁画巨噬细胞浸润,血管生成和主动脉金属蛋白酶2和9表达。已知心肌细胞表达CCL5,并且向心肌细胞中添加CCL5显著降低了肌细胞的收缩性。由于趋化因子CCL5和CXCL4通过异构化发挥特定功能,因此通过氢离子阻断它不应改变这些趋化因子的水平,但它确实阻断了异构体的功能。 氢离子的处理减少了单核细胞向缺血细胞的浸润。

