硫化钴锂离子电极材料的制备和应用研究
韩 旭,王利娟,毕研峰
(辽宁石油化工大学石油化工学院,辽宁抚顺113001)
锂离子电池(LIBs)自20 世纪90 年代实现商业化生产后,因具有工作电压高、能量密度大、使用寿命长、无记忆效应等优点,已经广泛用于各种便携式电子设备,并且是有应用前景的电动力汽车用电源[1-3]。
对于锂离子电池,电极材料的性能在很大程度上决定了电池的各项性能指标。目前商业化锂离子电池负极大多为石墨,但是石墨电极的理论比容量低(372 mA·h/g),能量密度低,安全性差,限制了其在动力电池上的广泛应用[4]。因此,寻求高比容量和安全性的负极材料成为锂离子电池研究的热点之一。硫化钴类化合物因具有理论比容量和电子电导率较高、热稳定性好等优点成为很有希望用在动力锂离子电池上的一类负极材料[5-6]。
在钴的硫化物中,由于化学键Co-S 存在多种作用力和结合机制,可以形成离子键、共价键和金属键,因此可以形成多种硫化钴类化合物,如CoS、Co S2、Co3S4、Co1-xS、Co9S8[7-8]。硫化钴类化合物均具有较高的导电性能、天然高丰度、低成本以及较高的理论容量。其中,CoS、CoS2、Co3S4、Co1-xS 和Co9S8的理论容量分别为590.0、870.0、702.8、682.6、544.0 mA/g,均高于石墨电极的理论容量,而CoS、CoS2和Co9S8是目前研究较为广泛的电极材料,具有良好的热稳定性;Co3S4和Co1-xS 是优秀的电催化和光催化材料,近些年来才出现在锂离子电极材料的研究领域,其具有较高的理论容量和特有的性能,将是未来硫化钴锂离子电极材料中的重要成员。
然而,硫化钴类化合物应用于锂离子电池电极材料时存在循环周期短、倍率性能差等问题。同时,循环过程中发生体积膨胀或缩小的变化会导致电极材料上纳米颗粒的崩坏。目前,主要是通过形貌调控改性和导电物包覆改性、异种元素掺杂等手段提高硫化钴电极材料锂电性能。
1 Co9S8负极材料研究进展
在众多钴的硫化物中,Co9S8具有相对优良的导电性、较高的理论比容量(544 mA·h/g)以及较低的制备成本[9],被认为是很有应用前景的锂离子电池负极材料之一。
Co9S8的晶体结构如图1 所示[10]。S 原子为立方紧密堆积,其中8/9的Co原子被S 原子形成的四面体包围,其余1/9 的Co 原子被S 原子形成的八面体包围。X.Liu 等[11]对Co9S8的XRD 数据进行分析,同样得到了Co9S8的晶体结构,如图2 所示。该结构由CoS6八面体和CoS4四面体组成,其中每个CoS6八面体均与24个CoS4四面体共同占据6个角。每个Co9S8单元中,9个Co原子占据4b(Co1)和32f(Co2)位,8个S 原子占据8c(S1)和24e(S2)位。Co1 与6 个S2 原子配位形成CoS6八面体,Co2 与一个S1 和3 个S2 原子配位形成扭曲的CoS4四面体。Co1-S2、Co2-S1和Co2-S2的键长分别为0.234、0.212、0.223 nm。

图1 Co9S8的晶体结构示意图[10]
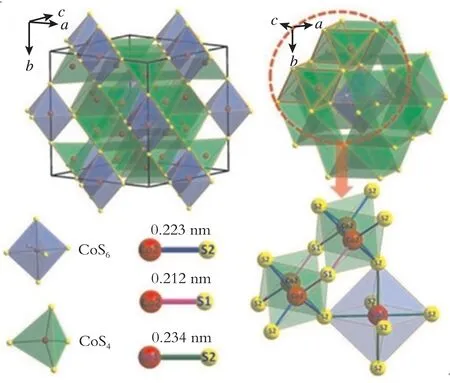
图2 Co9S8立方体结构示意图[11]
Co9S8拥有较高的理论比容量主要是因为锂和硫化物之间的可逆转换,Co9S8与Li+的充放电反应方程式为:Co9S8+16Li++16e-↔9Co+8Li2S。然而,Co9S8电子电导率低,充放电过程中体积变化大,颗粒团聚以及在电解液中溶解导致容量衰减快[12-13]。研究者主要采取以下方法来解决这些问题:①通过形貌控制构建新型纳米结构,如中空结构、介孔结构和3D 分级结构等,获得更大的比表面积以缩短Li+脱嵌的距离,提高反应速率来减缓充放电过程中体积的膨胀[14]。②通过碳包覆,既能提高电极材料的导电性能,又能抑制充放电过程中体积膨胀,这有利于改善材料的循环和倍率性能;同时,引入碳材料也会减缓Co9S8的溶解,延长材料的循环寿命[12]。因此,近年来诸多学者基于以上两种方法对Co9S8电极材料进行改性,以此来提高其循环和倍率性能以及放电比容量。
1.1 形貌调控改性Co9S8
理论上,具有纳米尺寸的锂离子电池电极材料具有许多优点:①小的粒径可以缩短Li+脱嵌的距离;②大的比表面积可以确保与电解质的高度接触以提高反应速率。然而,纳米尺寸的材料也有以下缺点:①纳米颗粒在长循环过程中容易发生团聚;②低振实密度会降低电极材料的体积能量密度[15]。因此,构建新型的纳米结构对于提高Co9S8的循环及倍率性能和放电比容量具有重大意义。
1.1.1 微/纳和二维纳米片结构Co9S8的制备
2017 年,Y.H.Wang 等[15]以Co3O4为前驱体,硫化后成功制备了具有微/纳结构的立方形Co9S8和球形Co9S8。微/纳结构的电极材料具有微米尺寸材料的高振实密度和纳米尺寸材料的高比表面积。这两种形状的Co9S8表现出良好的电化学性能,在电流密度为545.0 mA/g 时,初始放电比容量分别为599.0、550.0 mA·h/g,循环300 次后仍保留了370.0、369.0 mA·h/g 的放电比容量。
同年,P.Long 等[16]为了探究Co9S8纳米片与纳米颗粒对材料电化学性能的影响,使用聚乙烯醇(PVA)辅助的沉淀反应合成具有二维结构的Co9S8纳米片;不含PVA,但在相同工艺下制备了Co9S8纳米颗粒。电化学结果表明,Co9S8纳米片由于独特的二维纳米结构表现出比纳米颗粒更好的倍率性能和循环稳定性。在电流密度为0.1 A/g时,Co9S8纳米片的首次放电比容量高达1 215.5 mA·h/g;当电流密度提高到1.0 A/g 时,Co9S8纳米片循环300 次后仍然能释放高达746.8 mA·h/g 的比容量,这远远高于Co9S8纳米颗粒(63.6 mA·h/g)。即使在2.0 A/g 的高电流密度下,Co9S8纳米片仍具有712.7 mA·h/g 的高放电比容量,而Co9S8纳米颗粒 仅 有137.5 mA·h/g。因此,开发了一种用于合成二维Co9S8纳米片的简便途径,与溶剂热合成和常规水热合成方法相比,具有成本低、反应时间短和能耗低且易于大规模生产的特点,而且该方法制备的锂离子电池负极材料Co9S8具有高可逆容量、优良的倍率性能和循环稳定性。
1.1.2 核-壳与中空结构Co9S8的制备 研究表明,拥有核-壳结构、中空结构的电极材料可以利用其特殊的结构抑制脱嵌锂引起的体积变化,进而提高材料的循环稳定性[17-23]。
2017 年,X.Tang 等[21]以碳球为核、Co9S8为壳设计了一种核-壳C@Co9S8复合材料。葡萄糖碳化后的碳球被Co9S8外壳包裹,由于碳球的支撑可以抑制Co9S8在充放电过程中结构塌陷以及颗粒团聚。此外,在Co9S8外壳上形成的一层薄的固体电解质膜(SEI)可以减缓材料在电解液中溶解(见图3)。这都有利于材料的电化学性能,在电流密度为1 000.0、2 000.0、4 000.0 mA/g 时,循环300 次后放电比容量分别为588.0、518.0、489.0 mA·h/g。因此,Co9S8显示出良好的倍率和循环性能。

图3 C@Co9S8的SEI 壳层的形成及电子传导示意图[21]
金属有机骨架(MOFs)是由多齿有机配体与金属离子通过自组装过程形成的具有周期性网络结构的一类新材料。近年来,以MOFs为前驱体合成先进功能材料,如纳米多孔碳材料、金属氧化物纳米材料,成为MOFs化学及新功能材料研究领域的新热点。
MOFs衍生的金属硫化物@碳纳米复合材料中金属硫化物通常为纳米粒子,且可以均匀分布在碳基材料中,这种复合物不仅能提高材料的导电性能,而且能增加活性物质和电解液之间的接触面积,有利于提高材料的电化学性能。2016年,J.Liu等[22]以室温合成的ZIF-67(Co的MOF)为模板,合成了中空纳米Co9S8和碳的复合材料(HCSP⊂GCC),其中碳可以提高材料的电子电导率,减缓纳米Co9S8的团聚。Co9S8的中空结构可以缓冲其体积膨胀,易于Li+脱嵌,以此提高反应速率,从而改善循环和倍率性能。复合材料HCSP⊂GCC 在电流密度为100.0 mA/g 时,初始放电比容量高达2 700.0 mA·h/g 左右,循环40 次后可保持在1 600.0 mA·h/g;在1 000.0 mA/g 的高电流密度下,循环350次后仍具有1 300.0 mA·h/g的高比容量。
1.2 导电物包覆改性Co9S8
1.2.1 碳包覆改性Co9S8碳包覆不仅可以有效地提高Co9S8电极材料的导电性能,而且能够抑制Co9S8纳米颗粒的聚集。另外,碳材料所具有的弹性特征还可以缓冲Co9S8电极在充放电过程中的体积变化,维持结构稳定性,进而提高其倍率性能、循环稳定性和可逆比容量[14,24-31]。
2015 年,Y.Zhou 等[25]通过溶剂热反应,经高温煅烧将Co9S8纳米颗粒负载在无定形碳包覆的多壁碳纳米管(MWCNTs)上,成功合成了MWCNT@a-C@Co9S8纳米复合材料(见图4)。无定形碳夹在Co9S8和多壁碳纳米管之间可以增加MWCNTs上硫化物的负载量;高导电性MWCNTs使Co9S8具有良好的电化学性能。该纳米复合材料在电流密度为0.1 A/g 时,初始充电比容量为988.0 mA·h/g,库伦效率为70.7%。MWCNT@a-C@Co9S8在电流密度为1.0 A/g时,循环120次后可逆比容量为662 mA·h/g,远高于Co9S8纳米颗粒(85.0 mA·h/g)和MWCNT@Co9S8纳 米 复合材料(337.0 mA·h/g)。 MWCNT@a -C@Co9S8在电流密度为0.1、0.2、0.5、1.0、2.0、5.0 A/g时,可逆比容量分别为878.0、823.0、765.0、697.0、646.0、492.0 mA·h/g,当电流密度回复到0.1 A/g 时,可逆比容量为938.0 mA·h/g。当在电流密度为2.0 A/g 时循环700 次后,MWCNT@a-C@Co9S8的可逆比容量仍可保持在1 065.0 mA·h/g。与Co9S8和MWCNT@Co9S8材料相比,MWCNT@a-C@Co9S8纳米复合材料显示出优异的倍率性能和循环稳定性。

图4 MWCNT@a-C@Co9S8纳米复合材料的合成示意图[25]
2016年,G.Qu等[28]通过简单的两步法,即碳化聚多巴胺(PDA)包覆的金属配位聚合物(MCPs)和硫化过程,合成了多孔碳纤维包覆的Co9S8纳米颗粒(Co9S8@C)。在电流密度为0.1C(1.0C=539.0 mA/g)时,初始放电比容量为1 565.0 mA·h/g,循环100次后仍有872.0 mA·h/g。在倍率性能的测试中,在电流密度为0.1、0.2、0.5、1.0、2.0、5.0 A/g时,放电比容量分别为982.0、893.0、845.0、710.0、586.0、318.0 mA·h/g,高于纯Co9S8电极的放电比容量。当电流密度回到0.1C时,又可回复到932.0 mA·h/g 的高比容量。结果表明,该复合电极具有良好的循环稳定性和倍率性能。
2017 年,M.Lu 等[30]开发了一种基于液相的“热注射”合成方法。通过该方法合成了无定形碳和石墨烯共同包覆的中空Co9S8纳米颗粒,其具有双重保护层的结构可以有效缓冲Li+脱嵌过程中Co9S8纳米颗粒的体积变化。目前为止,很少有探究温度变化对Co9S8电化学性能的影响。因此,该课题组在温度为20~70 ℃的条件下,对Co9S8进行充放电测试。在电流密度为200.0 mA/g(30 ℃)时,首次放电和充电比容量分别为1 085.0、714.7 mA·h/g。在电流密度为500.0 mA/g(70 ℃)时,循环100 次后的可逆比容量为910.0 mA·h/g;而在1 000.0 mA/g(70 ℃)时,循环200次后可逆比容量为622.0 mA·h/g。同时,探究了Co9S8的可逆比容量随温度的变化趋势。结果表明,可逆比容量随着测试温度的升高而增加。此外,Co9S8的电荷转移阻抗随温度升高而降低。Co9S8优异的倍率特性以及高低温性能,使其成为很有应用前景的动力锂离子电池负极材料。
2018 年,J.Huang 等[14]成功地合成了直径为40~60 nm 的多孔碳包覆的Co9S8纳米复合材料(C-CS)。该电极材料在电流密度为100.0 mA/g时,首次放电和充电比容量分别为1 243.0、877.0 mA·h/g;在电流密度为2.0 A/g 时,循环400 次后保留了476.0 mA·h/g 的比容量。在倍率性能的测试中,该电极材料在6.4 A/g 的电流密度下仍有841.0 mA·h/g 的高比容量。其良好的倍率性能和循环稳定性可归因于诸多方面:多孔结构有利于电解液的渗透和Li+扩散;Co9S8纳米颗粒上的薄碳层增强了电导率;Co9S8纳米结构缩短Li+扩散距离。
1.2.2 氮掺杂碳包覆改性Co9S8研究表明,N 元素掺杂碳材料具有以下优点[32-34]:①N 元素提供的额外孤对电子可以提高碳材料的电子电导率;②N元素掺杂的碳材料不仅可以提供更多的活性点和成核点(有效抑制活性颗粒的无限长大和团聚),而且可以有效增强碳层和活性物质的结合力以及电解液对活性物质和碳层界面的浸润能力,同时使碳层对活性物质包覆得更均匀;③N 元素的掺杂可以使碳材料产生缺陷,缺陷有利于Li+在碳材料和活性物质的界面进行扩散。另外,采用N 元素掺杂的碳包覆Co9S8可以增强S 原子和碳材料之间的结合力,从而提高Co9S8复合电极材料的循环稳定性。
2016 年,J.Mujtaba 等[32]通过一种简便的方法,以ZIF-67 为前躯体,氩气气氛中与硫粉在600 ℃下硫化煅烧,成功地将Co9S8纳米颗粒包裹在含有氮掺杂的介孔碳网(NMCN)中,合成了Co9S8@NMCN 纳米复合材料。Co9S8@NMCN 在电流密度为0.1 A/g时,初始放电和充电比容量分别为1 705.0、1 125.0 mA·h/g,首次库仑效率为66.0%。循环80 次后可保留988.0 mA·h/g 的比容量,且具有良好的倍率性能。
2017年,P.Y.Zeng等[33]同样以ZIF-67为前驱体、乙硫醇为硫源,通过原位热解和硫化工艺成功合成了氮掺杂的碳空心球包覆Co9S8(Co9S8/N-C),其表现出良好的储锂性能和循环稳定性。在电流密度为1.0C(1.0C=544 mA/g)时,循环400 次后放电比容量为784.0 mA·h/g。即使在电流密度为4.0 C 时,所制备的Co9S8/N-C仍具有518.0 mA·h/g的放电比容量。
通过形貌和组分调控,极大地改善了Co9S8电极材料导电性能低、循环过程中体积变化大、颗粒团聚以及在电解液中溶解导致容量衰减快等劣势。这些改良手段促进了Co9S8在锂离子电池领域的研发,同时也为CoS2、CoS、Co3S4以 及Co1-xS 电 极 材料的进一步研发与优化提供了参考价值。
2 CoS2负极材料研究进展
CoS2由于电子电导率较高、热稳定性好以及成本低,成为锂离子电池负极材料的研究热点。CoS2的晶体结构见图5(a),空间群为T6 h(Pa,No.205),1 个晶胞中有4 个Co 原子和8 个S 原子,每个Co 原子与周围的6 个S 原子形成八面体配位(见图5(b)),每个S 原子与周围3 个Co 原子和1 个S 原子形成四面体配位(见图5(c))[34]。

图5 CoS2的结构及配位模型图[34]
CoS2理论比容量为870.0 mA·h/g[35],这不仅远高于目前所使用的石墨材料(372.0 mA·h/g),同样高于Co9S8电极材料的理论比容量。CoS2与Li+的充放电反应方程式为:CoS2+4Li++4e-↔Co+2Li2S。然而,CoS2电极材料与Co9S8一样存在电子电导率低、充电放电过程中严重的体积变化而引起的材料粉化、在电解液中溶解引起容量衰减等问题。
研究者主要采取以下方法来解决这些问题:①通过形貌控制构建新型纳米结构,如中空结构、核-壳结构等,获得更大的比表面积以缩短Li+脱嵌的距离,提高反应速率来减缓充放电过程中体积膨胀;②通过碳包覆提高材料的电子电导率、抑制充放电过程中体积膨胀、减缓材料溶解,这有利于改善材料的倍率和循环性能。
2.1 形貌调控改性CoS2
2011 年,Q.H.Wang 等[36]认为,充放电电压范围是影响锂离子电池循环性能的关键因素之一。当放电电压为1.6 V 时,CoS2脱嵌锂的反应方程式为:CoS2+xLi++xe-↔LixCoS2。在这种可逆反应过程中,材料的结构几乎不被破坏。而当放电电压下限为0.02 V 时,其脱嵌锂的反应方程式为:CoS2+4Li++4e-↔Co+2Li2S,材料结构坍塌。为防止CoS2结构在充放电过程中被破坏,该课题组以溶剂热法合成均匀的CoS2中空微球,并进行电化学测试。在电流密度为100.0 mA/g、电压为0.01~3.00 V 时,首次放电比容量约为1 210.0 mA·h/g,循环40 次后约保留了320.0 mA·h/g 的可逆比容量。结果表明,中空结构能够抑制CoS2在充放电过程中结构破坏。
2015 年,R.C.Jin 等[37]在没有任何表面活性剂或模板剂的情况下,采用溶剂热法成功地制备由超薄纳米片构成的分层蠕虫状CoS2纳米材料,其具有超高的比表面积,可以有效地缩短Li+的扩散路径,并减缓Li+脱嵌过程中的体积变化,从而产生优异的储锂性能。电化学测试结果表明,在电流密度为100.0 mA/g 时,分层蠕虫状的CoS2负极材料的初始充放比容量分别为1 073.0、1 416.0 mA·h/g,库仑效率为75.8%,循环100 次后仍保留了883.0 mA·h/g的放电比容量。在电流密度为2 000.0 mA/g 时,循环50 次后也可以提供高达501.0 mA·h/g 的放电比容量,充分显示出良好的循环性能和优异的倍率性能。交流阻抗谱测试进一步显示出CoS2电极材料具有良好的循环稳定性能。
2016 年,L.Yu 等[38]通过简单的两步扩散控制策略,制备了由纳米尺寸气泡状CoS2构成的分级中空棱柱。如图6 所示,首先通过转化过程合成了由互相连接的纳米多面体构成的具有中空棱柱状的ZIF-67;然后通过硫化反应和热处理将ZIF-67 结构单元转化为由CoS2气泡状中空颗粒构成的复杂中空棱柱。所获得的CoS2中空棱柱作为锂离子电池的负极材料,在0.05~3.00 V 的电压范围和200.0 mA/g 电流密度下进行恒电流充放电测试。结果表明,初始放电和充电比容量分别为1 542.0、861.0 mA·h/g。CoS2中空棱柱在电流密度为5 000.0 mA/g 时,可逆比容量仍可保留到470.0 mA·h/g。此外,当电流密度最终降至200.0 mA/g 时,容量迅速回复到864.0 mA·h/g,与初始时比容量910.0 mA·h/g 相近,这表明该电极材料具有优异的倍率性能。

图6 CoS2纳米气泡中空棱柱的合成示意图[38]
CoS2中空棱柱在电流密度为1 000.0 mA/g 时,循环200 次后的可逆比容量约为737.0 mA·h/g。CoS2中空棱柱的优异电化学性能主要得益于独特的结构,一级纳米中空结构超薄的壁可以大大缩短Li+的扩散距离,从而改善电化学动力学性能。另外,由泡状的亚单元构成的分级中空棱柱状的CoS2提供的多级中空内壁可以减缓材料充放电过程中体积变化,材料结构完整,表现出良好的循环性能。
2018 年,H.C.Wang 等[39]采用Co-MOC 模板,通过自模板法成功制备了由氮掺杂的碳(NCH)包覆CoS2颗粒形成的核-壳结构组成的十六面体CoS2@NCH(见图7)。CoS2@NCH 的循环伏安曲线中还原峰分别为1.00、1.28、1.59 V,而氧化峰分别为1.89、2.34 V。其中,在1.00 V 处的还原峰主要受到固体电解质界面膜(SEI)形成的影响。在电压为0.005~3.000 V、电流密度为1.0 A/g 时,CoS2@NCH的首次放电和充电比容量分别为1 088.1、569.0 mA·h/g(库仑效率为52.3%)。该电极材料在电流密度为1.0 A/g下循环1 000次后,能保持778.0 mA·h/g的高可逆比容量;在20.0 A/g 的高电流密度下具有220.0 mA·h/g 的高比容量,并且当电流密度回复到2.0 A/g 时,其可逆比容量与循环前几乎相同,表现了出色的倍率性能。CoS2@NCH 复合电极材料表现出优异的电化学性能主要归因于三个方面:①氮掺杂的多孔碳外壳相互连接,形成具有高导电性能的骨架结构,便于电子的快速传递,并防止材料结构坍塌;②纳米级CoS2颗粒缩短了Li+传输距离,提供了额外的电化学活性位点;③多孔碳壳上的介孔利于Li+进入颗粒内部,而颗粒间隙形成的介孔不仅使电解液完全渗透到电极材料中,而且还可以缓解体积膨胀的影响,以确保电极材料的完整性。

图7 CoS2@NCH 的合成示意图[39]
2.2 导电物包覆改性CoS2
2.2.1 碳包覆改性CoS2二维(2D)石墨烯因具有超高的电子电导率、大的比表面积、好的柔韧性、优异的化学和热稳定性等优点被用于修饰锂离子电池负极材料CoS2,但是,石墨烯和CoS2之间的相互作用机理尚不明确,这引起了诸多学者极大的兴趣。B.Qiu 等[40]为了区别还原氧化石墨烯(RGO)和CoS2各自在CoS2/RGO 复合材料中的贡献,将CoS2/RGO 与同等条件下合成的CoS2和RGO 进行循环性能比较,在100.0 mA/g 的电流密度下循环20 次后,CoS2/RGO 电极材料保留了690.0 mA·h/g的比容量,而CoS2、RGO 电极材料仅保留了250.0、150.0 mA·h/g 的可逆比容量,证实了CoS2/RGO 可逆比容量的增加主要是RGO 和CoS2之间的协同效应。此外,这种协同效应导致CoS2/RGO 复合材料显示出比CoS2高得多的可逆比容量。
与上述二维石墨烯片不同,由二维石墨烯片组装的三维石墨烯网络不仅具有二维石墨烯片的固有特性,而且与电极材料复合后材料机械强度大,电极/电解液接触面积大,Li+扩散路径短。为了探究三维石墨烯网络结构对CoS2电极材料的影响,F.Fu等[41]通过水热法合成了具有三维分层结构的CoS2/RGO 复合材料(3DCG)。如图8所示,首先GO 片由于强烈的亲水性和静电排斥作用分散在水中;在水热过程中GO 片被还原后变得疏水,部分被还原的GO 随着含氧官能团的减少变得疏水;随着水热反应的进行,借助疏水性和π-π堆积作用力,被还原的GO 形成3D 自由堆积;最后,随着这两种作用力的增强形成三维交联的RGO网络。同时,吸附在GO 表面上的Co2+与硫源反应生成CoS2颗粒,并通过冷冻干燥进一步处理得到3DCG。与CoS2和RGO相比,3DCG负极材料具有优异的电化学性能:在电流密度为100.0 mA/g 下,首次放电比容量为1 579.0 mA·h/g,循环150 次后可保持1 245.0 mA·h/g 的放电比容量;即使在4 000.0 mA/g的电流密度下,仍保留了306.0 mA·h/g 放电比容量。其优异的电化学性能可以归因于独特的三维多孔结构,其中RGO 网络可以保证复合材料的高导电性,减缓循环期间CoS2颗粒体积变化,并缩短Li+扩散距离,从而提高其循环和倍率性能。与文献[41]类似,S.Tao等[42]也合成了具有分层结构的石墨烯修饰的CoS2纳米球复合材料(CoS2/G)。该电极材料在电流密度为500.0 mA/g时,1 000次循环后下获得约400.0 mA·h/g的放电比容量。此外,在电流密度为3 500.0 mA/g时,还能提供约398.0 mA·h/g的高可逆比容量。

图8 3DCG 的合成示意图[41]
2018 年,W.H.Zhang 等[43]通过冷冻干燥法和水热处理过程,以NaCl 为模板剂、葡萄糖为碳源,合成了海绵状的CoS2/C 复合材料。碳的良好电子电导性和多孔结构的协同作用,使CoS2/C 的电化学性能显著提高,多孔结构可以为材料在充放电过程中的体积膨胀提供空间,同时为Li+/电子的传输提供通道。电化学结果表明,海绵状的CoS2/C 复合材料具有优良的储锂性能。该复合材料在电流密度为100.0 mA/g 时,初始放电和充电比容量分别为1 420.0、796.5 mA·h/g(库仑效率为56.1%);在电流密度为500.0 mA/g 时,循环120 次后具有610.0 mA·h/g 的比容量;即使在2.0 A/g 的高电流密度下,也有391.5 mA·h/g 高的比容量。此外,在这项工作中开发的冷冻干燥和水热工艺技术可用于构建许多其他高容量金属硫化物复合材料,也可应用于钠离子电池的电极材料领域。
2.2.2 氮掺杂的碳包覆改性CoS22015 年,Q.F.Wang 等[44]通过使用MOF 模板制备了高性能的新型多孔碳/CoS2复合材料。该合成方案和透射电镜如图9 所示。选择具有Co(II)金属离子和含N 的甲基咪唑配体的ZIF-67 作为MOF 模板,经低温硫化后,得到超小CoS2纳米颗粒均匀地分散在富含氮的多孔碳基中。多孔碳/CoS2复合材料表现出良好的储锂性能,在电流密度为100.0 mA/g 时,循环50 次后可保持560.0 mA·h/g 的可逆比容量。即使在电流密度高达2 500.0 mA/g 时,也获得410.0 mA·h/g的可逆比容量。该电极材料拥有良好的电化学性能主要是由于超小的CoS2颗粒和MOF 模板衍生的薄的富含氮的多孔碳层的协同作用。

图9 新型多孔碳/CoS2复合材料的合成以及中间产物与最终产物的透射电镜[44]
同年,W.D.Qiu 等[45]采用一种简便且无模板的溶剂热法,制备了蛋黄-壳CoS2和氮掺杂的石墨烯片(NG)的复合材料(CoS2@NG)。NG 不仅可以作为缓冲基底,而且可以作为导电基体,能够使材料颗粒得到均匀分散,保证材料整体上具有高的电子电导率;蛋黄-壳的中空结构有利于Li+传输,缓解体积膨胀。制备的复合材料可以直接作为锂离子电池的柔性负极材料,不需要任何黏合剂、炭黑导电剂和集流体。这种柔性电极在电流密度为100.0 mA/g 时,首次放电比容量为1 120.0 mA·h/g,循环150 次后的放电比容量为882.0 mA·h/g,远高于同等条件下合成的蛋黄-壳CoS2和中空CoS2负极材料的放电比容量。这种双重保护的策略提供了一种有效且通用的方法来改善体积变化大的高比容量电极材料的循环和倍率性能,从而为设计和制备其他柔性的新型电子器件提供了可能性。
2017 年,J.T.Zhang 等[46]通 过ZIF-67(Co 的MOF)直接热解和硫化处理两步法,在氮掺杂的碳纳米管空心骨架(NCNTF)中嵌入CoS2纳米颗粒,合成了CoS2/NCNTF 纳米复合材料。所得的互连碳骨架结构可以使CoS2超细纳米颗粒分散良好、导电性提高、结构稳定性增强,其显著的结构和组成特点,使CoS2/NCNTF 纳米复合材料表现出良好的电化学性能。CoS2/NCNTF 复合材料在电流密度为1.0 A/g 时,初始放电和充电比容量分别为1 187.0、927.0 mA·h/g(库仑效率约为78.0%),循环160 次后保持了937.0 mA·h/g 的放电比容量;在电流密度分别为0.2、0.5、1.0、2.0 A/g 时,放电比容量分别约为1 191.0、952.0、779.0、615.0 mA·h/g,即使在电流密度为5.0 A/g 时,该电极材料也能提供高达439.0 mA·h/g 的放电比容量,具有出色的倍率性能。CoS2/NCNTF 所具有的优异电化学性能主要归功于其独特的结构和组成,超细CoS2纳米颗粒嵌入碳骨架中的结构不仅能够缩短Li+的传输距离,而且还能使活性材料和电解液之间充分接触,加快电化学反应。另外,由互连的碳纳米管组成的中空结构可以为CoS2在循环过程中的体积膨胀提供足够的空间。
2.3 氧化物包覆改性CoS2
2017年,L.Fang等[47]首先合成了Co6Al2O3(OH)16·4H2O 纳米片,以此为前驱体,在低温硫化后获得了嵌入氧化铝纳米片的CoS2纳米颗粒复合材料,CoS2NP/Al2O3NSs 的合成示意图见图10。多孔Al2O3纳米片支撑和分散CoS2纳米颗粒,减轻活性物质的聚集并减缓电解液中的酸对活性物质的侵蚀,还增加电解液与活性物质的接触面积并有效缓冲循环过程中的体积变化。此外,厚度较薄的二维结构也缩短离子的扩散距离,增大活性物质与电解液的接触面积。CoS2NP/Al2O3NSs 复合材料的所有这些优点使其具有良好的储锂性能。CoS2NP/Al2O3NSs 在电流密度为100.0 mA/g 时,初始放电比容量为1 150.0 mA·h/g,循环150 次后可达到626.0 mA·h/g,与CoS2纳米颗粒(CoS2NPs)相比,其具有较好的循环稳定性。另外,在电流密度为100.0、500.0、1 000.0、2 000.0 mA/g 时,CoS2NP/Al2O3NSs 能提供750.0、610.0、560.0、480.0 mA·h/g 的可逆比容量。当电流密度降至100.0 mA/g 时,容量回复到约为720.0 mA·h/g,凸显其较好的倍率性能。同时,为了了解Al2O3载体对复合材料电化学性能的贡献,该课题组还测试了Al2O3纳米片电化学性能,发现Al2O3纳米片的比容量较低,证实了复合材料可逆比容量的增加主要来自于活性材料CoS2纳米颗粒和Al2O3纳米片多孔结构的相互作用。

图10 CoS2 NP/Al2O3 NSs 的合成示意图[47]
3 CoS 负极材料研究进展
CoS 作为金属硫化物的重要成员之一,由于具有高理论比容量(590.0 mA·h/g)而被广泛研究。然而,与上述两种硫化钴类化合物相似,CoS 同样存在电子电导率低、充电放电过程中严重的体积变化而引起的材料粉化和在电解液中溶解引起容量衰减等问题。
3.1 碳包覆改性CoS
针对其暴露的缺陷,研究者主要采取碳包覆对CoS 进 行 改 性。2013 年,Y.Gu 等[48]合成了石墨烯包覆的CoS 复合材料,并与同等条件下制备的CoS 微球进行对比。CoS/石墨烯复合材料具有较高的可逆比容量和较好的循环稳定性,在电流密度为62.5 mA/g 时,初始放电比容量为1 669.0 mA·h/g,循环40 次后保留了749.0 mA·h/g 的可逆比容量,而CoS微球则从初始的1 433.0 mA·h/g 降到循环40 次后的241.0 mA·h/g。CoS/石墨烯复合材料良好的电化学性能与石墨烯的存在有关。
2016 年,H.J.Wang 等[49]报道了碳纳米管(CNTs)修饰CoS 纳米材料。电化学测试结果显示,CoS/CNTs 纳米复合材料在电流密度为100.0 mA/g 时,循环50 次后仍保持了780.0 mA·h/g 的放电比容量,即使在电流密度高达1 000.0 mA/g 时,仍可保持550.0 mA·h/g 的放电比容量;当电流密度回到100.0 mA/g 时,复合材料也可以获得736.0 mA·h/g 的高放电比容量。材料良好的电化学性能与碳纳米管优异的电子电导率、碳纳米管抑制材料坍塌和材料颗粒的溶解有关。
同年,Y.B.Tan 等[50]通过水热法和硫化过程,在RGO 表面上负载均匀分布的CoS 纳米颗粒,由于RGO 的存在,CoS 纳米颗粒不会发生团聚。这种纳米结构更易于缓解Li+脱嵌引起的CoS 体积变化。该复合材料CoS NFs-rGO 在电流密度为100.0 mA/g时,初始放电和充电比容量分别为1 869.0、1 299.0 mA·h/g,循环100 次后保持了939.0 mA·h/g 的高可逆比容量。此外,当电流密度为2 000.0 mA/g 时,CoS NFs-rGO 复合材料的相应放电比容量为570.0 mA·h/g,当电流密度回到100.0 mA/g 时,则回复到1 065.0 mA·h/g以上,这表明具有良好的倍率性能。
3.2 异种元素掺杂碳包覆改性CoS
聚丙烯腈(PAN)是合成碳基材料的典型烃类化合物,而静电纺丝技术是将PAN 制成一维纳米纤维的有效方法之一。同时,PAN 还具有许多CN 官能团,这使其在碳化过程中存在氮掺杂。2016 年,Y.M.Chen 等[51]利用PAN 纳米纤维的特征,通过静电纺丝技术和水热法合成了氮掺杂的碳包覆CoS 中空纳米管复合材料(见图11)。该复合电极材料作为锂离子电池的负极具有较好的倍率性能和较高的循环稳定性。复合材料在电流密度为1.0 A/g 时,初始放电和充电比容量分别为1 030.0、705.0 mA·h/g。在电流密度为0.5、1.0、2.0、3.0、4.0 A/g 时,分别具有1 337.0、1 091.0、877.0、766.0、641.0 mA·h/g 的高比容量。此外,该复合电极材料在电流密度为2.0 A/g 时,循环1 400次后还可保留671.0 mA·h/g的高比容量。
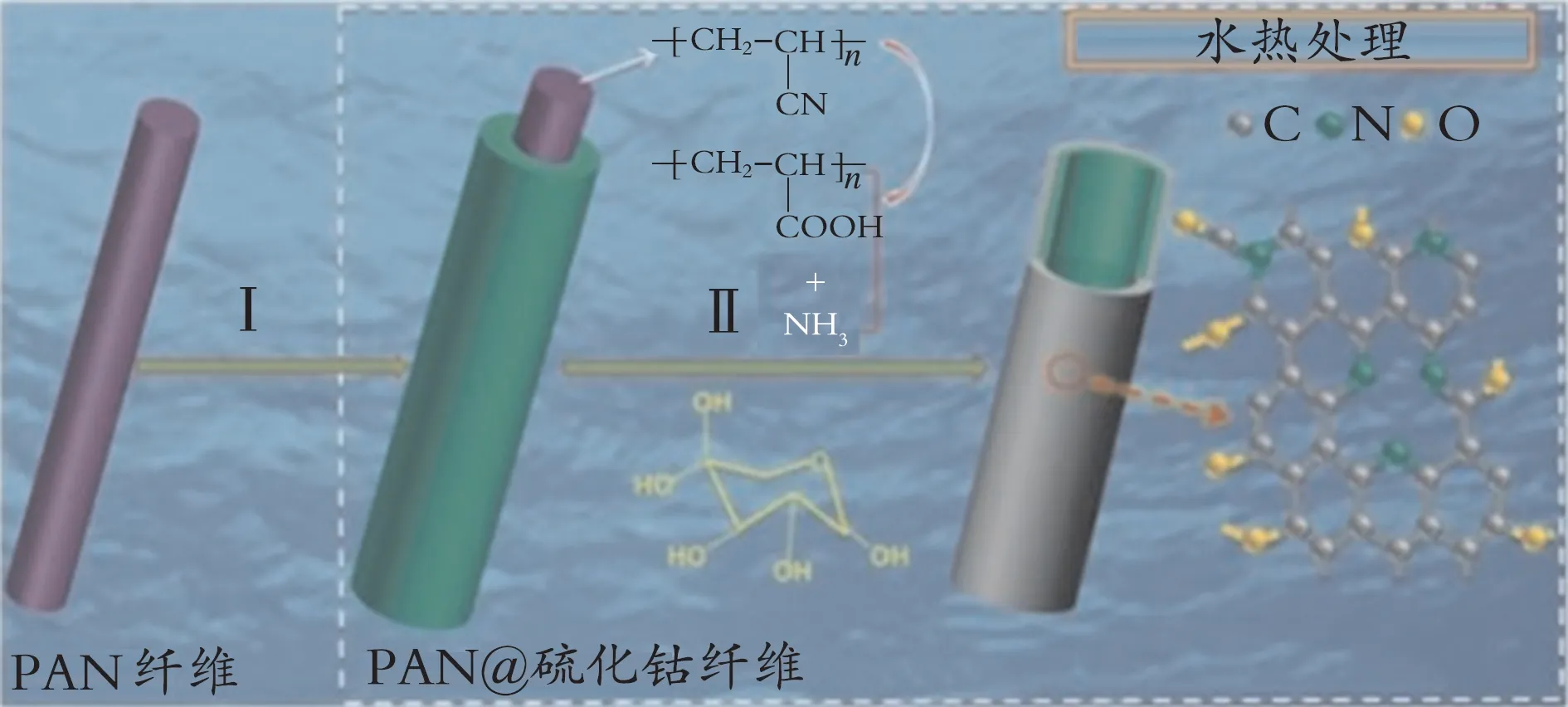
图11 氮掺杂的碳包覆CoS 中空纳米管复合材料的合成过程示意图[51]
2018 年,Y.F.Yao 等[52]通过电沉积和硫化等方法,将氮和硫掺杂碳壳包覆多孔CoS 纳米片分散在石墨烯泡沫上,通过可控制的前躯体,获得了3 种形态的复合材料:具有空隙空间和完整碳壳结构的多孔CoS 纳米片(ClPure);没有空隙空间,但具有完整碳壳结构的多孔CoS 纳米片(BrPure);没有空隙空间且具有不完整碳壳结构的多孔CoS 纳米片(ClPure-CHO)。以此来研究空隙空间、碳壳和内孔结构对电化学性能的影响。CoS 纳米片的空隙空间和多孔结构有利于提高Li+的扩散速率,而空隙空间和完整的碳壳结构可以提高电极材料的循环稳定性。同时,氮和硫掺杂的碳壳还可以增加电极材料的导电性,进而提高其倍率性能。基于以上空隙空间、碳壳结构和多孔纳米片结构的诸多优点,ClPure 复合电极材料在电流密度为0.1C(1.0C=600.0 mA/g)时,初始放电和充电比容量分别为686.5、567.6 mA·h/g,循环100 次后仍能提供481.7 mA·h/g 的可逆比容量。
4 Co3S4负极材料研究进展
Co3S4具有尖晶石结构,空间群为Fd3m,是一种较为特殊的磁性材料,在特定的温度下会发生磁性的转变[53]。由于其具有独特的磁性以及催化性能,因此在电催化、光催化和超级电容器等领域得到了广泛的研究与应用[54-59]。Co3S4电极材料的理论容量约为702.8 mA·h/g,高于CoS 和Co9S8,其充放电反应为:Co3S4+8Li++8e-↔3Co+4Li2S,可以作为具有优良性能的锂离子电极材料[60]。但是,目前在锂离子电池领域的研究还相对较少。
2013 年,N.Mahmood 等[60]通过简易的水热工艺,将石墨烯引入Co3S4体系,合成了Co3S4纳米管(NTs)和石墨烯的复合材料(Co3S4/G),从而提高了Co3S4的导电性和循环稳定性。电化学性能测试表明,该复合材料作为锂离子电池的负极材料表现出比Co3S4更好的电化学性能。合成的Co3S4/G 复合材料在电流密度为0.2C(1.0C=702.8 mA·h/g)时,初始放电和充电比容量分别为2 151.0、1 449.0 mA·h/g,循环100 次后保留了720.0 mA·h/g 的高放电比容量。复合材料良好的电化学性能,主要是基于Co3S4的多孔结构以及石墨烯的导电性和缓冲特性,这使Li+和e-能够快速迁移并减缓材料体积膨胀。
2015 年,Y.C.Du 等[61]以冷冻干燥和水合肼处理的方式,设计并制备了嵌入石墨烯片内的Co3S4多孔纳米片复合材料,Co3S4-PNS/GS 复合材料的合成示意图见图12。

图12 夹层型Co3S4-PNS/GS 复合材料的合成示意图[61]
相比Co3S4-PNS,Co3S4-PNS/GS 复合材料具有坚固的三维三明治夹层结构和多孔纳米结构,表现出了更好的电化学性能。在电流密度为0.5 A/g时,复合材料初始的放电和充电比容量分别为1 210.0、816.0 mA·h/g(库仑效率为67.4%),循环200 次后的可逆比容量为710.0 mA·h/g。当电流密度达到20.0 A/g 时,其可逆比容量为295.0 mA·h/g,而当电流密度回复至0.5 A/g 时,其可逆比容量也回复到了669.0 mA·h/g,与起始时的比容量接近,表现出了良好的倍率性能。
过渡金属氧化物作为锂离子电池的负极材料时,由于可以提供高理论容量和对Li+的高化学活性而已被广泛地探究与应用。其中,Co3O4具有较高的理论容量(890.0 mA·h/g),是一种很有前途的负极材料,但是由于在放电和充电过程中体积变化较大,导致与其对应的循环稳定性较差。然而,金属硫化物与金属氧化物相比,具有相对较弱的离子键,更易发生可逆的充电和放电反应,导致金属硫化物拥有更高的库仑效率和较好的循环稳定性。因此,2017 年,X.Wang 等[62]针对这两种材料的不同优缺点,制备了在泡沫镍上生长的三维异质Co3O4@Co3S4纳米阵列作为锂离子电池的无黏结剂电极材料Co3O4@Co3S4NAs,其合成示意图见图13。该复合材料比纯Co3O4和Co3S4纳米片表现出了更良好的导电性和较高的可逆容量,在电流密度为200.0 mA/g 时,初始放电和充电比容量分别为1 903.1、1 350.5 mA·h/g,初始库仑效率高达82.25%,远远高于其他钴氧化物或硫化物复合电极材料,循环40 次后可逆比容量仍有1 050.0 mA·h/g。即使在电流密度高达1 500.0 mA/g 时,其容量也可达到808.1 mA·h/g。Co3O4@Co3S4NAs 拥有较好的储锂性能主要归因于Co3O4和Co3S4之间的协同效应。同时,具有三维结构的泡沫镍提供有效的离子传输通道和较大的比表面积以增强其电化学性能。但是,Co3O4@Co3S4NAs 复合材料的长周期循环寿命未被探讨,因此这种具有异质结构的电极材料仍然面临较大的难题,需要进一步完善。
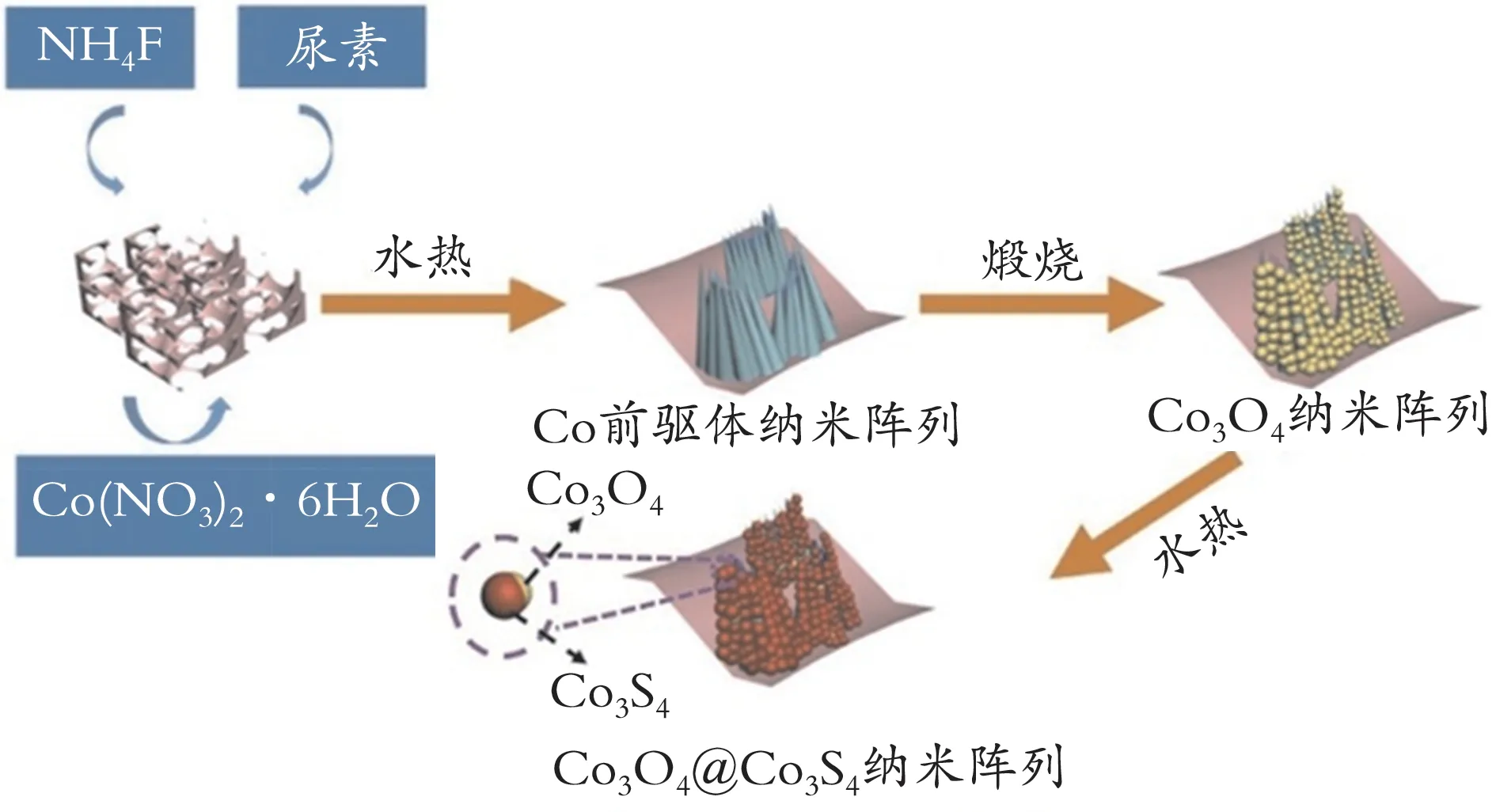
图13 Co3O4@Co3S4 NAs 复合材料的合成示意图[62]
5 Co1-xS 负极材料研究进展
Co1-xS 晶体结构属于六方晶系,空间群为P63/mmc[8]。与Co3S4相似的是,在锂离子电池领域的相关报道较少,但从已有的研究成果中不难看出Co1-xS负极材料拥有高达682.6 mA·h/g 的理论比容量,其锂化方程式为:Co1-xS+2Li++2e-↔1-xCo+Li2S,因此在锂离子电池领域仍有不断探究的价值。
2014 年,S.M.Liu 等[63]以柠檬酸三钠(Na3Cit)为螯合剂,通过水热法合成了新型的三维花状分层Co1-xS 纳米复合材料,其合成示意图见图14。

图14 三维花状分层Co1-xS 纳米复合材料的合成示意图[63]
Na3Cit作为配体和结构导向剂,在驱动纳米片组装成花状分层Co1-xS结构中起着至关重要作用,能有效控制花状Co1-xS 结构的形成。此外,还研究了Na3Cit浓度、有机添加剂和反应时间对产物形貌的影响,根据实验结果提出了其可能的生长机理。制备的三维花状分层Co1-xS 纳米复合材料作为锂离子电池负极材料,当电压为0.01~3.00 V、电流密度为50.0 mA/g 时,初始放电比容量可达1 244.0 mA·h/g,而在100.0 mA/g的电流密度下循环150次后,可逆比容量仅剩485.0 mA·h/g,虽然比同等条件下合成的Co1-xS微球要高,但循环寿命较短,容量衰减较快,且在经过200次充放电循环后,该三维花状结构被完全破坏。
2017 年,J.Lin 等[64]采用溶剂热法合成了由纳米Co1-xS 和稻壳衍生的活性炭(BC)复合的多孔微米材料(Co1-xS/BC)。Co1-xS/BC 复合材料作为锂离子电池负极材料,在电流密度为0.1 A/g 时,循环120 次后,保留了约630.0 mA·h/g 的可逆比容量,容量衰减小于0.7%。相比与同等条件下合成的Co1-xS 电极材料,该复合材料表现出了优异的储锂和倍率性能,主要可归因于BC 的引入,不仅阻止Co1-xS纳米颗粒的团聚,而且减缓了Co1-xS 纳米颗粒在充放电循环期发生的体积变化。此外,BC 还可以增强Co1-xS 纳米颗粒的导电性能,提高其脱嵌锂反应速率。
2018 年,C.F.Dong 等[65]利用图15 所示的合成方案,首次通过控制2-甲基咪唑的量,以溶剂热法制备了均匀且具有中空结构的Co1-xS 的纳米球前驱体。然后,通过直接煅烧或对得到的前驱体进行PPy 涂层和煅烧,选择性地制备出Co1-xS、Co1-xS/C和Co1-xS@C 这三种材料。其中Co1-xS/C 复合材料由超细Co1-xS 纳米粒子嵌入氮掺杂多孔碳的中空纳米球当中形成,而Co1-xS@C 复合材料则是Co1-xS 纳米粒子完全被外部的无定形碳层所包覆而形成。

图15 Co1-xS/C 的合成示意图及透射电镜[65]
Co1-xS/C 复合材料作为锂离子电池的负极材料,在电流密度为500.0 mA/g 时,循环100 次后保持了559.0 mA·h/g 的可逆容量,与其他两个样品相比,表现出了更高的可逆比容量和更好的循环稳定性。其较好的电化学性是因为:①复合材料独特的微纳结构可以保证其在循环过程中结构稳定,嵌入氮掺杂多孔碳的中空纳米球(低密度、大比表面积)中的Co1-xS/C 纳米颗粒不仅可以缩短Li+的传输距离,而且可以缓冲充放电过程中的体积膨胀;②碳包覆层可以提高该电极材料的稳定性和导电性;③醚类电解液可以减缓循环过程中间产物的溶解;④Co1-xS和碳之间的协同效应可以在一定程度上弥补Co1-xS 纳米颗粒本身的不足。此外,该新策略还具有简单、低成本等优点,并且可以用于制造其他微米、纳米硫化物电极材料,在钠离子和锂离子电池领域极具研究价值。
6 结论与展望
锂离子电池的快速发展对电极材料提出了更高要求。硫化钴化合物(CoS、CoS2、Co3S4、Co1-xS、Co9S8等)因高的比容量和良好的热稳定性成为很有应用前景的锂离子电池负极材料。但是,硫化钴化合物电子电导率低,充放电过程中材料体积膨胀、颗粒团聚以及在电解液中溶解导致容量衰减快。研究者主要采取以下方法来解决这些问题:①通过形貌控制构建新型纳米结构,获得更大的比表面积以缩短Li+脱嵌的距离,提高反应速率来减缓充放电过程中体积膨胀。②碳包覆,既能提高电极材料的导电性能,又能抑制充放电过程中体积膨胀,这有利于改善材料的循环和倍率性能;同时,引入碳材料也会减缓硫化钴化合物的溶解,延长材料的循环寿命。
硫化钴的脱嵌锂电位高使其安全性高,但是高的脱嵌锂电位也会降低其能量密度;另外,虽然硫化物的比容量高于商业化锂离子电池负极石墨,但是远低于硅基材料。所以,通过金属元素掺杂降低硫化钴的脱嵌锂电位,与更高比容量的负极材料复合,提高硫化钴的整体可逆比容量,这两方面以往研究的较少,是今后硫化钴研究的两个方向。

