抗富亮氨酸胶质瘤失活蛋白1 抗体相关脑炎临床分析
赵清青 戴淑娟 艾明达 陈玲 艾青龙
抗富亮氨酸胶质瘤失活蛋白1(LGI1)抗体相关脑炎是一种由LGI1 抗体介导的自身免疫性脑炎(AE)[1-2]。自2010 年Lai 等[3]首次报告抗LGI1 抗体相关脑炎以来,我国在2013 年确诊首例病例[4],此后越来越多的抗LGI1 抗体相关脑炎病例被报道。然而,在临床实践中由于部分患者临床表现不典型,极易误诊或漏诊。笔者对昆明医科大学第一附属医院神经内科近年收治的6 例抗LGI1 抗体相关脑炎患者的临床资料进行回顾分析,探讨其临床特点和诊疗经过,以期加强临床医师对该病的认识。
临床资料
一、诊断标准
根据2016 年Lancet Neurol发表的抗LGI1 抗体相关脑炎诊断标准[5],以及2017 年《中国自身免疫性脑炎诊治专家共识》[6],符合以下条件者确诊为抗LGI1 抗体相关脑炎:(1)急性或亚急性发病并呈进行性加重。(2)临床表现符合边缘性脑炎或面-臂肌张力障碍发作(FBDS)。(3)脑脊液白细胞计数正常或呈轻度淋巴细胞性炎症。(4)头部MRI 显示双侧或单侧颞叶内侧异常信号或无明显异常。(5)脑电图异常。(6)血清和(或)脑脊液LGI1 抗体呈阳性反应。(7)同时排除病毒感染、中毒、代谢紊乱、中枢神经系统肿瘤等原因引起的脑炎,以及其他自身免疫性脑炎。
二、临床特点
1.一般资料 选择2016 年9 月至2018 年4 月在昆明医科大学第一附属医院神经内科住院治疗且诊断明确的抗LGI1 抗体相关脑炎病例共6 例,男性3 例,女性3 例;年龄36 ~64 岁,平均50.33 岁;急性发病1 例、亚急性发病5 例;发病至确诊时间21 ~248 d,平均89.83 d。6 例患者中2 例有高血压病史、1 例曾与他人争吵(可能诱因)、1 例曾行脂肪瘤切除术,其余2 例既往体格健康;所有患者均否认传染病接触史或家族遗传史。
2.临床表现 (1)认知功能障碍:本组所有患者均存在认知功能障碍,其中5 例表现为近记忆力明显减退、2 例定向力障碍、4 例计算力下降。(2)癫发作:共4 例患者病程中出现发作,发作类型以全面性强直-阵挛发作(GTCS,3 例)或面-臂肌张力障碍(2 例)发作为主。(3)精神行为异常:1 例表现为幻觉、2 例呈现发作性语言混乱。(4)睡眠障碍:5 例出现睡眠障碍,3 例表现为维持睡眠障碍即易惊醒、2 例呈嗜睡状态。(5)自主神经功能障碍:尿频、大小便失禁和腹泻各1 例。(6)其他伴随症状:分别为乏力(1 例)、心悸(1 例)、头痛(1 例)、共济失调(1 例)或自动症(1 例)。(7)神经功能预后评分:入院时改良Rankin 量表(mRS)评分分别为5 分1 例、4 分1 例、3 分2 例、2 分2 例。
3.实验室检查 (1)血清学:4 例患者呈低钠血症(125.81 ~133.52 mmol/L)、3 例低氯血症(92.21 ~96.74 mmol/L)、3 例低钾血症(2.86 ~3.36 mmol/L)以及1 例低钙血症(2.06 mmol/L)。其中,2 例患者血清呼吸道九项检测提示肺炎支原体阳性;1 例肿瘤标志物癌胚抗原(CEA,8.92 ng/ml)和糖类抗原72-4(CA72-4,49.08 U/ml)异常,以及甲状腺抗体[甲状腺过氧化物酶(TPO)抗体(61.29 IU/ml)和甲状腺球蛋白(TG)抗体(204.40 IU/ml)]水平升高;1 例合并亚临床甲状腺功能减退症[促甲状腺激素(TSH)9.80 mU/L]。其余各项实验室指标如肝肾功能,以及血清免疫全套检测[抗核抗体(ANA)、抗中性粒细胞胞质抗体(ANCA)、抗磷脂抗体(APL)、类风湿因子(RF)抗体等]均于正常参考值范围。(2)脑脊液:本组患者入院后首次腰椎穿刺(未治疗前)颅内压125 ~180 mm H2O(1 mm H2O=9.81×10-3kPa),其中,1 例氯化物水平低于正常值(118.80 mmol/L)、1 例蛋白定量(1010.04 mg/L)和IgG(87.02 mg/L)水平升高。(3)LGI1 抗体:采用基于细胞底物实验(CBA)的间接免疫荧光法(IIF)对本组病例血清和脑脊液标本进行检测(北京协和医院实验室或北京海思特临床检验所),血清LGI1 抗体均呈阳性反应,其中4 例血清和脑脊液LGI1 抗体双阳性、4 例单纯脑脊液LGI1 抗体阳性(图1 ~4)。其他自身免疫性脑炎相关性神经细胞抗体如N-甲基-D-天冬氨酸受体(NMDAR)抗体、接触蛋白相关蛋白-2(CASPR2)抗体等呈阴性反应。
4.影像学检查 (1)脑电图:本组共有4 例患者脑电图异常,分别表现为边缘状态(2 例)、局灶性慢波(1 例)和起源于左侧颞叶的异常癫波(1 例)。(2)影像学:本组6 例患者入院后均行头部MRI 检查,3 例炎症性病灶位于海马和颞叶内侧,其中1 例同时行18F-FDG PET 检查,提示右侧海马局限性代谢增高,双侧尾状核、壳核和双侧背侧丘脑代谢相对增高,大脑皮质和小脑半球代谢呈轻度弥漫性减低。胸部CT 平扫显示2 例患者合并肺结节,1 例同时合并甲状腺结节、胸腺小结节及左乳腺小结节,随访期间结节无明显进展。
三、治疗及预后
2. 预后 本组患者共住院12 ~25 d,平均为18.33 d。出院后随访6 ~24 个月,平均15.17 个月,无死亡病例;mRS 评分2 分1 例、1 分3 例、0 分2 例。其中,3 例遗留记忆力障碍、1 例遗留面-臂肌张力障碍发作、2 例遗留低钠血症,1 例遗留睡眠障碍。

图1 例1 患者LGI1 抗体检测 CBA-IIF 法 ×200 1a 血清LGI1-IgG 呈阳性反应(1 ∶100) 1b 脑脊液LGI1-IgG 呈阳性反应(1 ∶3.20)Figure 1 Detection of LGI1 antibody in Case 1 CBA-IIF × 200 LGI1-IgG in the serum was positive (titer 1 : 100, Panel 1a).LGI1-IgG in cerebrospinal fluid was positive (titer 1:3.20, Panel 1b).
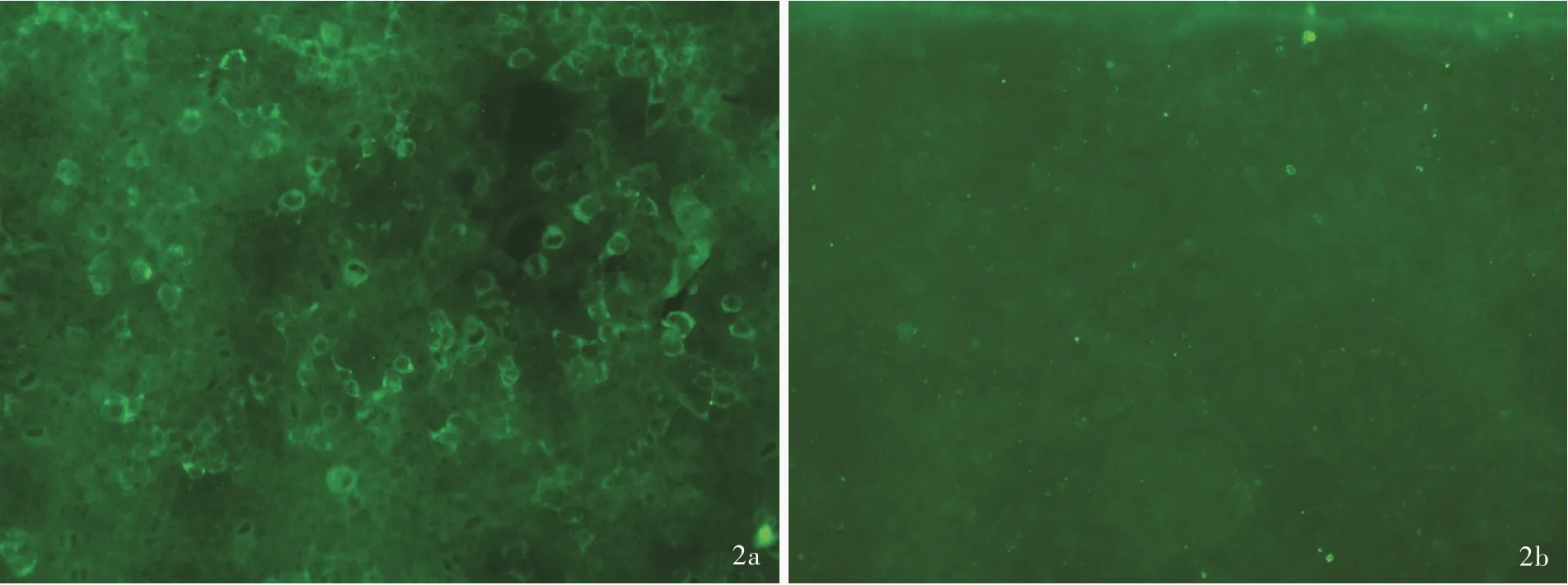
图2 例2 患者LGI1 抗体检测 CBA-IIF 法 ×200 2a 血清LGI1-IgG 呈阳性反应(1 ∶10) 2b 脑脊液LGI1-IgG 呈阴性反应Figure 2 Detection of LGI1 antibody in Case 2 CBA-IIF ×200 LGI1-IgG in serum was positive (titer 1:10, Panel 2a). LGI1-IgG in cerebrospinal fluid was negative (Panel 2b).
典型病例
患者 女性,45 岁。主诉记忆力减退15 天,于2017 年8 月31 日入院。患者于入院前15 天无明显诱因出现记忆力减退,以近记忆力下降明显,伴有阵发性胡言乱语,持续2 ~3 秒后自行终止,共计发作3 次,病程中无抽搐、意识丧失、大小便失禁等症状,同时伴有阵发性心悸、乏力。自发病以来精神、饮食稍差,睡眠尚可,大小便正常,体重无明显变化。既往患有高血压病3 年,血压控制尚可。个人史、家族史无特殊。入院后体格检查:体温36.8 ℃,脉搏100 次/min,呼吸20 次/min,血压120/80 mm Hg(1 mm Hg=0.133 kPa)。心、肺、腹部查体未见明显异常。神经系统检查神志清楚、语言流利,查体合作。记忆力下降,近期记忆力下降明显,定向力、计算力、理解力正常;脑神经未见明显异常,四肢肌张力正常,四肢肌力5 级,双侧共济运动稳准;四肢浅感觉、深感觉对称正常;双侧腱反射对称正常,病理征未引出;颈软、无抵抗,脑膜刺激征阴性。实验室检查:血常规、尿常规、便常规等指标均于正常值范围。血清钠131.83 mmol/L(137 ~147 mmol/L)、血清氯96.74 mmol/L(99 ~110 mmol/L),血清呼吸道九项检测提示肺炎支原体阳性。肝肾功能、电解质、免疫反应、肿瘤标志物、甲状腺功能及感染性疾病(乙型肝炎、梅毒、人类免疫缺陷病毒感染、结核病)均无异常。腰椎穿刺脑脊液压力125 mm H2O,外观略浑浊,白细胞计数2×106/L,葡萄糖4.37 mmol/L(同步指尖血糖6.20 mmol/L)、蛋白定量280 mg/L;脑脊液细菌、真菌、抗酸杆菌、病毒抗体阴性。血清LGI1抗体阳性(1 ∶100)、脑脊液LGI1 抗体阴性,其余自身免疫性脑炎相关神经细胞抗体检测均为阴性。头部MRI 检查显示,双侧海马体积缩小,呈T1WI 稍低信号、T2WI 和FLAIR 异常稍高信号(图5)。脑电图未见样放电。认知功能检查(患者初中文化程度):简易智能状态检查量表(MMSE)评分为25 分(27 ~30 分)、蒙特利尔认知评价量表(MoCA)评分17 分(≥25 分)。MQ=71,记忆商等级:差;IQ=86,智商等级:低于正常。入院诊断抗LGI1 抗体相关脑炎。予甲泼尼龙1000 mg/d 冲击治疗,逐渐减量,联合免疫球蛋白0.40 g(/kg·d),共治疗5 天,于2017 年9 月12 日出院,出院时记忆力有所改善、阵发性胡言乱语完全消失,精神、饮食、睡眠尚可,但仍存在阵发性心悸。出院后继续口服激素,逐渐减量至停药。出院1 个月后(2017 年10 月12 日)复查,仍有阵发性心悸,但记忆力明显改善;MMSE 评分28 分(入院时25 分)、MoCA 评分20 分(入院时17 分);MQ=83、记忆商等级:低于正常,IQ=86、智商等级:低于正常;血清钠为138.40 mmol/L、血清氯为101.60 mmol/L,血清及脑脊液LGI1 抗体呈阴性反应。2017 年10 月17 日复查头部MRI 提示:双侧海马异常信号较前明显减少(图5)。出院后3 个月随访,阵发性心悸消失;出院后18 个月随访,遗留近记忆力下降,但已恢复正常工作;出院后30 个月随访,完全恢复正常,头部MRI 显示炎症性病灶消失。
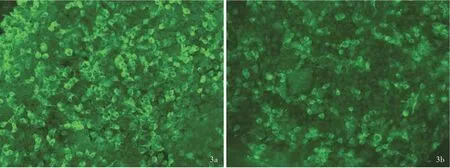
图3 例5 患者LGI1 抗体检测 CBA-IIF 法 ×200 3a 血清LGI1-IgG 呈阳性反应(1 ∶320) 3b 脑脊液LGI1-IgG 呈阳性反应(1 ∶10)Figure 3 Detection of LGI1 antibody in Case 5 CBA-IIF × 200 LGI1-IgG in the serum was positive (titer 1 : 320, Panel 3a).LGI1-IgG in cerebrospinal fluid was positive (titer 1:10, Panel 3b).
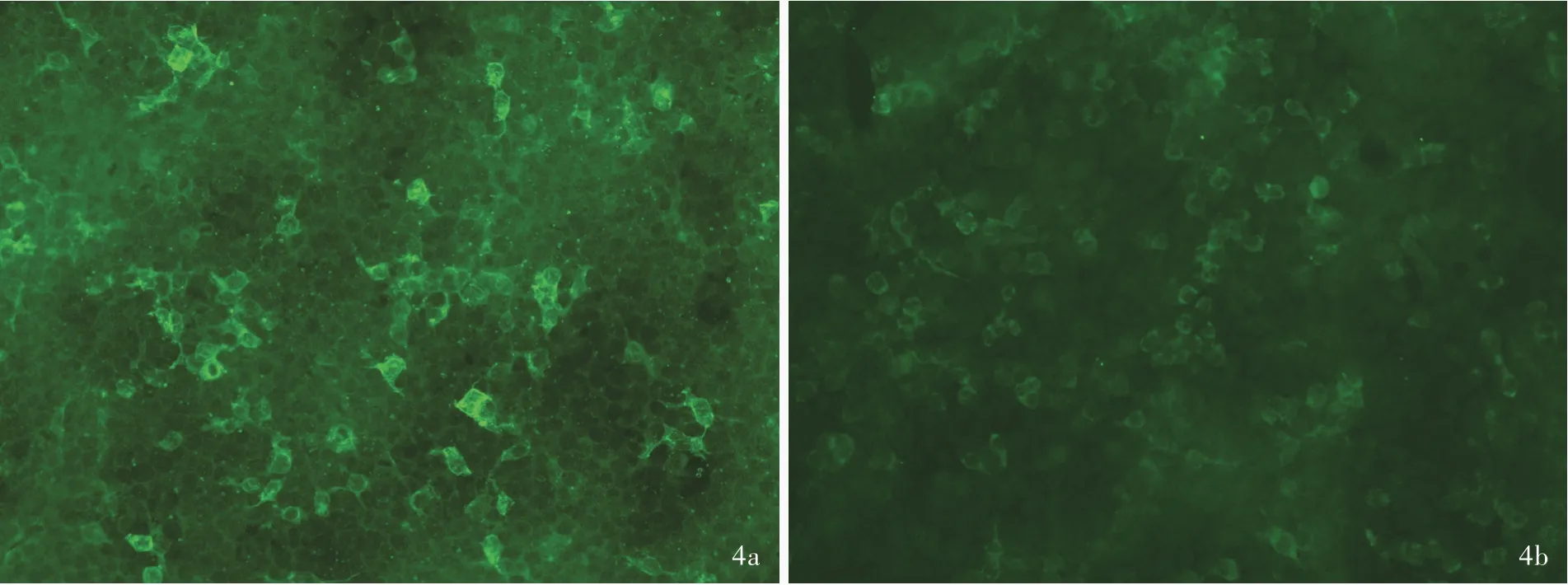
图4 例6 患者LGI1 抗体检测 CBA-IIF 法 ×200 4a 血清LGI1-IgG 呈阳性反应(1 ∶32) 4b 脑脊液LGI1-IgG 亦呈阳性反应(1 ∶1)Figure 4 Detection of LGI1 antibody in Case 6 CBA-IIF ×200 LGI1-IgG in serum was positive (titer 1:32, Panel 4a). LGI1-IgG in cerebrospinal fluid was positive (titer 1:1, Panel 4b).

图5 头部MRI 检查所见 5a 入院时横断面T1WI 显示双侧海马体积缩小,呈稍低信号 5b 入院时横断面T2WI 显示双侧海马体积缩小,呈稍高信号 5c 入院时横断面FLAIR 成像显示双侧海马体积缩小,呈异常稍高信号 5d 治疗1 个月后横断面T1WI 可见双侧海马呈稍低或等信号影,较入院时减轻 5e 治疗1 个月后横断面T2WI 可见双侧海马呈稍高信号影,信号强度较入院时减低 5f 治疗1 个月后横断面FLAIR 成像显示双侧海马异常信号范围较入院时缩小,信号强度减低Figure 5 Head axial MRI findings The volume of the bilateral hippocampus was reduced upon admission, with slightly lower signal on T1WI (Panel 5a), and slightly higher signal on T2WI (Panel 5b) and FLAIR (Panel 5c). After 1 month of treatment, the bilateral hippocampal abnormal signal were significantly reduced. It was slightly lower or equal signal on T1WI(Panel 5d), slightly higher signal on T2WI (Panel 5e) and FLAIR (Panel 5f).
讨 论
根据文献报道,抗LGI1 抗体相关脑炎男女发病比例约为2 ∶1,平均发病年龄为64 岁[2],本组男女发病比例为1 ∶1,平均发病年龄约50.33 岁。抗LGI1 抗体相关脑炎呈急性或亚急性病程,以认知功能障碍、癫发作和精神行为异常为主要临床特征,本组患者急性发病1 例、亚急性发病5 例。抗LGI1抗体相关脑炎的癫发作类型可分为3 种亚型,分别为面-臂肌张力障碍发作、局灶性发作和全面性强直-阵挛发作。面-臂肌张力障碍发作是抗LGI1 抗体相关脑炎的特征性表现,半数以上患者病程中可出现面-臂肌张力障碍发作,主要表现为单侧手臂(或下肢)及面部不自主运动,仅持续数秒,发作频繁者每日可发作多达100 次。本组例4 发病后曾出现四肢麻木无力及口角抽搐,考虑为伴感觉症状的面-臂肌张力障碍发作;例6 表现为左侧面部、双上肢抽搐,每次持续数秒,每日平均发作约30 次,亦为面-臂肌张力障碍发作。局灶性发作具有刻板性和重复性,每日约发作10 次,可分为感觉和运动性发作两种类型,患者就诊时常将感觉性发作描述为“说不清的感觉、思想逃逸、身体颤抖、胃气上升、竖毛发、恐惧或脸红”,而运动性发作则表现为凝视、自动症或发声[7-9],本文例6 患者即为自动症,表现为双手来回搓衣服,每天发作10 余次。本组6 例患者均未详细提及感觉事件,考虑可能存在感觉发作被忽视的情况。面-臂肌张力障碍发作和局灶性发作大多发生在记忆障碍出现之前,至疾病后期,则多以全面性强直-阵挛发作为主[10],本文有3 例患者呈全面性强直-阵挛发作,其中2 例发作前无面-臂肌张力障碍发作和局灶性发作,但均伴有认知功能障碍,提示部分抗LGI1 抗体相关脑炎患者疾病前期可无面-臂肌张力障碍发作或局灶性发作,直接进入中后期即认知功能障碍和全面性强直-阵挛发作。
研究显示,约95%的抗LGI1 抗体相关脑炎患者存在认知功能障碍,表现为近记忆力下降[11]。本组6 例患者均存在认知功能障碍,例2 和例3 以近记忆力下降为主诉,而无任何类型的癫发作,使诊断难度增加,提示抗LGI1 抗体相关脑炎患者以认知功能障碍最为常见甚至是其唯一的临床表现。
抗LGI1 抗体相关脑炎患者常伴有精神行为异常,以幻视幻听、焦虑抑郁、烦躁不安、活动过度、思维活跃、偏执、健谈、淡漠或强迫症等常见[12]。本组例1 患者即表现为幻觉,例3 和例4 患者则以胡言乱语为主症,与既往研究相似[12]。约有半数抗LGI1抗体相关脑炎患者可伴有严重失眠和快速眼动睡眠期行为障碍(RBD)等自身免疫性睡眠障碍[12],本组患者睡眠障碍(5 例)和自主神经功能障碍如尿频、大小便失禁、腹泻等(3 例)症状亦十分常见。
本组6 例患者血清和脑脊液LGI1 抗体检测均呈阳性,且血清抗体滴度高于脑脊液,而脑脊液常规、生化、免疫等项指标则于正常参考值范围,与文献报道基本相符[13-14]。其中,4 例血清学检测呈现低钠血症,表明低钠血症也是抗LGI1 抗体相关脑炎的特征性表现,因此临床上对于LGI1 抗体检测阴性,但低钠血症难以纠正的患者应考虑LGI1 抗体阴性自身免疫性脑炎可能,尽早施行免疫治疗,以纠正低钠血症。
有研究显示,约75%的自身免疫性脑炎患者头部MRI 检查颞叶内侧或海马呈T2WI 高信号[10],本组有3 例患者头部MRI 异常,然而头部MRI 正常者亦不能排除抗LGI1 抗体相关脑炎的可能。Tripathi等[15]对自身免疫性脑炎患者进行18F-FDG PET 研究,发现此类患者顶叶和枕叶皮质呈低代谢而基底节区呈高代谢。本组例6 患者基底节区代谢相对增高,大脑皮质和小脑半球代谢轻度降低,与Tripathi等[15]的报道相一致。抗LGI1 抗体相关脑炎较少合并肿瘤,据文献报道合并不同肿瘤患者仅占5% ~10%,以胸腺瘤多见[2],本组无合并肿瘤病例,且部分患者随访2 年以上亦未发现肿瘤。
抗LGI1 抗体相关脑炎是一种可治性自身免疫性疾病,未合并肿瘤的患者对免疫治疗反应良好。免疫治疗分为一线治疗、二线治疗和长程免疫治疗。一线免疫治疗药物主要包括糖皮质激素冲击疗法、静脉注射免疫球蛋白和血浆置换疗法;二线药物以利妥昔单抗和环磷酰胺为主,适用于一线药物疗效欠佳者;长程免疫治疗药物包括吗替麦考酚酯和硫唑嘌呤等,主要用于复发性病例,也可用于一线免疫治疗效果欠佳患者[11]。关鸿志等[16]认为,吗替麦考酚酯联合一线免疫治疗药物具有较好的抗LGI1 抗体相关脑炎治疗效果。本组6 例中5 例患者采用激素联合静脉注射免疫球蛋白治疗,余1 例因拒绝接受激素治疗仅予静脉注射免疫球蛋白治疗。随访6 ~24 个月,3 例遗留记忆力下降,考虑与海马萎缩或硬化有关;6 例患者经治疗后均恢复正常工作与生活,无复发、无死亡病例,提示该病预后良好,早期施以免疫治疗可明显改善预后,降低复发率和病死率。
本研究为病例回顾性研究,证据级别较低、样本量偏小,有待大样本临床试验深入研究。总之,抗LGI1 抗体相关脑炎患者具有特征性的临床表现,应尽早识别其症状与体征,早期开始免疫治疗,以改善患者生活质量。

