CYP2D6基因多态性与利培酮治疗精神分裂症的相关性研究*
于晓东 杨 楹 刘增训 李宪伟 滕伟钰 王 旸, 2 王汝展
精神分裂症是精神科临床上常见的重性精神障碍之一,常常伴随特殊的情感、思维和感知觉方面的不协调障碍,给患者带来巨大痛苦的同时,也给家庭造成较大的经济负担[1,2]。目前精神分裂症的治疗主要是以药物治疗为主,常选用利培酮、奥氮平、阿立哌唑、帕利哌酮等非典型抗精神病药物,但是由于不同精神分裂症患者之间存在个体差异,同一药物治疗的疗效和安全性之间也有所不同,这与遗传因素(尤其是基因多态性)、社会因素、个体因素、医疗因素等有着密切的关系[3~5]。有研究表明[6~8],细胞色素P4502D6(CYP2D6)基因作为细胞色素P450蛋白酶超家族中的一员,具有高度的基因多态性,且能参与利培酮等抗精神病药物的代谢反应。而在中国人群中,CYP2D6*10为最常见的等位基因突变类型,在精神分裂症患者中占30%~50%[9]。为了配合精神分裂症的精准医疗,为精神科临床用药提供必要的实践依据,本研究旨在探讨CYP2D6*10基因型的精神分裂症患者应用利培酮系统治疗的疗效及安全性。现汇报如下。
1 对象与方法
1.1 对象 入组患者为2017年1月~2018年10月在山东省精神卫生中心住院治疗的精神分裂症患者。入组标准:符合美国精神障碍诊断与统计手册第5版(DSM-V)中精神分裂症的诊断标准;汉族;年龄18~59岁;性别不限;病程≥3个月;首次就诊,未曾应用抗精神病药物系统治疗;就诊前2周内未服用任何精神科药物。排除标准:患有严重的躯体疾病者;妊娠或哺乳期妇女;既往有与研究有关的药物过敏史者;具有酒精等物质依赖者;器质性精神障碍;精神发育迟滞者;有严重的冲动攻击行为或者自伤自杀企图者;入组前3个月内行无抽搐电休克治疗(MECT)者;与其他精神障碍存在共病者。脱落标准:出现严重不良反应,或因疗效不佳而换药治疗者;依从性差;使用了影响试验结果的药物;其他原因导致中途退出者。患者及其家属签署知情同意。研究已经过相应伦理委员会审核。
本研究共计收集302例患者,完成全部研究的296例,完成率98.01%,脱落6例(中途退出者2例,出现严重不良反应者2例,疗效不佳而换药者2例)。在治疗前,根据CYP2D6基因多态性检测的结果,将患者进行分组:(1)研究组:CYP2D6基因多态性检测结果[6~8]为08CYP2D6基因检测为TT、10CYP2D6基因检测为GG、06CYP2D6基因检测为CC、基因型分析结果为*10/*10、代谢型为IM的患者,共入组100例,最终完成98例,脱落2例(中途退出2例),完成率为98.00%。其中男46例,女52例;年龄18~36岁,平均(28.79±9.11)岁;身高(173.74±6.26)cm;体质量(77.13±12.83)kg;病程6~23个月,平均(13.71±7.59)个月;(2)对照组:除研究组之外的患者,即CYP2D6基因多态性检测结果为非08CYP2D6基因检测为TT、10CYP2D6基因检测为GG、06CYP2D6基因检测为CC、基因型分析结果为*10/*10、代谢型为IM的患者,共入组202例,最终完成198例,脱落4例(严重不良反应者2例,疗效不佳而换药者2例),完成率98.02%。其中男92例,女106例;年龄20~38岁,平均(27.96±8.46)岁;身高(172.85±5.03)cm;体质量(77.24±15.70)kg;病程7~25个月,平均(12.39±10.16)个月。两组在完成率、性别比、年龄、身高、体质量、病程等一般资料方面比较,差异均无统计学意义(P>0.05),组间具有可比性。
1.2 方法
1.2.1 CYP2D6基因多态性检测流程 所有入组患者的CYP2D6基因多态性检测均在药物治疗前进行,并根据检测的结果进行分组。CYP2D6基因检测的内容范围见表1。采用数字荧光分子杂交技术进行检测,入组患者空腹采取外周静脉血,应用含有EDTA抗凝剂的采血管抽血,并在-20 ℃冰箱中保存。检测采用美国应用生物系统(ABI)公司生产的ABI7300实时荧光PCR扩增仪,应用北京华夏时代基因科技发展有限公司提供的测序反应通用试剂盒(英文名称Universal Sequencing Kit)。具体检验方法:(1)取出试剂包装管,轻弹管壁使试剂充分混匀,短暂离心后,置于冰板上备用;(2)取1.5 μl处理过的粒细胞混悬液,加到1支试剂中,盖严管盖,充分混匀并短暂离心;(3)将加入粒细胞样本的试剂盒放入检测设备中,避免液体震动到管壁上;(4)在设备控制电脑上,点开软件,选取基因类型(08CYP2D6基因检测为TT,10CYP2D6基因检测为GG,06CYP2D6基因检测为CC,基因型分析结果为*10/*10,代谢型为IM),并运行系统。应用实时荧光PCR检测CYP2D6基因多态性。PCR反应:在37 ℃下10 min,在95 ℃下5 min,在特定条件下扩增40倍循环(即95 ℃下15 s,在60 ℃下60 s),在每个循环结束时,采集荧光信号。其中基因类型(08CYP2D6基因检测为TT,10CYP2D6基因检测为GG,06CYP2D6基因检测为CC,基因型分析结果为*10/*10,代谢型为IM)为FAM检测通道,设为红色,样本计入研究组;非基因类型(非08CYP2D6基因检测为TT,10CYP2D6基因检测为GG,06CYP2D6基因检测为CC,基因型分析结果为*10/*10,代谢型为IM)为VIC检测通道,设为黑色,样本计入对照组。

表1 CYP2D6基因检测的内容
1.2.2 药物治疗方法 所有患者均应用利培酮口崩片(以下简称利培酮)单一系统治疗,起始剂量为1 mg/d,之后根据患者的症状变化情况酌情加量,最终剂量范围2~8 mg/d,每天晨、晚两次服药,疗程共计6周。在研究期间,禁止合并其他抗精神病药物、抗抑郁药、心境稳定剂、研究规定外的抗焦虑药。若患者在服药过程中,出现急性肌张力障碍可酌情加用盐酸苯海索4 mg/d,出现静坐不能可临时加用普萘洛尔10 mg,出现睡眠障碍可临时加用阿普唑仑0.4 mg,以作对症处理。
1.2.3 疗效评价 由富有科研经验、并经过本研究培训的精神科临床医生(主治及以上)执行所有的药物调整和量表评价工作。应用阳性和阴性综合征量表(Positive and Negative Syndrome Scale,PANSS)、临床总体印象量表-病情严重程度(Clinical Global Impression-Severity of Illness,CGI-SI)、治疗中需处理的不良反应症状量表(Treatment Emergent Symptom Scale,TESS)于研究基线和治疗后第2、4、6周末分别对两组患者评定疗效和不良反应。在基线和治疗后第2、4、6周末对全部入组患者检测血压、血常规、肝功能、尿常规及心电图、脑电图等基本实验室检查。一致性试验Kappa=0.91。
1.2.4 统计学方法 将所有数据输入SSPS 22.0进行统计学分析,计量数据采用独立样本t检验,计数资料采用卡方检验。检验标准α=0.05。
2 结果
2.1 两组治疗6周末利培酮剂量比较 在治疗后第6周末,将两组所用的利培酮剂量进行比较,结果显示,研究组的利培酮用量为(4.77±1.51)mg/d,对照组的利培酮用量为(5.70±1.20)mg/d,研究组用量低于对照组(t=3.26,P=0.002)。
2.2 两组基线及治疗后各阶段CGI、PANSS评分比较 治疗后第4、6周末,两组CGI评分、PANSS总分及各因子分均较各自基线时降低(P<0.05)。见表2。
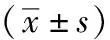
表2 两组基线及治疗后各阶段CGI、PANSS评分比较
2.3 两组基线及治疗后各阶段安全性比较 在治疗后第2、4、6周末,研究组TESS评分及不良反应的例次数均低于对照组(P<0.05)。见表3。在治疗后第6周末,研究组中共8例患者存在不良反应(其中激越4例,失眠2例,体质量增加2例),总不良反应发生率为8.16%;对照组共37例患者存在不良反应(其中激越14例,体质量增加11例,失眠5例,口干4例,心动过速3例),总不良反应发生率为18.69%。研究组的总不良反应发生率低于对照组(χ2=5.63,P=0.018)。研究过程中,所有患者的基本实验室检查结果均无明显、严重异常。
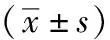
表3 两组基线及治疗后各阶段安全性比较
3 讨论
精准医疗是一种基于个体的基因、生活方式、自然和社会环境等个体化差异因素之上,用于各种疾病的诊断、预防、治疗等领域的新兴的医疗方式,即通过相关的基因检测,指导医生应用对患者有效的药物,而避免应用对患者无效的药物的一种医疗方式[10,11]。2015年美国率先提出了“精准医疗计划(PMI)”,美国国立卫生院(NIH)对精准医疗详细制定了短期目标、长期计划,我国在2016年将精准医疗列入国家重点研发计划中(位于首位),并投入了大量的财力和人力资源[12,13]。随着相关技术的进步,基因检测越来越多地应用于各种躯体疾病的治疗中,例如各类癌症、心脑血管性疾病等,通过基因检测能够指导医生合理设置患者的个体化治疗方案,使患者在治疗中最大化地受益,并取得了较好的临床疗效[14~16]。对于精神障碍而言,药物治疗存在比较明显的个体化差异,影响个体治疗的个体化差异的重要因素众多,例如基因多态性、代谢酶个体化、转运体突变等,这些因素都或多或少影响着精准医疗在精神障碍中的应用状况,同时也增加了实践应用的难度[17],再加上目前精神障碍的诊断、分类、治疗等仍处于相对较为模糊的状态,所以将精准医疗充分用于精神医学领域,并不是一件十分容易的事情[18]。作为最常见的也是最重要的精神障碍之一,精神分裂症的精准治疗开展相对较早,国外资料显示,CYP2D6基因多态性与精神分裂症药物治疗之间存在一定的相关性[19,20]。在目前的国内研究中,基因检测的精准医疗主要集中于血药浓度、症状关联、药物代谢、RNA调控等方面[21~24],而将基因检测的精准医疗手段应用于精神分裂症等精神障碍的治疗过程中的临床治疗指导研究相对较少。本研究正是基于目前的研究现状,将基因检测的精准医疗手段应用于精神分裂症的利培酮药物治疗过程中,进行具体药物应用指导。
在本研究结果中,有以下的内容呈现:(1)临床疗效:治疗后第4、6周末,两组CGI评分、PANSS总分及各因子分均较各自基线时降低,说明在治疗后第4周末开始,两组患者应用利培酮治疗都有一定的疗效,而在基线及治疗的各阶段,两组CGI评分、PANSS总分及各因子分比较差异没有统计学意义,说明两组在应用利培酮治疗的疗效方面基本相当;(2)服用剂量:在治疗后第6周末,研究组的利培酮平均用量低于对照组,这说明CYP2D6基因多态性检测结果为08CYP2D6基因检测为TT,10CYP2D6基因检测为GG,06CYP2D6基因检测为CC,基因型分析结果为*10/*10,代谢型为IM的患者,对利培酮具有更高的治疗敏感性,应用相对较少剂量的利培酮即可达到正常水平的治疗效果,这不仅可以明显降低患者的治疗经济负担,还可以通过服用较少的药物剂量在一定程度上提高患者的长期治疗依从性;(3)治疗安全性:在治疗后第2、4、6周末,研究组TESS评分及不良反应的例次数均低于对照组,研究组的总不良反应发生率低于对照组,说明研究组患者对利培酮的耐受性更好,安全性更高,既可以大大提高治疗过程中的安全性,而且还会明显减少药物治疗对患者生活质量的影响、更多的对抗不良反应的药物服用所带来的相关问题,患者在治疗的过程中能够得到更多的间接受益。
由此,也可以得到一些对于精神分裂症临床治疗过程中的推测和建议:(1)在应用药物治疗前,尤其是面对首发精神分裂症患者,根据基因检测的结果,有选择地对于CYP2D6基因多态性检测结果为08CYP2D6基因检测为TT,10CYP2D6基因检测为GG,06CYP2D6基因检测为CC,基因型分析结果为*10/*10,代谢型为IM的患者,首选应用利培酮系统治疗,对于其他基因型的患者首选其他抗精神病药物,可能是一个比较理想的药物治疗方案选择;(2)在治疗前对精神分裂症的患者进行基因检测,对于那些CYP2D6基因多态性检测结果为08CYP2D6基因检测为TT,10CYP2D6基因检测为GG,06CYP2D6基因检测为CC,基因型分析结果为*10/*10,代谢型为IM的患者,在应用利培酮系统治疗过程中,药物加量过程可以适当放缓,药物最终治疗量适当降低,极有可能也可以取得快速加量、较高剂量的利培酮同样的治疗效果;(3)在治疗过程中,面对患者的不良反应时,可以适当采用减少对抗不良反应的药物种类和剂量的方式,尽量避免预防性用药,更加保证治疗过程中的安全性。
当然,本研究还存在一些不足和局限:(1)纳入样本相对较少:这需要在下一步的深入研究中纳入更多的样本,以进一步证实目前研究结果;(2)性别差异:本研究中同时纳入男性和女性患者,以验证精神分裂症患者的整体状况,希望在下一步的研究中可以针对男性或女性患者进行单独的研究,以辨别是否有性别差异的存在;(3)观察时限相对较短:本研究仅观察了6周时间,这对于精神分裂症的全病程而言,相对较短,希望在下一步的研究中,可以适当延长观察时限,以验证本研究结果在长期治疗尤其是维持期治疗中是否存在。
综上所述,在药物治疗前,对精神分裂症患者进行CYP2D6基因多态性检测,当检测结果为08CYP2D6基因检测为TT,10CYP2D6基因检测为GG,06CYP2D6基因检测为CC,基因型分析结果为*10/*10,代谢型为IM时,首先选用利培酮系统治疗,可取得较好的临床疗效,更低的药物治疗剂量,更高的治疗安全性,较少的经济负担,值得临床推广。

