微生态制剂预防儿童抗生素相关性腹泻的临床综合评价
尉耘翠,都赛飞,贾露露,魏 婷,金 彦,王晓玲*
0 引言
抗生素相关性腹泻(Antibiotic-associated diarrhea,AAD)是指伴随抗生素使用而发生的无法用其他原因解释的非感染性腹泻,其实质是抗生素引起微生态失衡所导致的腹泻[1]。近年来,随着抗生素在临床上的广泛应用,AAD的发生率呈逐年增加趋势[2]。由于儿童比成人更容易罹患感染性疾病,其抗菌药物的使用率是成人的3倍[3]。在使用抗生素的患者中,成人AAD的发病率为5%~39%,儿童AAD的发病率达15%~39%,婴幼儿由于其自身解剖及生理特点导致其AAD发生率更高,可达30%~45%[4]。AAD的发生不仅造成了患者的经济损失,迁延者还可引起营养不良、免疫力低下,严重者可能并发感染性休克、中毒性巨结肠、肠穿孔等[4]。因此,预防儿童AAD的发生至关重要。抗生素的合理使用在一定程度上能够有效预防AAD,但依旧难以避免其发生。近年来,应用微生态制剂治疗AAD已在国内外达成共识[5],然而目前在临床上使用抗生素治疗原发病的同时早期应用微生态制剂预防AAD的发生,尚未得到广泛认可和重视。本研究通过系统梳理国内外相关指南及文献,从有效性、安全性、经济性多维度开展综合评价,为微生态制剂预防儿童AAD提供依据和参考。
1 资料与方法
1.1 评价维度与证据来源 本研究的评价维度包括安全性、有效性、经济性。证据来源于临床指南/共识、系统评价/Meta分析文献以及成本分析。
1.2 文献分析法
1.2.1 检索数据库 本研究检索数据库包括英文数据库和中文数据库。英文数据库包括PubMed、EMBASE、Cochrane library。中文数据库包括中国期刊全文数据库(CNKI)、万方数字化期刊全文库、中文科技期刊全文数据库(VIP)、中国生物医学数据库(CBM)。检索时间为建库至2019年9月15日。
1.2.2 检索策略 文献检索策略如表1所示。

表1 文献检索策略
1.2.3 纳入排除标准 纳入标准:本研究纳入标准参考PICOS原则。①研究对象(P):年龄小于等于18岁接受抗菌药物治疗的儿童患者。②干预措施(I):微生态制剂(种类、剂量、剂型不限)与抗生素联用。③对照措施(C):安慰剂或空白对照(剂量与剂型不限)与抗生素联用。④结局指标(O):有效性结局指标包括AAD发生率、平均腹泻持续时间、日均腹泻次数、平均住院时间等;安全性指标包括不良反应发生情况等;经济性指标包括成本分析、成本效果分析、成本效用分析等。⑤研究设计(S):系统评价、Meta分析、药物经济学评价、卫生技术评估。
排除标准:①微生态制剂用于治疗AAD;②重复的文献;③仅为研究方案的文献。
1.2.4 数据提取及质量评价 2名评价员对纳入研究独立进行质量评价和资料提取,然后交叉核对,如有分歧则交由第三者并共同讨论解决。
采用AMSTAR 声明评价纳入Meta分析文献的报告质量。AMSTAR是国外研发的用于评价系统评价/Meta分析方法学质量的测量工具,包括11条项目清单,具有良好的效度、信度和反应度,可以客观真实地报道文章的方法学质量,证实提供证据的可信度。
1.2.5 统计分析 用事先设计的资料提取表提取资料,提取内容包括研究基本信息、研究方法、研究对象基本特征、干预/对照措施、主次要结局指标等。采用描述性分析方法进行文献汇总分析。
1.3 成本分析法 本研究对国内上市的主要微生态制剂进行成本分析。药品价格采用药智网最低中标价格,用药剂量采用药品说明书中3~7岁儿科人群(儿童AAD高发年龄)最低推荐剂量和频次,若药品说明书无儿童推荐剂量,则采用本课题组前期调研结果中的临床实际使用剂量[全国儿科微生态制剂使用情况调查分析(调查对象来自全国6个行政区36家医院213名儿科临床医师/药师)]。根据临床经验,以7 d为疗程计算疗程成本。
2 结果
2.1 有效性评估结果
2.1.1 有效性临床指南/共识情况 共梳理12项国内外微生态制剂应用相关临床指南/共识,其中8项指南/共识(国外4项、国内4项)推荐微生态制剂用于预防儿童AAD。国外指南倾向推荐鼠李糖乳杆菌、布拉氏酵母菌;因鼠李糖乳杆菌目前在中国没有上市,国内指南主要推荐双歧杆菌、乳杆菌、布拉氏酵母菌等。
现在的旅游市场也在变化,旅游者不再只是简单的游玩,而是要求更有新意、更有含金量的旅游,这就要求职业导游学生的能力培养要向着实效性、适应性和科学性的方向发展。而且有一些特种旅游,对导游的要求更高,更专业。对于一名职业导游来说,潜水、登山、摄影等技能也会成为必备的技能,重要性非常明显。所以,可以在职业导游培养的过程中,分出一些特长班或者兴趣班,学生可以根据自己的爱好和职业方向,来选择自己的专项技能培养。
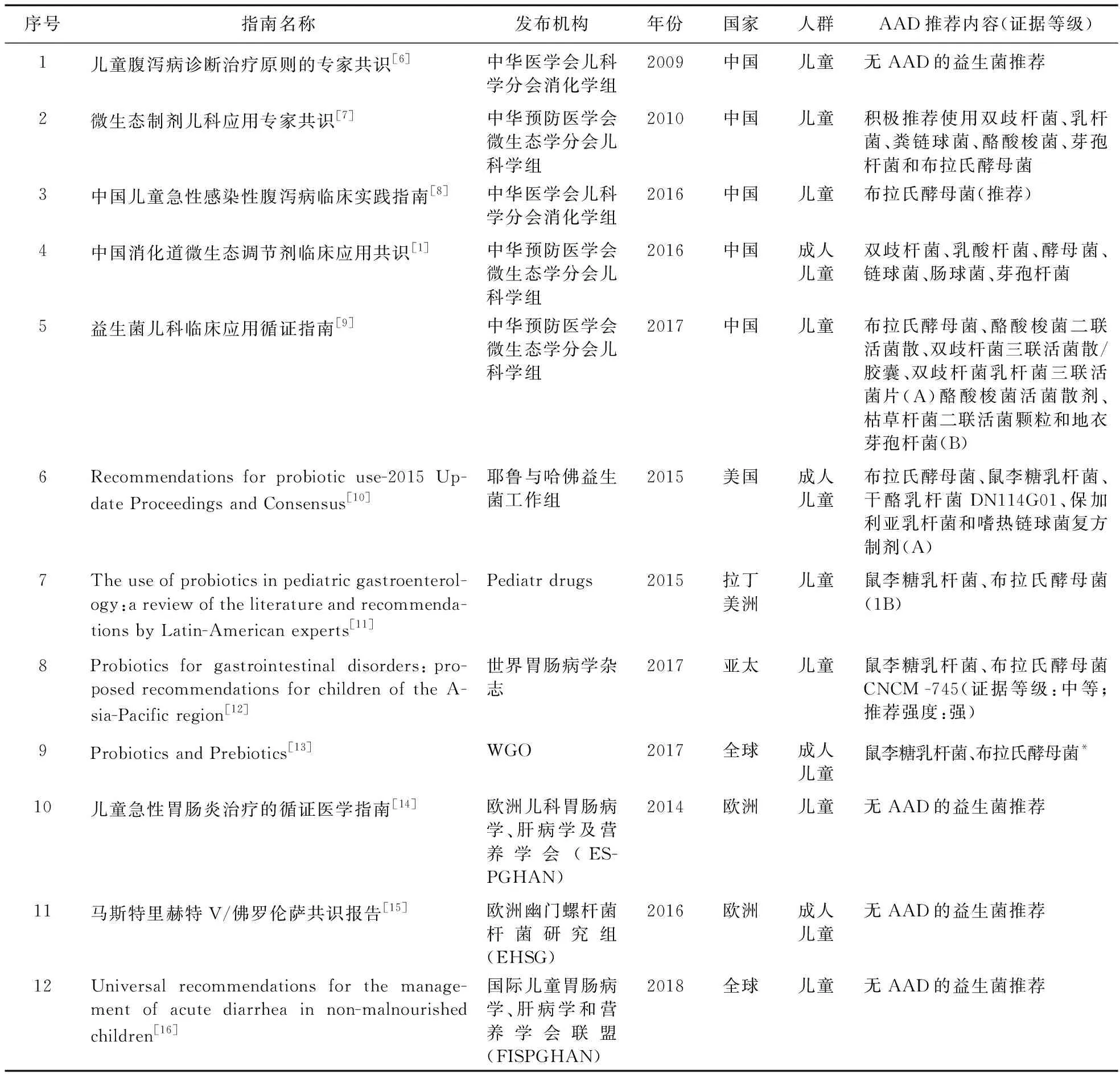
表2 指南/共识中微生态制剂预防儿童AAD的汇总分析
2.1.2 有效性Meta分析文献梳理情况 文献筛选结果显示,共检索出Meta分析文献113篇,去重后剩余文献98篇;初筛阅读题目和摘要,剩余文献38篇;全文阅读,排除23篇,包括非儿童患者、会议摘要、无数据、疾病类型不符、综述,最终纳入有效性文献15篇、安全性文献14篇。文献检索流程图如图1所示。
本研究共纳入15篇Meta分析文献(英文7篇,中文8篇):其中12篇为儿科人群研究,3篇为全人群研究(包括成人和儿童),对儿科人群进行亚组分析。纳入Meta分析文献基本特征如表3所示。
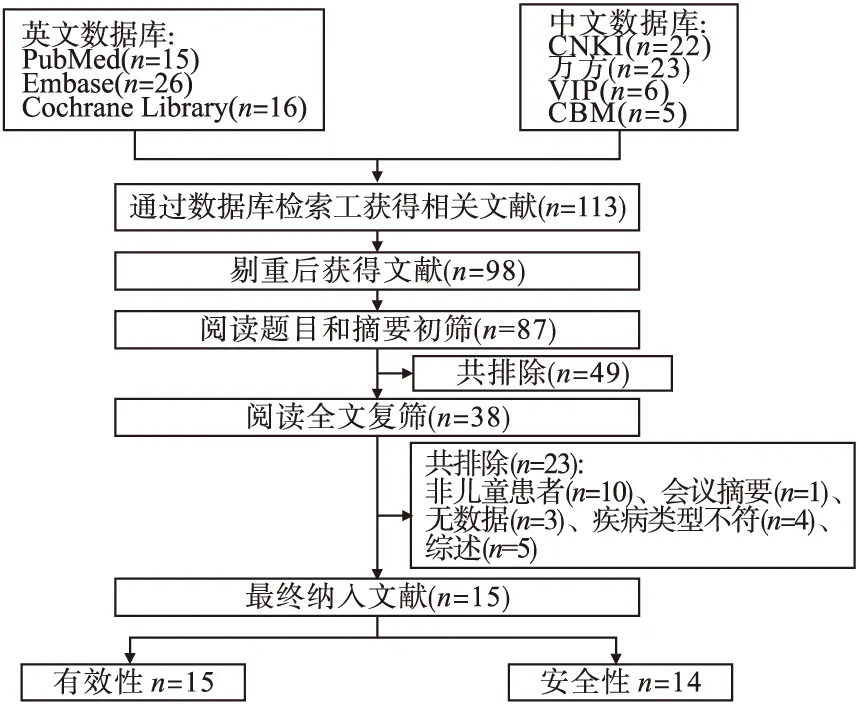
图1 文献检索流程图
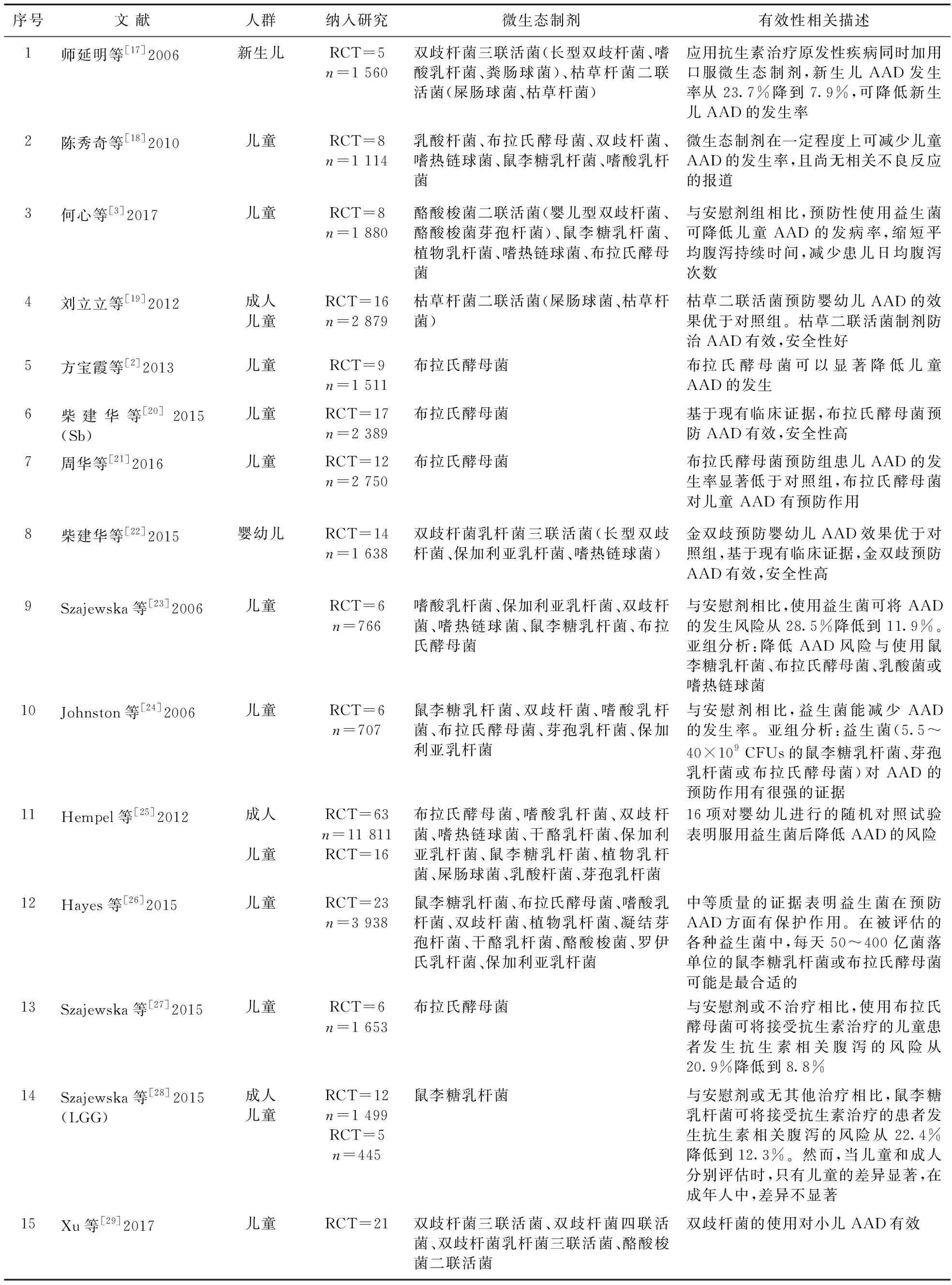
表3 有效性Meta分析文献基本特征
按照AMSTAR 声明11条项目清单评价纳入的15篇Meta分析文献的报告质量,结果显示:8篇文献质量较高(国内2篇、国外6篇),7篇文献为中等质量(国内6篇、国外1篇)。见表4。
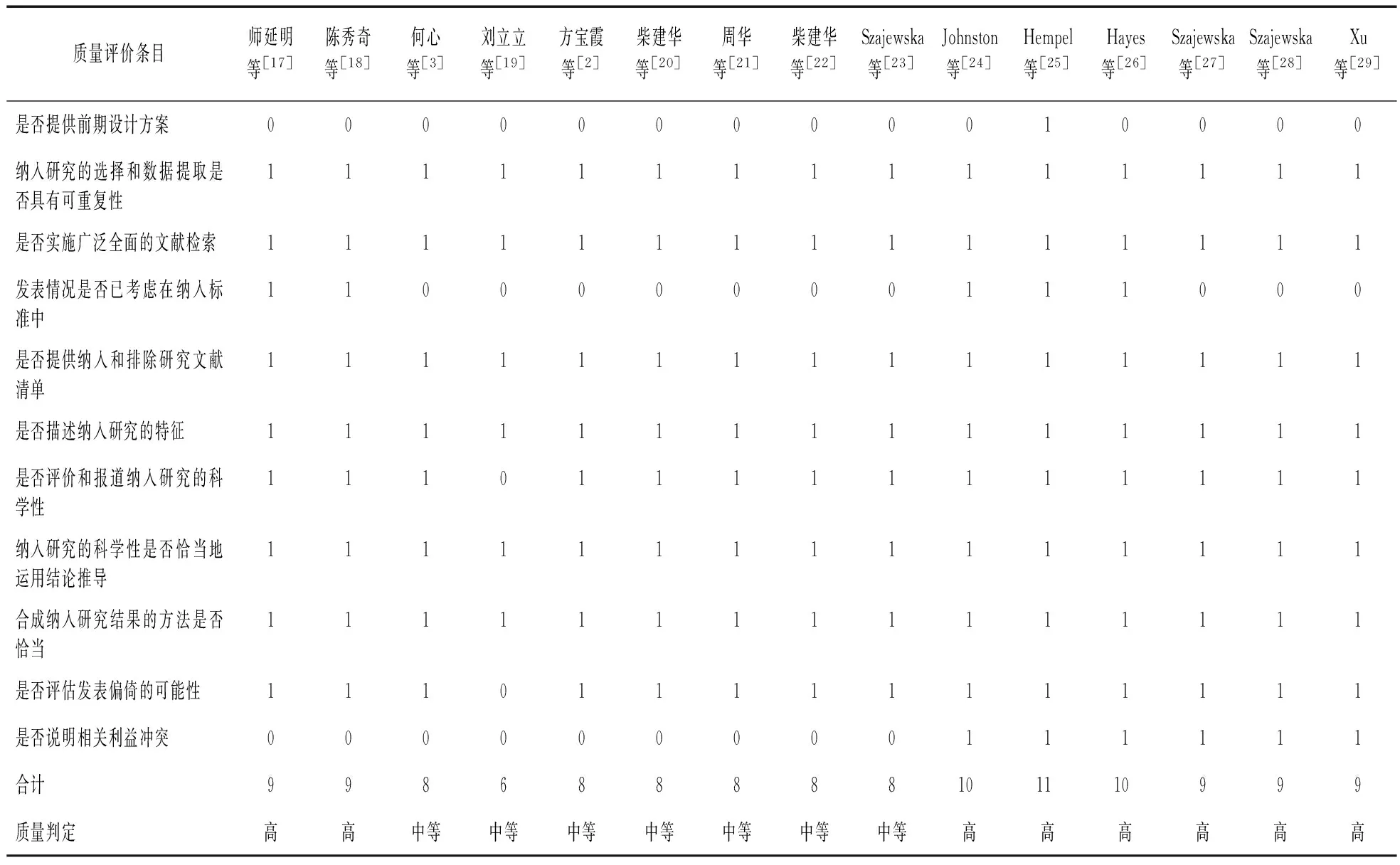
表4 AMSTAR 声明评价纳入Meta分析文献报告质量
15篇国内外Meta分析文献结果显示,应用抗生素治疗原发性疾病同时加用微生态制剂,可有效预防儿童AAD,缩短平均腹泻持续时间,减少患儿日均腹泻次数。单一菌种分析显示,鼠李糖乳杆菌、布拉氏酵母菌、双歧杆菌、枯草杆菌可能是较好的选择。见表5。

表5 有效性Meta分析文献汇总分析
2.2 安全性评估结果
2.2.2 安全性Meta分析文献梳理情况 本研究共纳入安全性Meta分析文献14篇,文献质量评价结果参见有效性评估部分。14篇国内外Meta分析均显示,整体微生态制剂预防儿童AAD具有较好的安全性。其中11篇未观测到药物不良反应,3篇报道了相关不良反应,主要包括皮疹、恶心、胀气、腹胀、腹痛、呕吐、痰增多、胸痛、便秘、味觉障碍、食欲不振、腰背痛、头晕等,均在治疗过程中自行缓解。安全性Meta分析文献汇总分析见表7。
2.3 经济性评估结果
2.3.1 成本分析 对国内上市的主要微生态制剂进行成本分析结果显示,国内儿童微生态制剂平均单日服用价格为4.53元,平均7 d疗程价格为31.70元,成本负担较轻。成本较低的微生态制剂包括枯草杆菌二联活菌颗粒、双歧杆菌活菌胶囊、酪酸梭菌二联活菌胶囊、双歧杆菌三联活菌胶囊等。见表8。

表6 安全性指南/共识汇总分析

表7 安全性Meta分析文献汇总分析
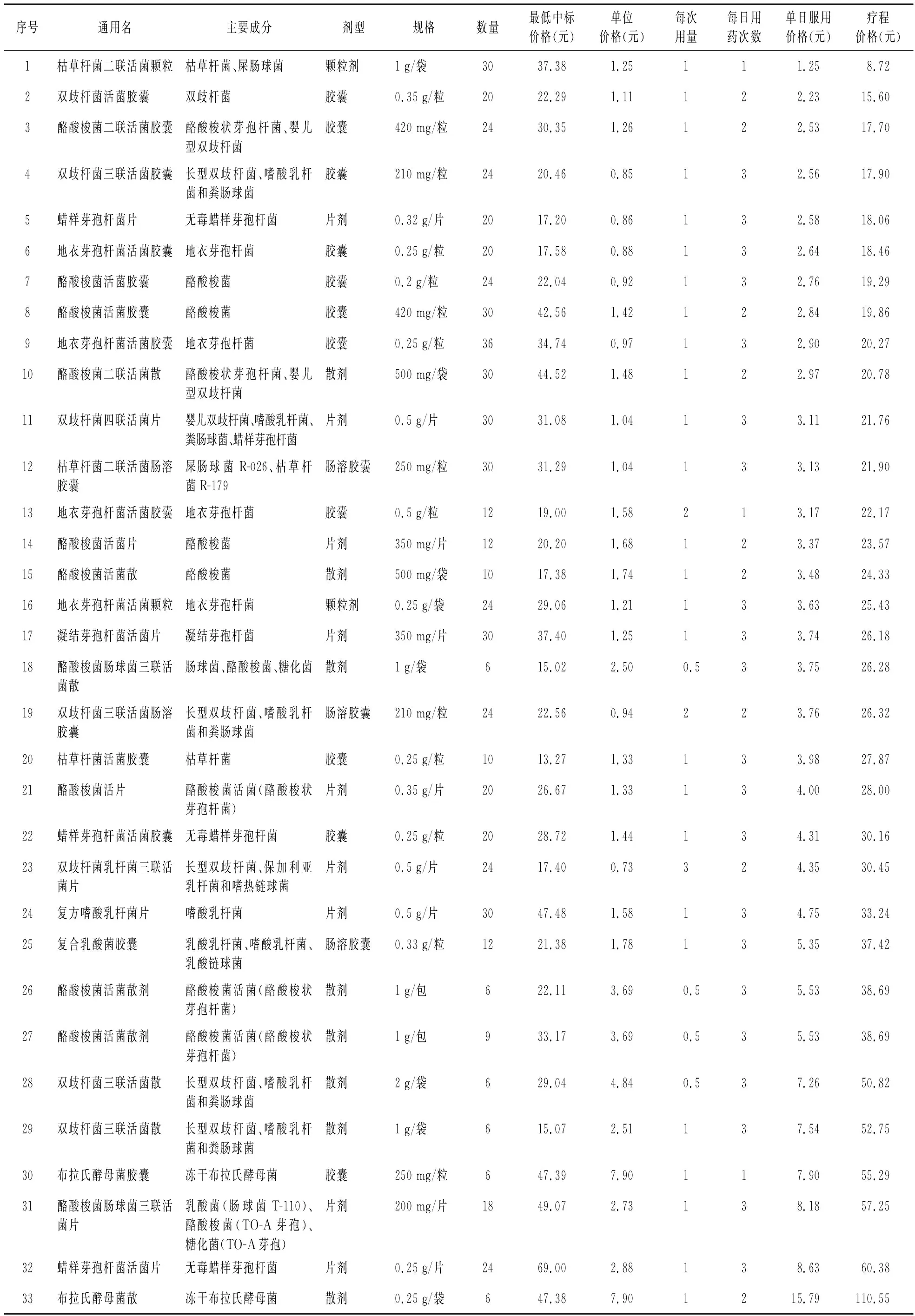
表8 国内上市的微生态制剂成本分析
2.3.2 药物经济学评价文献分析 本研究未检索到微生态制剂预防儿童AAD的药物经济学评价文献,因此对其在成人AAD中的药物经济学评价文献进行梳理。结果显示,2篇国外药物经济学评价研究均显示微生态制剂预防AAD可节约成本、具有经济学效应,但研究人群均为成人人群。国内尚未检索到微生态制剂预防成人或儿童AAD的药物经济学评价研究。见表9。

表9 微生态制剂预防AAD的药物经济学评价文献分析
3 讨论
近年来,随着抗生素的广泛应用,AAD的发病率逐年增高[32]。小儿由于自身肠道发育不成熟,其临床表现往往较重。AAD的治疗原则主要包括停用或调整抗菌药物,补液、止泻以及应用微生态制剂调节肠道菌群等[33-34]。本研究通过对国内外指南、专家共识以及Meta分析文献的系统梳理,发现应用微生态制剂可有效预防儿童AAD的发生,且具有较好的安全性。成本分析结果显示,应用微生态制剂预防儿童AAD,成本负担轻,可以减少抗菌药物的使用,节约成本。
目前微生态制剂在全国应用广泛,品种多,且多为复方制剂,菌种的组成和剂量不尽相同。但其在儿科临床应用的不合理现象仍较为突出,本课题组前期调研结果显示其在超说明书用药方面仍存在很大问题。主要体现在:①超适应证用药现象普遍:调研全国36家儿童医院213名医生,86.3%(184/213)的被调查者存在超适应证用药问题。②超用法用量及超人群用药比例较高:因大多数微生态制剂说明书中无具体的儿童用法用量,因此分别有89.7%(191/213)、62.9%(134/213)的被调查者存在超用法用量、超人群用药问题。③个别调查者将微生态制剂灌肠应用,但是微生态制剂作为药物,灌肠后的体内过程,包括药物存留时间、在体内的定植和繁殖、对肠道原有菌群的影响等均不明确,其安全性及有效性均有待考证。因此,虽然已有大量循证医学证据证明微生态制剂在预防儿童AAD方面的作用,遵循药品临床应用指导原则、临床诊疗指南和药品说明书等合理使用微生态制剂仍是前提。
除此之外,目前普遍认为,几乎所有的抗菌药物均有可能引起AAD,而长期使用三代头孢菌素及其与其他抗菌药物联合治疗的患者中AAD的发生率在50%以上[3]。因此,除应用微生态制剂预防儿童AAD的发生外,合理使用抗菌药物、减少抗菌药物滥用,是从源头减少AAD发生的有效策略。
本研究的局限性主要体现在以下两方面:①艰难梭菌是AAD的主要病原菌,但因艰难梭菌相关性腹泻(Clostridium difficile-associated diarrhea,CDAD)属于感染性腹泻范畴,与AAD的发病机制不完全相同,本研究未纳入相关研究文献。后续可以进一步开展微生态制剂预防儿童艰难梭菌相关性腹泻的研究。②由于国内外相关文献不足,本研究仅对整体微生态制剂或单一菌种预防儿童AAD进行研究,未开展不同菌种间的比较研究。
综上,微生态制剂对于儿童AAD的预防安全有效,但对于有严重潜在健康问题的儿童仍缺乏使用经验,其规范合理的使用也应引起临床的足够重视。未来仍需进一步开展基于中国儿童的多中心、前瞻性研究,为儿童AAD的防治以及微生态制剂的合理使用提供更多的依据。

