临氢缓和条件下温度对煤-油共炼反应的影响
孙昱东,赵凌云,韩忠祥,顾 强
(中国石油大学(华东)化学工程学院,山东 青岛 266580)
与国外相比,我国的能源储量特点是“贫油富煤少气”,虽然煤炭资源相对较丰富,但利用方式主要是作为燃料直接燃烧,能源利用率低且带来了一系列环境问题;而随着国内外对石油资源需求量的与日俱增,原油重质化与劣质化问题越来越突出,石油加工过程也面临着一系列严峻的挑战。为了适应能源发展趋势及我国的国情,需要充分发挥我国的能源优势,除实现资源的高效清洁利用以外,还应积极寻求可替代能源和新的能源利用途径[1-4]。随着近几年煤直接液化技术的发展,煤-油共炼技术取得了重大进展。煤-油共炼技术是以劣质重油代替传统煤直接液化过程中溶剂油的新型煤液化技术[5],煤-油共炼过程中,利用煤与溶剂油的协同效应,进行裂解、加氢等一系列复杂的化学反应以制备轻质油品,是煤清洁化利用的技术之一,既是我国对煤炭资源利用途径的创新,又可以解决石油资源劣质化和重质化的问题。在此过程中反应条件以及原料性质的改变均会对反应结果产生不同程度的影响。本课题主要探索反应温度对煤-油共炼过程反应结果的影响。
1 实 验
1.1 原 料
试验原料为3种不同来源和属性的国产煤,编号分别为M0,M1,M2,其性质见表1。煤液化所用溶剂油为具有较好供氢性能的催化裂化油浆,取自中国石油长庆石化公司两段提升管催化裂化装置,其主要性质见表2。
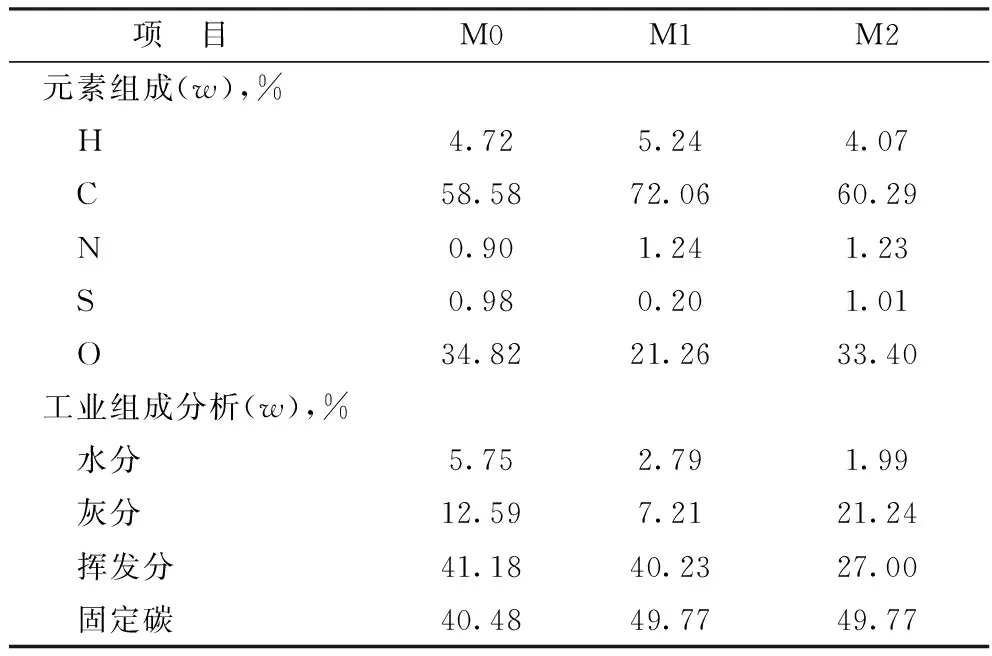
表1 原料煤的性质
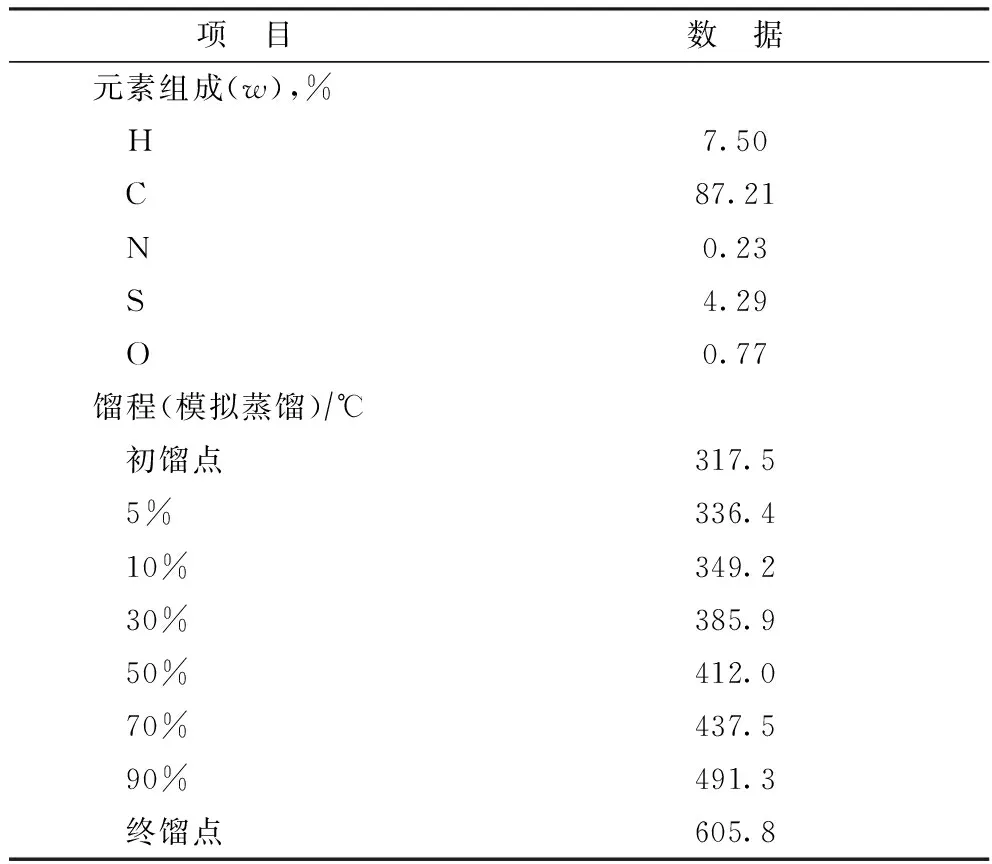
表2 催化裂化油浆的性质
1.2 试验方法
煤-油共炼反应试验在CQF0.15高压反应釜中进行,根据课题组前期的研究结果[6],在煤油质量比为1∶2、氢初始压力为3.5 MPa或5.0 MPa、反应时间为60 min的条件下,考察反应温度对煤液化率及产物性质的影响。
将原料煤经研磨后,选取颗粒小于100目的煤粉作为反应原料。将干燥后的煤粉、作为溶剂油的油浆、自制的铁系催化剂[6]以及硫助剂同时加入高压釜中,密封并用氮气试漏合格后,用氢气连续吹扫3次以置换高压釜中的空气,然后通入试验方案预定压力的氢气;打开冷却水,接通加热电源,升温高压釜至试验方案预定的温度后,开始计时反应;直至设定的时长,停止加热和搅拌,将高压釜从加热炉中取出并放入水浴中冷却,待釜温降至40 ℃以下时,通过排水集气法收集气体产物,采用索氏抽提器以甲苯为溶剂抽提分离液体和固体产物,并对所得产物进行物性和组成分析。
1.3 液化率计算
煤的液化率是评价煤-油共炼过程的一个重要指标,其计算方法见式(1)。
(1)
式中:Y为煤的液化率,%;m0为原料煤的质量,g;mc为催化剂的质量,g;ms为固体产物的质量,g;mg为气体产物的质量,g。
2 结果与讨论
2.1 反应温度对煤液化率的影响
原料煤在不同反应温度下的液化率见表3。
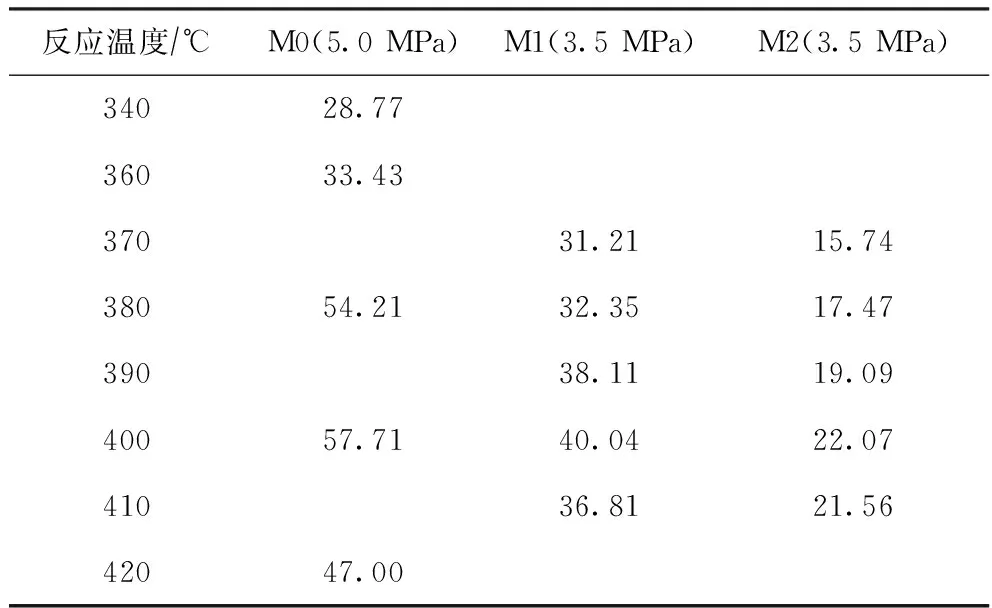
表3 不同反应温度下煤的液化率 %
由表3可以看出:反应温度对煤的液化率具有明显的影响,随着反应温度升高,3种煤的液化率均呈现先增大后减小的变化趋势;对于M0,在反应温度由340 ℃升高到360 ℃时液化率增长较缓慢,当温度由360 ℃升高到380 ℃时液化率快速增长,在400 ℃时液化率达到最高值,然后随温度进一步升高液化率呈下降趋势;对于M1,在反应温度由370 ℃升高到380 ℃时液化率呈缓慢增长趋势,当温度由380 ℃升高到390 ℃时液化率快速增长,其后液化率增长速率放缓,并于400 ℃时达到最大值,然后随温度进一步升高呈下降趋势;对于M2,在反应温度由370 ℃升高到400 ℃的过程中,液化率一直呈缓慢增长趋势,于400 ℃时达到最大值,温度超过400 ℃后,液化率呈现下降趋势。
煤是一种组成复杂的混合物,主要是由大量的有机物及少量的无机物和矿物质组成,多变的自然环境导致了煤炭结构的复杂性和多样性,通常认为煤是由相似的“结构单元”通过各种桥键连接而成的超分子结构[7],其间还包容着各种有机小分子物质。在煤-油共炼过程中,主要存在加氢裂解和缩聚两种方向相反的反应[8-12],且两种反应之间存在着竞争关系。随着反应温度的升高,首先发生以浸出为主的物理变化过程,即煤逐渐被软化,小分子有机物从煤中逸出并溶解于溶剂中,发生的是以分子间作用力削弱和破坏为主的变化;随着反应温度逐渐升高,煤分子逐渐被活化,较弱的化学键开始断裂并释放出部分小分子,由于这部分化学键的键能较低,反应速率较快,煤的液化率迅速增长;随着反应温度进一步提高,活化分子数增加,某些键能较大的化学键也开始断裂,生成大量的自由基碎片[13],使反应速率和液化率持续增加。虽然高温有利于加氢裂解反应的进行,但过高的温度会使煤快速分解并产生大量的自由基碎片[14],因自由基碎片来不及加氢而重新缩聚生成大分子,且受煤的结构和化学性质影响,本身可分解的有机大分子数量有限,高温下发生过多的缩聚反应,反而会引起煤的液化率降低。
不同煤化程度的原料煤的液化性能受反应温度的影响也有所不同,一般来说,氢碳原子比(nH/nC)大、挥发分含量较高的煤更容易液化[15]。与褐煤M0、M1相比,M2作为一种烟煤,其中可参与加氢裂化反应的有机大分子含量相对较少,因此液化率较低,且随着温度的升高,其液化率增加的速率比较缓慢,远远低于M0和M1;但是过高的反应温度有利于烟煤的缩聚反应,因此会出现液化率先增加后减小的变化趋势。
2.2 反应温度对半焦性质的影响
选取M1和M2为原料煤,在氢初始压力为3.5 MPa时,考察反应温度对煤液化后所得半焦性质的影响,结果见表4和表5。

表4 不同反应温度下M1液化后所得半焦的性质 w,%
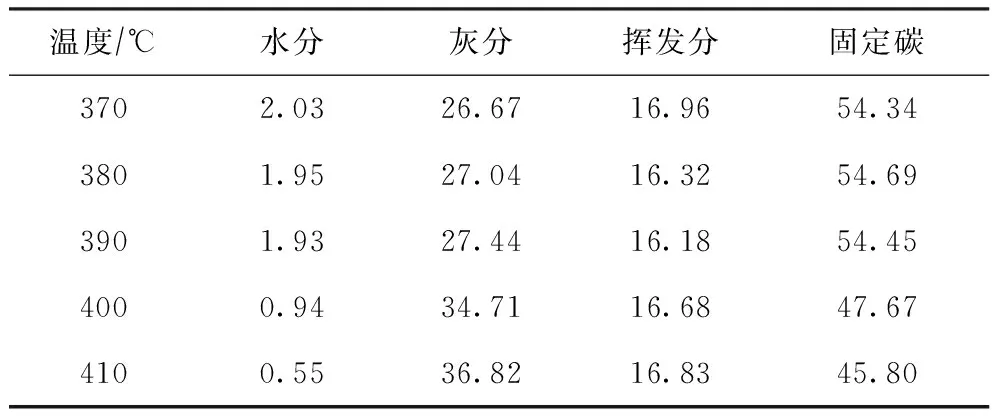
表5 不同反应温度下M2液化后所得半焦的性质 w,%
由表4可以看出,随着反应温度升高,M1液化后所得半焦的挥发分含量逐渐减少,固定碳含量呈先增加后减小的变化趋势,而灰分含量则逐渐上升。由表5可以看出,随着反应温度升高,M2液化后所得半焦的挥发分含量呈先减小后增加的变化趋势,但总体变化幅度不大,固定碳含量逐渐减小,灰分含量逐渐上升。
在煤的液化过程中,不同组分的反应性能和反应方向不同。挥发分是容易发生反应的组分,通过加氢裂解生成小分子,是影响液化率的主要因素,温度升高有利于促进挥发分加氢裂解生成小分子油品;固定碳组分可以通过加氢裂解反应生成挥发分,使其含量降低,但反应的难度较大,反应速率较低;灰分基本不参与任何反应,绝对含量保持不变,但随着反应过程中挥发分和固定碳含量的逐渐减少,灰分在半焦中的相对含量逐渐上升。
对于M1,在反应温度370~390 ℃之间,随着温度升高,加氢裂解反应加剧,挥发分含量持续减少,灰分的相对含量增加,难于反应的固定碳的相对含量也略有增加;当温度超过390 ℃后,固定碳开始发生明显的加氢裂解反应,首先生成挥发分,再进一步加氢分解生成更轻的组分,但因为反应温度相对较低,反应速率和所生成挥发分含量的增加有限,而挥发分的加氢分解反应速率持续增加,所以,固定碳和挥发分的含量均减少。对于M2,在反应温度370~390 ℃之间,随着温度升高,加氢裂解反应速率增加,挥发分含量持续减少,灰分相对含量增加,固定碳含量由于加氢裂解反应速率低而变化不明显;当温度超过390 ℃以后,固定碳开始发生明显的加氢裂解反应而生成挥发分,其含量开始降低,但由于M2的挥发分含量较低,固定碳组分在比较苛刻的条件下转化为挥发分的速率大于挥发分的加氢分解速率,因此挥发分含量略有增加。
2.3 反应温度对液化油性质的影响
以M0为原料煤,在氢初始压力为5.0 MPa的条件下,考察反应温度对煤液化后所得液化油性质的影响,结果见表6。
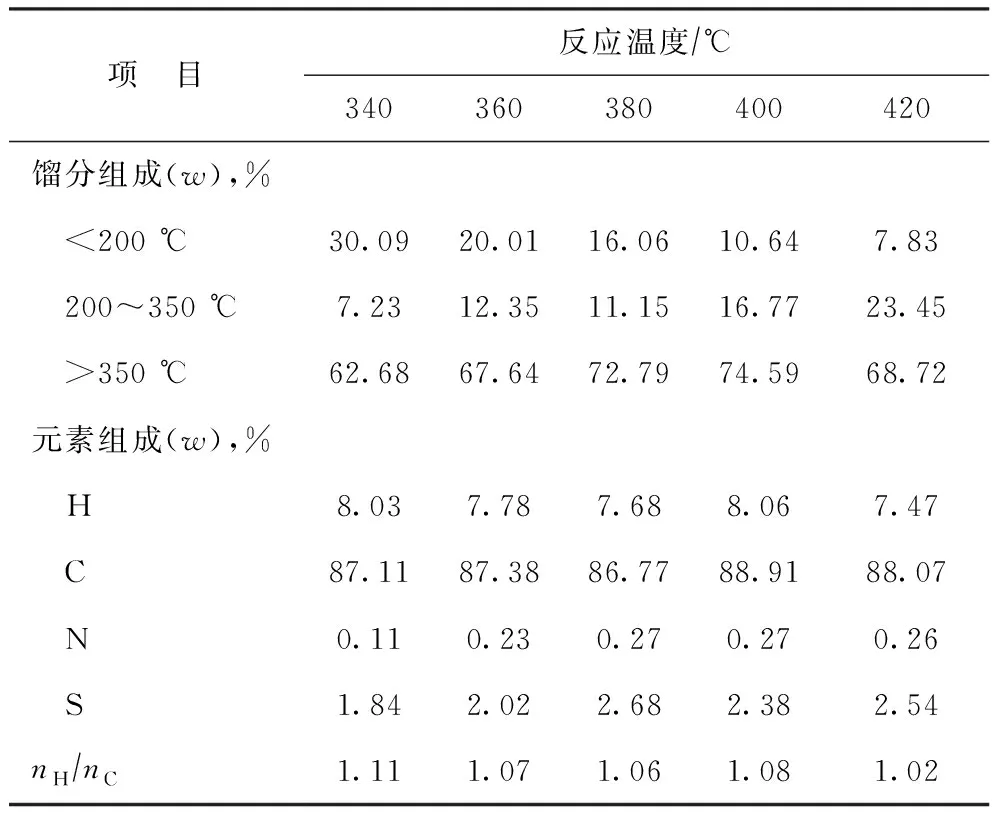
表6 不同反应温度下M0液化后所得液化油的性质
由表6可以看出:随着反应温度升高,液化油中的汽油馏分(<200 ℃)含量逐渐减小,柴油馏分(200~350 ℃)含量逐渐增加,渣油馏分(>350 ℃)含量则呈先增加后减小的变化趋势;nH/nC逐渐减小,杂原子S、N含量则逐渐增加。
前文已经提到,随着反应温度升高,煤的液化率呈先增加后减小的变化趋势,温度由340 ℃提高到400 ℃时,液化率逐渐增加,液化油收率也逐渐增加,但由于煤液化的直接产物大部分是沥青烯(正己烷不溶而甲苯可溶的物质)和前沥青烯(甲苯不溶而四氢呋喃可溶的物质)[16],含有大量的稠环结构,相对分子质量和沸点较高,导致液化油的重组分含量逐渐增加,轻油含量则逐渐减少,油品的nH/nC逐渐降低。煤及其液化产物沥青烯中含S、N等杂原子结构较多,引起液化油的杂原子含量逐渐增加。当反应温度高于400 ℃时,缩聚反应加剧,液化油的重组分含量开始降低。
3 结 论
(1)在煤-油共炼过程中,主要存在加氢裂解和缩聚两种竞争反应,影响煤的液化率。煤-油共炼存在一个最佳反应温度,当反应温度较低时,加氢裂解反应占优势,提高反应温度有利于煤的液化;反之,则缩聚反应占优势,提高反应温度使煤的液化率呈下降趋势。随着反应温度升高,煤的液化率先增加后减小。
(2)升高反应温度会促进煤的裂解反应,半焦中挥发分含量逐渐降低;随着反应温度进一步升高,固定碳转化为挥发分的能力逐渐增强,挥发分含量会缓慢增加,固定碳含量降低;灰分不参与反应,其绝对含量不变,但相对含量随温度升高而逐渐增加。
(3)随着反应温度升高,液化油中汽油馏分含量逐渐降低,柴油馏分含量逐渐增加,渣油馏分含量则先增加后降低;液化油的nH/nC逐渐减小,S、N等杂原子含量逐渐增加。

