青霉素在硼掺杂金刚石薄膜电极上的电化学行为研究
曲有鹏,吕江维,冯玉杰,张杰
(1.哈尔滨工业大学 城市水资源与水环境国家重点实验室,黑龙江 哈尔滨 150090;2.哈尔滨工业大学 生命科学与技术学院,黑龙江 哈尔滨 150080;3.哈尔滨商业大学 药学院,黑龙江 哈尔滨 150076)
青霉素是临床上广泛使用的一类抗生素,由于频繁超剂量的使用,已引起严重的环境污染,严重威胁人类健康[1-4]。因此对青霉素类抗生素的检测及分析十分必要。硼掺杂金刚石(BDD)薄膜电极是一种理想的电极材料,背景电流很小,灵敏度较高,用于电化学分析时利于研究一些目标物在较高或较低电位下的氧化还原反应[5-9]。因此BDD电极在电化学分析中具有一定的优势。本文以典型的青霉素为目标物,采用循环伏安法(CV)和电化学交流阻抗谱(EIS)来研究青霉素在BDD电极上电化学过程及电极动力学参数,探讨相应的反应机理,对BDD电极用于电化学分析抗生素类药物具有一定的参考价值。
1 实验部分
1.1 试剂与仪器
氢气(纯度99.999%);甲烷(纯度99.999%);硼酸三甲酯、无水Na2SO4均为分析纯;青霉素G钠(1 650 U/mg)。
PARSTAT2273电化学工作站。Pt电极;Ti板;Ag/AgCl参比电极。
1.2 BDD电极制备
采用直流等离子体化学气相沉积设备进行高压辉光放电,利用反应气体氢气(并以氢气为载气将硼酸三甲酯带入腔体内)和甲烷进行反应解离,将碳原子沉积于基体材料单晶硅片表面,控制电压、温度、气源比例等的参数沉积得到BDD薄膜[10]。
1.3 电化学分析方法
电化学分析方法采用CV和EIS,测试在PARSTAT2273电化学工作站上进行,选用三电极体系(其中工作电极:BDD电极,对电极:Pt电极,参比电极:Ag/AgCl电极)。配制浓度为2.0 g/L的青霉素G钠溶液(含0.1 mol/L的Na2SO4为电解质)。CV测试的扫描电势范围是-1.5~2.5 V(vs.Ag/AgCl),从开路电位(OCP)开始正向扫描至2.5 V,再负向扫描至-1.5 V,扫描速率分别为5,10,20,50,80,100 mV/s。EIS测试频率范围为10-2~104Hz,交流电的振幅为5 mV,极化电位分别为OCP和1.2,1.5,1.8,2.0,2.1,2.2,2.3,2.4,2.5 V(vs.Ag/AgCl),数据采用ZSimpWin 3.10 软件结合选取的适宜的等效电路进行各电化学元件阻抗参数的拟合。
2 结果与讨论
2.1 循环伏安CV测试
图1是在青霉素G钠溶液中扫描速率为20 mV/s,扫描5圈的CV曲线。
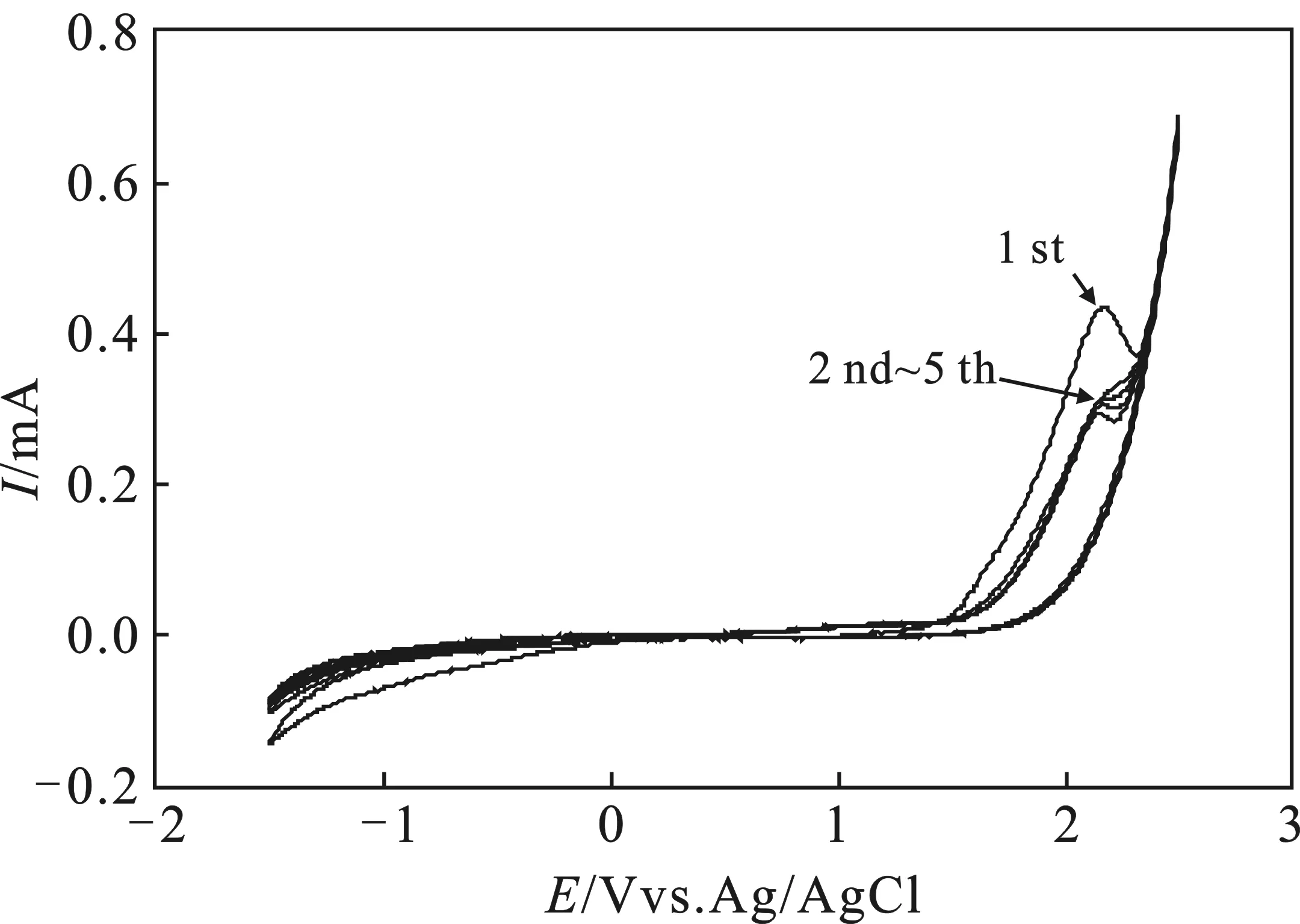
图1 青霉素G钠溶液中BDD电极的CV测试
由图1可知,扫描第1圈时出现了较强的氧化峰,氧化峰电位为2.2 V,峰电流为0.4 mA,在随后的第2~5圈时氧化峰变小,说明电极表面有中间产物的吸附引起的钝化现象。前期在研究苯酚在BDD电极上的电化学行为时也出现了聚合物形成的薄膜吸附在电极表面使氧化峰电流减小[11]。但对使用后吸附钝化的BDD电极,在大于H2O的电解电势下持续通电氧化后电极表面可以自清洁恢复原来的活性。对青霉素G钠负向扫描时没有出现还原峰,说明青霉素G钠在电极上的电化学氧化过程为不可逆过程。
由于电极在扫描多次后有钝化现象,为了提高测试的灵敏度响应性,因此对不同扫描速率条件下的CV曲线取第1圈的扫描结果,且每次扫描后均对电极表面进行清洁活化。图2是扫描速率为5,10,20,50,80,100 mV/s的CV曲线。

图2 青霉素G钠溶液中BDD电极在不同扫描速率的CV测试
由图2可知,不同扫描速率下,青霉素G钠的氧化峰电流随扫描速率的提高而增大,氧化峰电位也出现正移现象。
2.2 电化学阻抗谱EIS
对不同电位条件下青霉素G钠在BDD电极上的EIS进行测试,得到的Bode图见图3。

图3 青霉素G钠在不同电位下的Bode图
由图3可知,Bode图所有曲线都只有1个峰值,说明有1个时间常数,因此拟合选择的等效电路应该有1个电容元件。所以利用图5含有一个电容元件的两种等效电路进行拟合,将测试得到Nyquist图和相应拟合曲线进行比较(如图5所示),并将拟合得到的等效电路各元件的参数值列于表1中。
由于存在“弥散效应”,Nyquist图(图5)中的圆弧并不是标准的半圆轨迹,而是略有偏离半圆的轨迹,这可能与电极表面的不均匀性、电极表面的吸附层剂溶液导电性差有关,因此用常相位角元件代替了纯电容,以获得更好的拟合结果[12-14]。

图5 青霉素G钠在不同电位下的Nyquist图及拟合曲线
由表1可知,不同电位下溶液电阻Rs的平均值为(131.2±7.5) Ω·cm2,图5(a)~(c)分别对应OCP、1.2 V及1.5 V时的Nyquist图,OCP为平衡电位,此时不发生氧化还原反应;Nyquist图为一个高频端的容抗弧紧接着一个斜率角约为π/4的Waburg阻抗直线,因此按照Rs(Q(RctW))的等效电路拟合(图4(a)),拟合得到的误差也最小,对应的电荷转移电阻Rct由4.193×104Ω·cm2(OCP)降至3 776 Ω·cm2(1.5 V),韦伯阻抗Zw由2.358×10-5S·s0.5/cm2(OCP)增加至7.98×10-4S·s0.5/cm2(1.5 V),说明该电位范围内电荷传递动力学不是很快,电极过程由电荷传递过程和扩散过程共同控制,电化学极化与浓差极化同时存在。图5(d)~(j)对应1.8~2.5 V时的Nyquist图,此时的阻抗图为不同直径的圆弧,此电位范围内发生了青霉素G钠的氧化反应,此时电极过程由电荷传递过程控制,没有扩散过程引起的阻抗,因此按照Rs(QRct)的等效电路拟合,拟合的误差最小。电荷转移电阻Rct先从3 776 Ω·cm2(对应1.8 V)降至316.8 Ω·cm2(对应2.1 V),又增加至631.9 Ω·cm2(对应2.2 V),再降低至270.4 Ω·cm2(对应2.5 V)。在2.2 V出现Rct的峰值的原因可能与该电位条件下除了青霉素的氧化反应外,还有H2O在电极上的电解反应,产生·OH并进一步生成O2有关[15-16]。

图4 EIS拟合的等效电路
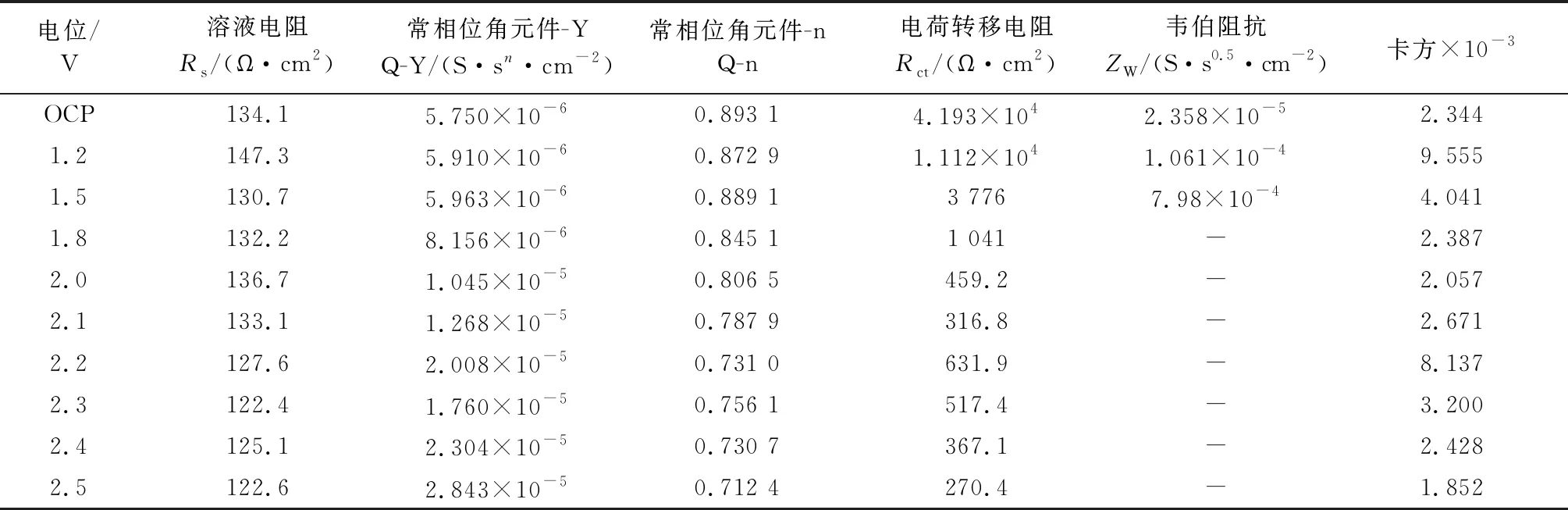
表1 青霉素G钠在不同电位下等效电路的拟合结果
3 结论
青霉素G钠在BDD电极上的电化学过程为不可逆过程,只有氧化峰出现,峰电位为2.2 V,没有还原峰出现。氧化的中间产物在电极表面有吸附,导致氧化峰电位逐渐降低。但在高于水分解电压下电解中间产物,电极能够恢复原来的活性。当电极电位在OCP至1.5 V时,电荷转移电阻Rct由4.193×104 Ω·cm2(OCP)降至3 776 Ω·cm2(1.5 V),韦伯阻抗Zw由2.358×10-5 S·s0.5/cm2(OCP)增加至7.98×10-4 S·s0.5/cm2(1.5 V),电极过程主要受电荷传递过程和扩散过程共同控制,电化学极化与浓差极化同时存在。当电极电位在1.8~2.5 V时,电荷转移电阻Rct先从3 776 Ω·cm2(对应1.8 V)降至316.8 Ω·cm2(对应2.1 V),又增加至631.9 Ω·cm2(对应2.2 V),再降低至270.4 Ω·cm2(对应2.5 V),在2.2 V出现Rct的峰值的原因可能与该电位条件下除了青霉素的氧化反应外,还有H2O在电极上的电解反应,产生·OH并进一步生成O2有关,电极过程主要由电荷传递过程控制。

