ICP-MS 测定甲磺酸帕珠沙星注射液及甲磺酸帕珠沙星氯化钠注射液中的12 种元素
胡幸 朱晓璐
(重庆市食品药品检验检测研究 重庆 401120)
甲磺酸帕珠沙星为第四代喹诺酮类抗菌药,由日本富山化学株式会社研发,2002 年在日本获批上市,国内于2004 年批准上市。本品通过抑制细菌DNA 旋转酶和DNA 拓扑异构酶IV 活性,阻碍DNA 合成而导致细菌死亡,具有抗菌谱广、抗菌作用强的特点[1]。主要不良反应有过敏反应、消化道反应、肝毒性和肾毒性等。虽然甲磺酸帕珠沙星原料在合成过程中未使用催化剂,但原料和制剂的生产使用过程中易通过原料、辅料、生产设备、包材等多种途径引入药品中,而且各种工艺在药品的生产过程中,并不能对重金属完全消除。拟采用电感耦合等离子体质谱法(ICP-MS)测定制剂中的砷(As)、汞(Hg)、镉(Cd)、铅(Pb)等12 种元素[2],全面评价药品的质量。
1.仪器与试药
微波消解仪:美国培安公司MARS6
电感耦合等离子体质谱仪(ICP-MS):珀金埃尔默公司NeXIDN350X
混合标准溶液:国家标准样品(GSB 04-1767-2004)多元素标准溶液,唯一标识:185009-1
汞标准溶液:国家标准样品(GSB 04-1767-2004)单元素标准溶液,唯一标识:19B019-3
优级纯硝酸(川东化工,65%~68%)
2.方法
2.1 样品前处理方法
消解罐内精密称取各样品约1g,加优级纯的硝酸5ml,盖好,静置10 分钟,再用微波消解仪进行消解[3]。微波消解完全后,用超纯水转移并定容至25ml。
2.2 稀释剂的配制
用优级纯的硝酸加超纯水配制成2%的稀硝酸溶液[4]。
2.3 标准曲线的配制
精密量取标准液适量,加稀释剂配制成质量浓度0、10、20、50、100、200ug/L 混合标准溶液[5]。
2.4 仪器使用的条件
2.4.1 微波消解参数见表1。
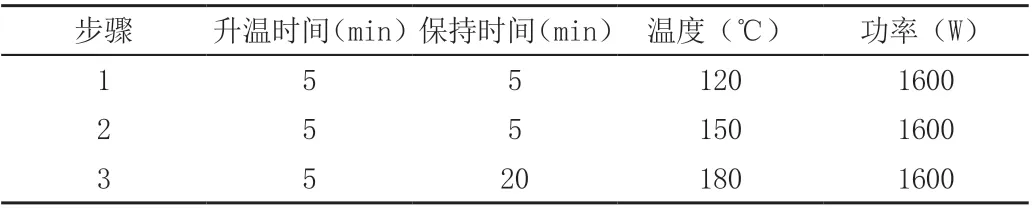
表1 微波消解参数表
2.4.2 电感耦合等离子体质谱仪(ICP-MS)仪器条件,选择干扰较小的He 碰撞模式,蠕动泵10r/min,雾化室温度2℃,跳峰扫描100 次,积分时间0.20s,采样深度:10mm,载气流量:1.03L/min。
2.5 测定的12 种元素线性方程及各自的检出限,见表2。
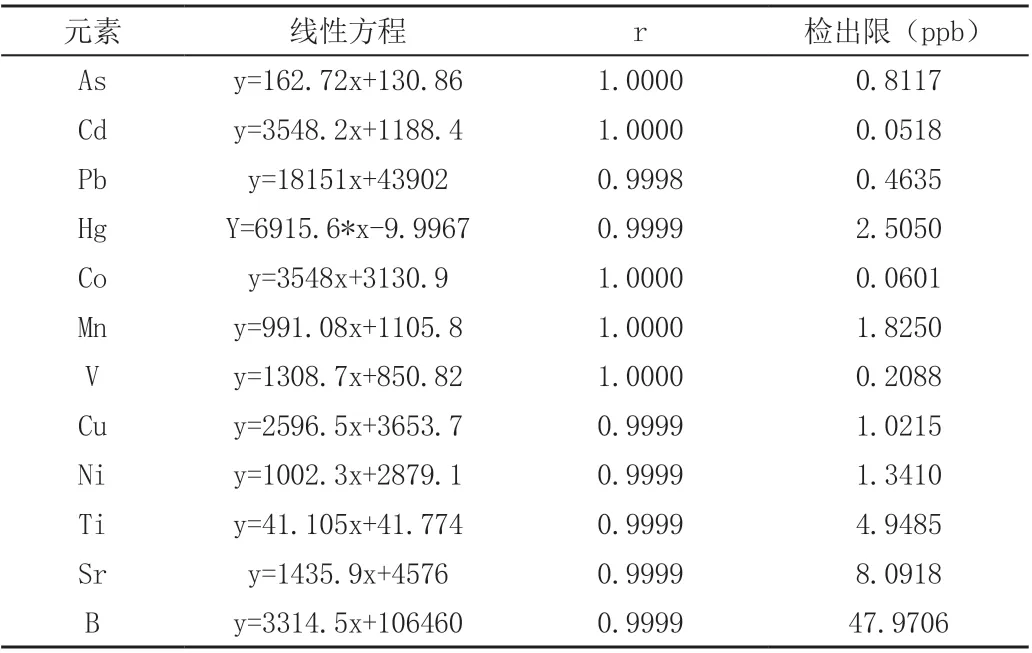
表2 测定的12 种元素的线性方程及各自的检出限
3.结果
测定114 批样品结果,砷、镉均未检出,铅有四批检出,含量为0.01ppm ~0.04ppm,汞有两批检出0.06 ~0.07ppm;A 公司生产的甲磺酸帕珠沙星注射液11 批中有9 批检测出钛元素,含量为:0.01ppm ~0.1ppm,6 批检测出硼元素,含量为:0.3ppm ~1.6ppm;B 公司生产的甲磺酸帕珠沙星氯化钠注射液4批有3 批检测出钛元素,含量为:0.02ppm ~0.1ppm。C 公司生产的2批甲磺酸帕珠沙星氯化钠注射液均检测出硼元素,含量为:0.1ppm;D 公司生产的甲磺酸帕珠沙星注射液4 批中有3 批检测出硼元素,含量为:0.1ppm ~0.6ppm;E 公司生产的甲磺酸帕珠沙星注射液4 批,均检出硼元素,0.4ppm ~1.3ppm。
4.讨论
4.1 根据ICHQ3D(R1) 最新规定元素分类:砷、铅、汞、镉为1 类,样品均为注射剂, Patenteral PDE 分别为:As 15μg/day,Cd 1.7μg/day,Pb 5μg/day,Hg 3.0μg/day。检测结果显示,1 类重金属其含量均远小于PDE,不影响药物安全性。
4.2 分析其他元素结果发现,大部分检测出TI 元素的为输液包装袋,初步推断TI 元素为包材引入。大部分检测出B 元素的都为小针剂,初步推断可能为设备或包材引入。具体原因有待进一步分析。

