朗伯-比尔定律的适用条件与限制
辛伍红
(山东理工大学 分析测试中心,山东 淄博 255000)
物质对光吸收的定量关系很早就引起了科学家的注意。皮埃尔·布格和约翰·海因里希·朗伯分别于1729年和1760年阐明了物质对光的吸收程度和吸收介质厚度之间的关系。1852年奥古斯特·比尔进一步提出了光的吸收程度和吸光物质浓度也具有类似关系。两者结合起来就得到了有关光吸收的基本定律——布格-朗伯-比尔定律,简称朗伯-比尔定律(Lambert-Beer law),这一定律是分光光度法的基本定律和定量基础[1-3]。
然而,朗伯-比尔定律是一个有限定律,入射光单色性差、溶质和溶剂的性质等均会导致偏离。例如,比尔定律只适用于稀溶液,因为浓度高时,吸光物质粒子平均距离减小,相互作用增强,受粒子间电荷分布相互作用的影响,摩尔吸收系数ε发生改变,导致偏离。因此,分光光度法的实验是基于关键定律适用的情形进行设置的[4-8]。在实验教学的过程中,研究者发现多数学生存在对适用条件不甚理解的情况。因此,本论文以紫外分光光度法测量布洛芬含量为例,分析定律适用条件对实验设置的影响,提高学生理论联系实际的能力[9, 10]。
1 朗伯-比尔定律的适用条件
朗伯-比尔定律描述了物质对光的吸收程度和吸收介质厚度、吸光物质浓度间的正比关系,其数学表达式如下[9]:
A=εbc=lg(1/T)
(1-1)
A为吸光度;ε为吸光系数,为常数;b为吸收层厚度;c为物质的浓度;T为透光率,T=It/I0,其中It为透射光强度,I0为入射光强度。
其物理意义是当一束平行单色光垂直通过某一均匀非散射的吸光物质时,其吸光度A与吸光物质的浓度c及吸收层厚度b成正比。具体适用条件如下:
(1) 入射光为平行单色光且垂直照射;
(2) 吸光物质为均匀非散射体系;
(3) 吸光质点之间无相互作用;
(4) 辐射与物质之间的作用仅限于光吸收,无荧光和光化学现象发生;
(5) 吸光度在0.2~0.8之间。
根据适用条件(3)和(4),当被测物与溶质无相互作用、与辐射间仅存在吸收作用时,以下公式成立:
I0=Ia+It+Ir
(1-2)
Ia为吸收光强度;Ir为反射光强度。
适用条件(2)中非散射体系的限制使Ir=0,公式(1-2)可以简化为:
I0=Ia+It
(1-3)
此时公式(1-1)中对T的定义成立。
通过上述讨论可以看出,朗伯-比尔定律适用条件(2)~(4)是针对实验体系做出的限制。本论文以布洛芬的氢氧化钠溶液为待测物,在该体系中,吸光物质为均匀非散射体系、吸光质点间无相互作用、辐射(紫外光)与物质间仅存在光吸收,满足适用条件(2)~(4)。以下讨论适用条件(1)和(5)成立的情形。
2 适用条件(1)的成立
紫外可见分光光度计主要由光源、单色器、样品池和检测器四个部分组成。其中单色器是指将光源发出的光分离成所需要的单色光的器件,由入射狭缝、准直镜、色散元件和出射狭缝构成。入射狭缝用于限制杂散光进入单色器;准直镜将光源发出的发散光变成平行光;色散元件是单色器的关键部件,作用是将复合光分解成单色光;出射狭缝用于限制通带宽度。可以看出,光源发出的混合光经单色器作用后满足适用条件(1)的“平行”和“单色光”描述。值得注意的是,“垂直照射”这一条有非常重要的限定作用。如图1所示,当光垂直照射在样品池表面时,可以通过样品池的厚度描述吸收层厚度b。而非垂直照射时,不但在样品池表面会发生反射Ir≠0,导致朗伯-比尔定律不成立,入射角度的差异也会影响吸收层的厚度。可见,在保证仪器稳定性的前提下,当样品池表面与色光通路垂直时,适用条件(1)成立。
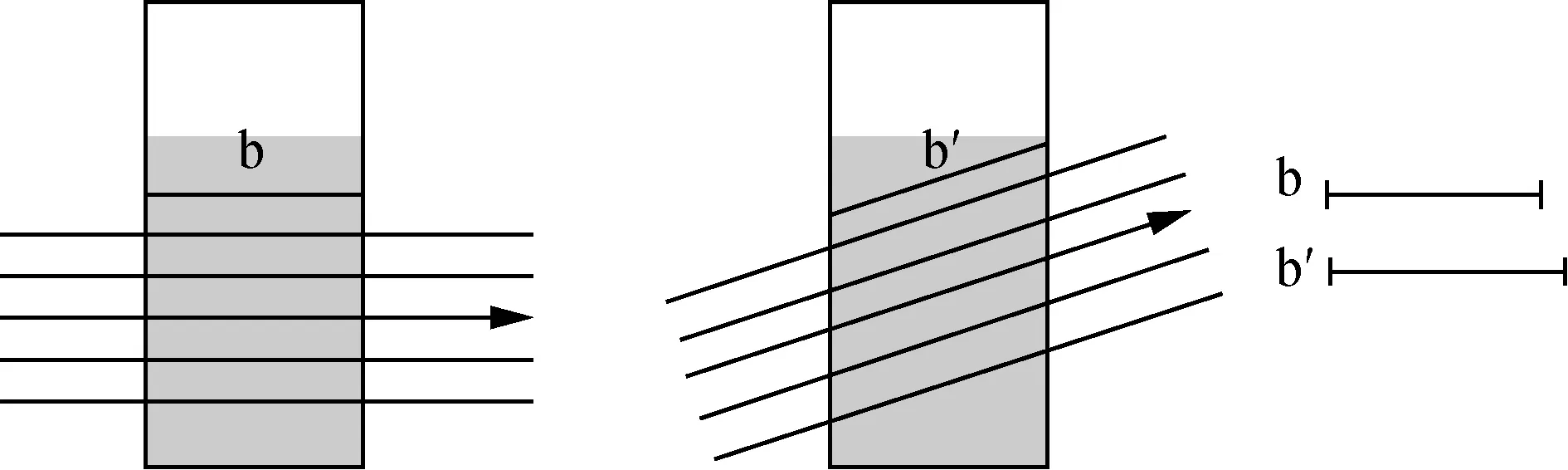
图1 入射光垂直照射和非垂直照射时吸收层的厚度示意图
3 适用条件(5)的成立
为了进一步理解适用条件(5)中对吸光度值限定的意义,分别配制标准溶液和参照溶液组。
3.1 标准溶液和参照溶液的配制
准确称取250 mg布洛芬标准品,溶于0.4%氢氧化钠溶液中,定容至50 mL,得到浓度为5 mg/mL的标准储备液。用移液管分别移取5、10、15、20和25 mL的标准储备液,用250 mL容量瓶定容,稀释溶剂为0.4%氢氧化钠溶液,制成0.10、0.20、0.30、0.40和0.50 mg/mL的标准溶液。
用移液管分别移取30、35、40、45和50 mL的布洛芬标准储备液,用250 mL容量瓶定容,稀释溶剂为0.4%氢氧化钠溶液,制成0.60、0.70、0.80、0.90和1.00 mg/mL的参照溶液。
3.2 测试及结果讨论
首先将标准溶液加入样品池中进行全波长扫描,获得吸收曲线并读取吸收峰对应的波长。图2所示为布洛芬标准溶液的吸收曲线,从图中可以观察到三个明显的吸收峰,分别位于226、264和272 nm。在分光光度法中,光吸收程度最大处叫做最大吸收波长,用λmax表示。根据定律,溶液浓度不同时,光吸收曲线的形状相同,λmax不变,只是吸光度与浓度成正比关系变化。依据此定义判断布洛芬氢氧化钠溶液的λmax。
首先研究不同波长处标准溶液和参照溶液组中物质浓度与吸光度间的关系,实验结果如图3所示。图3a为不同浓度布洛芬溶液在226 nm处的吸光度值,此时物质的吸光度与浓度不成线性关系,说明在226 nm处朗伯-比尔定律不成立,不符合λmax的定义。进一步研究264和272 nm波长处的情况,结果如图3b和3c所示。对标准溶液组(浓度0.10~0.50 mg/mL)而言,在264和272 nm处吸光度与浓度呈现良好的线型关系。根据定义,可以判断264 nm为布洛芬氢氧化钠溶液的λmax。
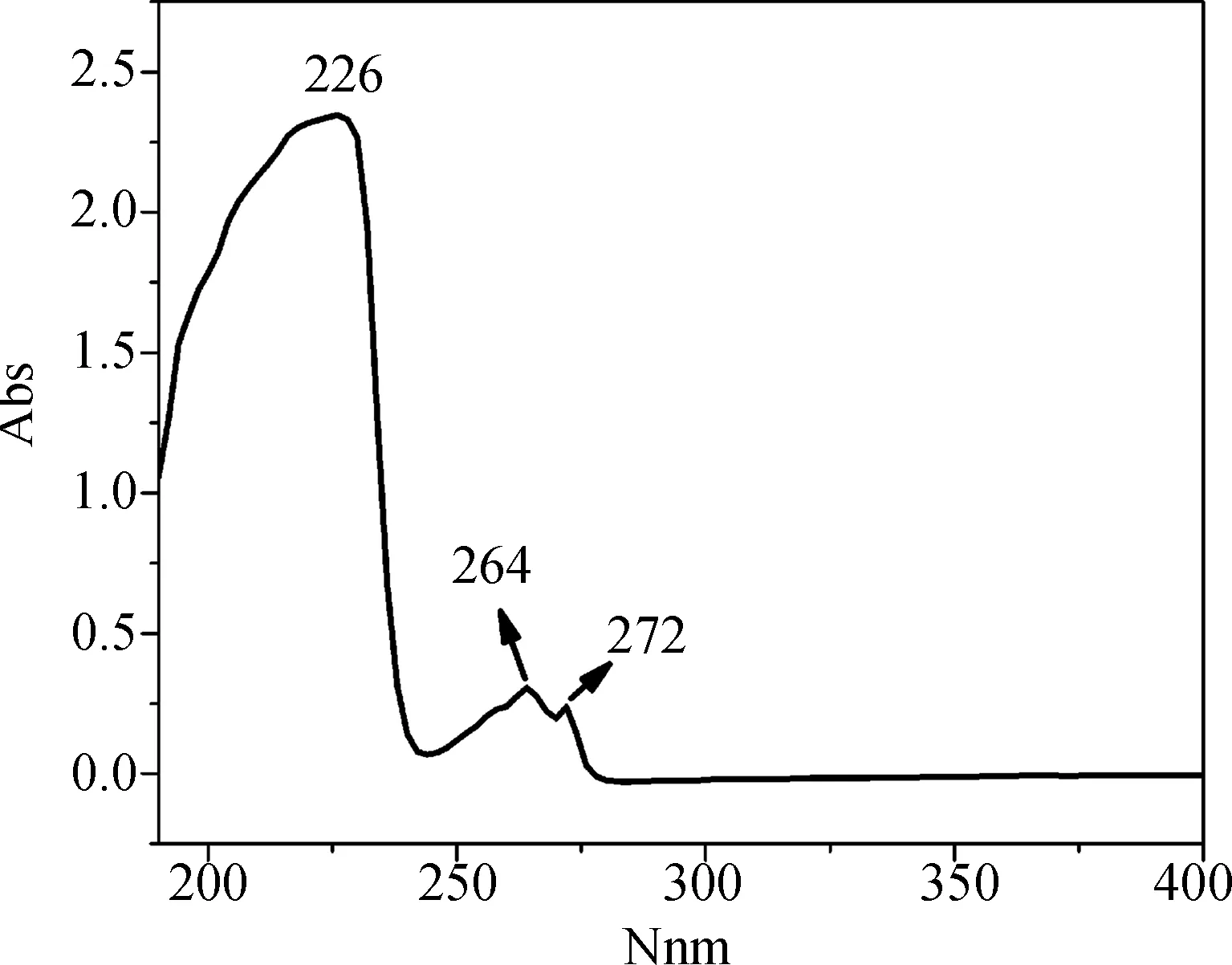
图2 布洛芬标准溶液的吸收曲线
进一步对比264和272 nm处标准溶液和参照溶液组间吸光度与浓度的关系,可以看出当溶液浓度增大后,两条吸收曲线均发生了负偏离。这主要是由于随着浓度的增大,布洛芬溶液的ε减小,导致实际曲线向浓度轴偏离。图3b和3c显示了随溶液浓度增大方差值(R2)的变化情况,可以用来指示实际曲线的负偏离程度。从R2的计算结果来看,在264和272 nm 处标准溶液组的吸光度-浓度曲线具有良好的线性(R2=0.999 9)。当溶液浓度进一步增大时,R2值逐步增大,负偏离程度不断加剧。在实际应用中,正偏离或负偏离都对分光光度法分析的准确性有重大影响。通过适用条件(5)的限定,可以帮助实验人员根据吸光度快速判断ε稳定的浓度区间,评估分光光度法分析对体系的适用情况。进一步观察图3c中的曲线可以发现,当溶液浓度升高至0.60 mg/mL时,尽管吸光度值低于适用条件(5)定义的最大值0.8,但数据点间的线性程度下降,R2降低。说明适用条件(5)中对吸光度的限定主要针对的是λmax处,合理的选择λmax很重要。
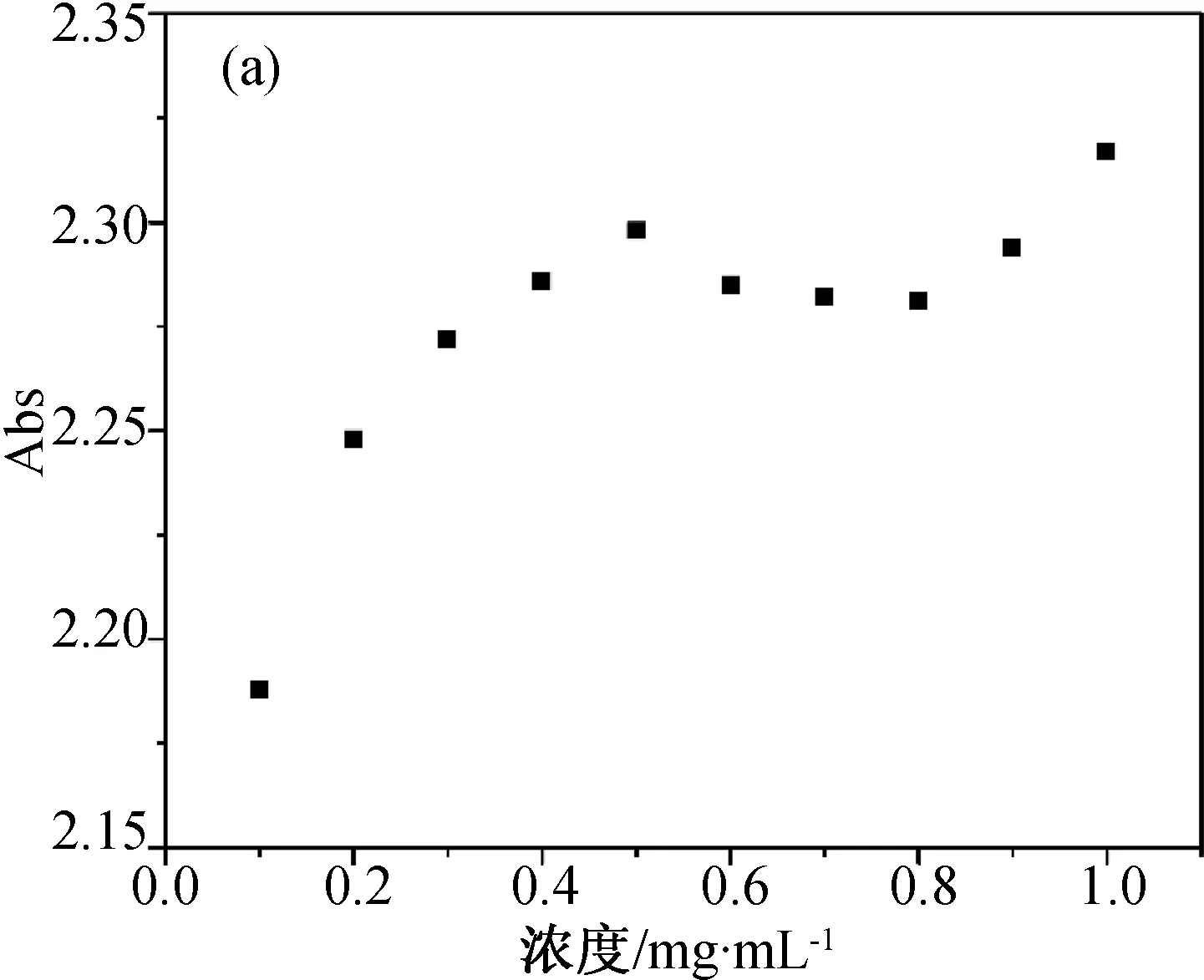
(a) 226 nm
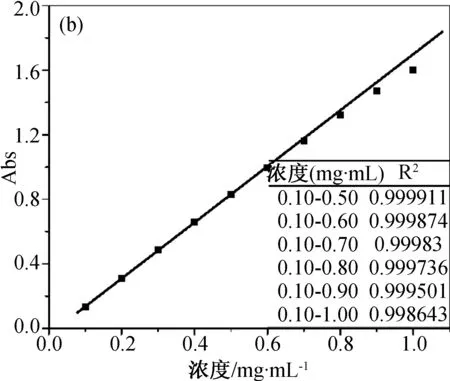
(b) 264 nm
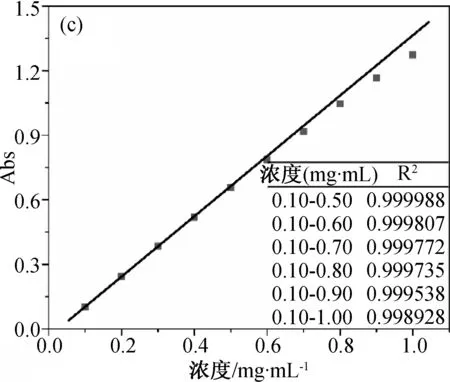
(c) 272 nm
根据本节的讨论,在实际测试中,需要首先根据朗伯-比尔定律的定义选择λmax,并进一步根据适用条件(5)选择合适的标准溶液浓度区间,确保分光光度法分析的准确性。
4 结语
实验教学的目的不仅在于培养学生的动手能力,更应侧重培养学生理论联系实际的能力。本论文从朗伯-比尔定律的定义和适用条件出发,以紫外分光光度法测量布洛芬含量为例,逐一研究适用条件限定的意义,明确分光光度法分析对体系的适用情况。通过这种逆向思考和讲解的方式,将课本上平面的定律变为立体的定律,培养了学生对实验方案的设计能力,体现了理论对实践的指导作用。这种教学方式有利于提升学生对基础理论的掌握,进一步激发学习热情,有极佳的课程效果。

