HPLC法同时测定舒肝和胃丸中5种成分的含量
宫兴华 郑磊 李娟


中图分类号 R917 文献标志码 A 文章编号 1001-0408(2020)14-1715-04
DOI 10.6039/j.issn.1001-0408.2020.14.10
摘 要 目的:建立同时测定舒肝和胃丸中7-羟基香豆素、6,7-二甲氧基香豆素、5,7-二甲氧基香豆素、欧前胡素、佛手柑内酯等5种成分含量的方法。方法:采用索氏提取法对舒肝和胃丸进行提取,经D101型大孔吸附树脂分离后,采用高效液相色谱法测定上述5种成分的含量。色谱柱为Venusil MP C18,流动相为甲醇-0.1%磷酸水溶液(梯度洗脱),流速为1.0 mL/min,检测波长为270 nm,柱温为30 ℃,进样量为10 μL。结果:7-羟基香豆素、6,7-二甲氧基香豆素、5,7-二甲氧基香豆素、欧前胡素、佛手柑内酯检测质量浓度的线性范围分别为1.875~187.5 μg/mL(r=0.999 9)、1.075~107.5 μg/mL(r=0.999 9)、1.261~126.1 μg/mL(r=0.999 9)、0.875~87.5 μg/mL(r=0.999 9)、2.033~203.3 μg/mL(r=0.999 8),精密度、穩定性(24 h)、重复性、耐用性试验的RSD均小于2.0%,平均加样回收率分别为95.18%~98.44%(RSD=1.27%,n=6)、95.35%~98.14%(RSD=1.16%,n=6)、95.21%~97.32%(RSD=0.83%,n=6)、95.43%~97.14%(RSD=0.76%,n=6)、95.12%~98.75%(RSD=1.35%,n=6)。3批舒肝和胃丸中上述5种成分的平均含量分别为0.424、0.239、0.305、0.180、0.459 mg/g(n=2)。结论:成功建立了可同时测定舒肝和胃丸中5种成分含量的方法。
关键词 舒肝和胃丸;高效液相色谱法;含量测定;7-羟基香豆素;6,7-二甲氧基香豆素;5,7-二甲氧基香豆素;欧前胡素;佛手柑内酯
Simultaneous Determination of 5 Components in Shugan Hewei Pills by HPLC
GONG Xinghua1,ZHENG Lei1,LI Juan2(1. Dept. of Pharmacy, Shandong Provincial Third Hospital, Jinan 250031, China; 2. Dept. of Pharmacy, the Second Hospital of Shandong University, Jinan 250033, China)
ABSTRACT OBJECTIVE: To establish a method for simultaneous determination of 7-hydroxycoumarin, 6,7-dimethoxy- coumarin, 5,7-dimethoxycoumarin, imperatorin and bergaptene in Shugan hewei pills. METHODS: Samples were extracted by Soxhlet extraction and separated by using D101 macroporous adsorption resin; HPLC method was used to determine the contents of above 5 components. The determination was performed on Venusil MP C18 column with mobile phase consisted of methanol-0.1% phosphoric acid water solution (gradient elution) at the flow rate of 1.0 mL/min. The detection wavelength was 270 nm and the column temperature was 30 ℃. The sample size was 10 μL. RESULTS: The linear ranges were 1.875-187.5 μg/mL for 7-hydroxycoumarin (r=0.999 9), 1.075-107.5 μg/mL for 6,7-dimethoxycoumarin (r=0.999 9), 1.261-126.1 μg/mL for 5,7-dimethoxycoumarin (r=0.999 9), 0.875-87.5 μg/mL for imperatorin (r=0.999 9), 2.033-203.3 μg/mL for bergaptene (r=0.999 8), respectively. RSDs of precision,stability (24 h), reproducibility and durability tests were lower than 2.0%. Average recoveries were 95.18%-98.44% (RSD=1.27%,n=6), 95.35%-98.14% (RSD=1.16%,n=6), 95.21%-97.32% (RSD=0.83%,n=6), 95.43%-97.14% (RSD=0.76%,n=6), 95.12%-98.75% (RSD=1.35%, n=6), respectively. The average contents of the above five components in 3 batches of shugan hewei pills were 0.424, 0.239, 0.305, 0.180, 0.459 mg/g (n=2).CONCLUSIONS: A method for simultaneous determination of five components in Shugan hewei pills was established.
KEYWORDS Shugan hewei pills; HPLC; Content determination; 7-hydroxycoumarin; 6,7-dimethoxycoumarin; 5,7-dimethoxycoumarin; Imperatorin; Bergaptene
舒肝和胃丸由佛手、白芍、醋香附、陈皮、木香等13味中药组成,具有舒肝解郁、和胃止痛的功效[1],临床用于治疗肝胃不和、两胁胀满、胃脘疼痛、食欲不振、呃逆呕吐及大便失调等症[2]。该制剂的质量标准收载于2015年版《中国药典》(一部),以芍药苷作为含量测定指标[1]。然而,在舒肝和胃丸中,佛手的用量最大,达150 g,且为该方君药,具有疏肝理气、和胃止痛、燥湿化痰的作用[3-5]。可见,现行标准仅以芍药苷作为舒肝和胃丸含量测定指标并不能有效控制组方中君药佛手的质量,更不能有效控制该制剂的整体质量。经查阅相关的文献资料发现,现有研究多以单一成分的含量作为舒肝和胃丸的质量控制指标[6-8];此外,单婷婷等[9]对舒肝和胃丸中挥发性成分进行了研究,也仅限于该类成分的指纹图谱研究。鉴于此,本文以舒肝和胃丸中君药佛手作为研究对象,拟建立同时测定该方中佛手活性成分7-羟基香豆素、6,7-二甲氧基香豆素、5,7-二甲氧基香豆素、欧前胡素、佛手柑内酯含量的高效液相色谱法(HPLC),旨在为有效控制舒肝和胃丸的质量提供方法支持。
1 材料
1.1 仪器
LC-20A型HPLC仪,配有二极管阵列检测器、自动进样器、柱温箱(日本Shimadzu公司);1200型HPLC仪(美国Agilent公司);Meteler XP205型电子分析天平(瑞士Mettler Toledo公司,精度:0.01 mg);KQ-600DE型超声波清洗器(昆山市超声仪器有限公司);A10型超纯水机[密理博(中国)有限公司]。
1.2 药品与试剂
7-羟基香豆素对照品(批号:111739-200501,供含量测定用)、6,7-二甲氧基香豆素对照品(批号:111740- 200702,供含量测定用)、欧前胡素对照品(批号:110826-201918,纯度:99.0%)、佛手柑內酯对照品(批号:520036-201401,纯度:99.2%)均购自中国食品药品检定研究院;5,7-二甲氧基香豆素对照品(北京北纳创联生物技术研究院,批号:A63874,纯度:98.0%);佛手(批号:190901)、白芍(批号:191212)、醋香附(批号:2001015)、陈皮(批号:200304)、木香(批号:190711)、郁金(批号:191203)、炒白术(批号:190808)、柴胡(批号:20100201)、广藿香(批号:20191204)、炙甘草(批号:190811)、莱菔子(批号:20191113)、焦槟榔(批号:20190902)、乌药(批号:200202)等中药饮片均购自药店,经山东省立第三医院李俊峰副主任中药师鉴定均为真品;舒肝和胃丸(北京同仁堂科技发展股份有限公司制药厂,批号:18032500、19033869、19013386,规格:水蜜丸每100丸重20 g);D101型大孔吸附树脂(粒径:0.25~0.84 mm,天津南大树脂科技有限公司);甲醇为色谱纯,磷酸为优级纯,其余试剂均为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:Venusil MP C18(250 mm×4.6 mm,5 μm);流动相:甲醇(A)-0.1%磷酸水溶液(B),梯度洗脱(0~9 min,20%A;9~17 min,20%A→50%A;17~30 min,50%A→55%A;30~60 min,55%A→100%A);流速:1.0 mL/min;检测波长:270 nm;柱温:30 ℃;进样量:10 μL。
2.2 溶液制备
2.2.1 供试品溶液 取舒肝和胃丸适量,研碎,精密称取粉末约2.0 g,置于250 mL圆底烧瓶中,加入甲醇100 mL,采用索氏提取法提取1 h,提取液蒸干,残渣加水10 mL使溶解,通过D101型大孔吸附树脂色谱柱(内径1.5 cm,柱高10 cm),依次用水50 mL、30%甲醇50 mL、甲醇50 mL洗脱,收集甲醇洗脱液,旋转蒸发至近干,用混合溶剂[甲醇-0.1%磷酸水溶液(20 ∶ 80,V/V),下同]转移并定容至10 mL量瓶中,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.2.2 对照品溶液 精密称取7-羟基香豆素对照品37.50 mg、6,7-二甲氧基香豆素对照品21.50 mg、5,7-二甲氧基香豆素对照品25.22 mg、欧前胡素对照品17.50 mg、佛手柑内酯对照品40.66 mg,分别置于20 mL量瓶中,用甲醇溶解并稀释至刻度,摇匀,作为各单一对照品贮备液。分别精密量取上述单一对照品贮备液各1 mL,置于同一20 mL量瓶中,用混合溶剂稀释至刻度,摇匀,经0.45 μm微孔滤膜滤过,取续滤液,即得上述成分质量浓度分别为93.75、53.75、63.05、43.75、101.65 μg/mL的混合对照品溶液。
2.2.3 阴性样品溶液 按照舒肝和胃丸处方配比,称取除佛手外的12味中药饮片,按照“2.2.1”项下方法制备不含佛手的阴性样品溶液。
2.3 专属性试验
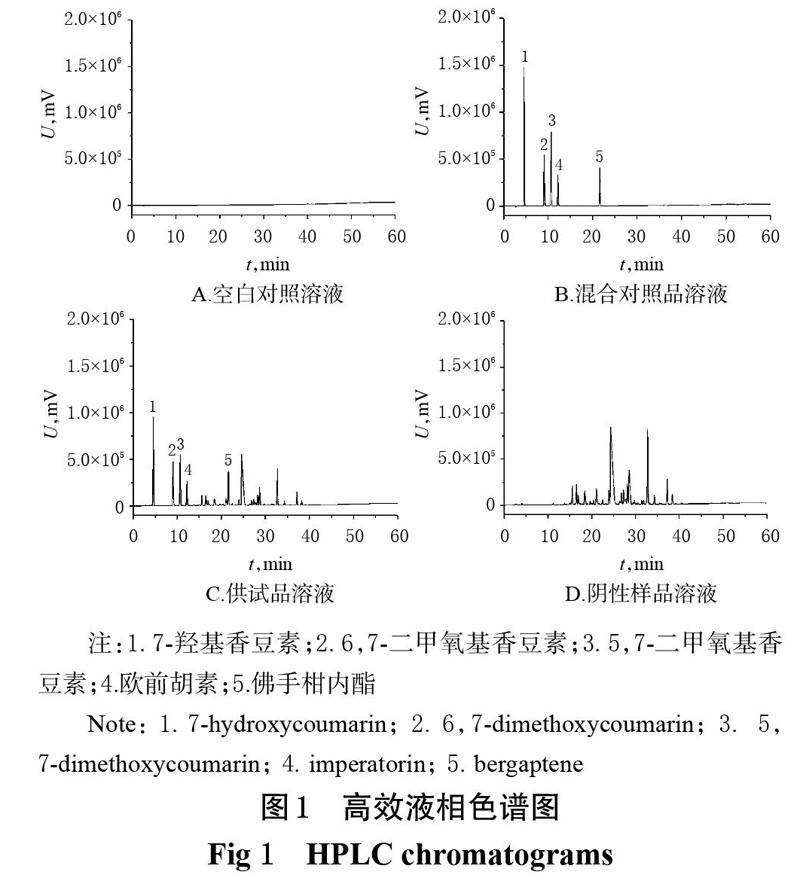
分别取空白对照溶液(混合溶剂)、混合对照品溶液、供试品溶液(批号:18032500)和阴性样品溶液,按“2.1”项下色谱条件进样测定,记录色谱图。结果,7-羟基香豆素、6,7-二甲氧基香豆素、5,7-二甲氧基香豆素、欧前胡素、佛手柑内酯的色谱峰峰形对称,其色谱峰与相邻色谱峰的分离度均不小于1.6,空白对照与阴性样品溶液对5种成分的测定均无干扰,详见图1。
2.4 标准曲线绘制
取“2.2.2”项下单一对照品贮备液0.1、0.5、1.0、5.0、10.0 mL,分别置于100 mL量瓶中,用混合溶剂稀释至刻度,摇匀,制成相应质量浓度的系列对照品溶液,按“2.1”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x,μg/mL)为横坐标、峰面积(y)为纵坐标进行线性回归,得回归方程与线性范围,详见表1。
2.5 精密度试验
精密量取“2.2.2”项下混合对照品溶液,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,7-羟基香豆素、6,7-二甲氧基香豆素、5,7-二甲氧基香豆素、欧前胡素和佛手柑内酯等5种成分峰面积的RSD分别为0.93%、1.17%、1.04%、0.88%、0.75%(n=6),表明仪器精密度良好。
2.6 稳定性试验
取“2.2.1”项下供试品溶液(批号:18032500)适量,分别在室温下放置0、4、8、12、24 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,7-羟基香豆素、6,7-二甲氧基香豆素、5,7-二甲氧基香豆素、欧前胡素和佛手柑内酯等5种成分峰面积的RSD分别为0.77%、1.24%、0.62%、1.43%、1.05%(n=5),表明供试品溶液在室温下放置24 h内稳定性良好。
2.7 重复性试验
取同一批舒肝和胃丸(批号:18032500)适量,共6份,按“2.2.1”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并按标准曲线法计算含量。结果,7-羟基香豆素、6,7-二甲氧基香豆素、5,7-二甲氧基香豆素、欧前胡素和佛手柑内酯等5种成分含量的RSD分别为1.42%、1.31%、1.27%、1.12%、1.05%(n=6),表明方法重复性良好。
2.8 加样回收率试验
精密称取已知含量的舒肝和胃丸(批号:18032500)1.0 g,共6份,置于圆底烧瓶中,分别精密加入5种待测成分单一对照品贮备液240 μL,按“2.2.1”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。
2.9 耐用性试验
取同一批舒肝和胃丸(批号:18032500)适量,共3份,按“2.2.1”项下方法制备供试品溶液,在“2.1”项色谱条件下,分别以不同仪器(Agilent 1200型和Shimadzu LC20A型HPLC仪)、色谱柱[Capcell pak C18(250 mm×4.6 mm,5 μm)和Venusil MP C18(250 mm×4.6 mm,5 μm)]、检测波长(268、270、272 nm)、柱温(25、30、40℃)和流速(0.95、1.00、1.05 mL/min)进样测定,记录峰面积并按标准曲线法计算含量。结果,改变上述色谱条件后,5种成分的色谱峰分离度良好,含量的RSD均不大于1.5%(n=6或n=9),表明本方法的耐用性良好。
2.10 含量测定
取舒肝和胃丸3批,按“2.2.1”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,每批样品平行测定2次,记录峰面积并按标准曲线法计算含量。结果,3批舒肝和胃丸中,7-羟基香豆素、6,7-二甲氧基香豆素、5,7-二甲氧基香豆素、欧前胡素、佛手柑内酯的平均含量分别为0.424、0.239、0.305、0.180、0.459 mg/g(n=2),详见表3。
3 讨论
3.1 待测成分的选择
2015年版《中国药典》(一部)在佛手药材的“含量测定”项下,采用橙皮苷作为指标成分[1]。但是在舒肝和胃丸中除佛手外,陈皮中也含有大量的橙皮苷,因此橙皮苷不能准确地反映佛手的质量。本文旨在考察舒肝和胃丸中君药佛手的质量,7-羟基香豆素、6,7-二甲氧基香豆素、5,7-二甲氧基香豆素、欧前胡素、佛手柑内酯等5种成分均是佛手中的香豆素类活性成分,具有抗菌、抗肿瘤、抗凝血、松弛平滑肌等作用[4]。因此,本研究选择上述5种特征性成分进行检测,以期能更加准确地评价舒肝和胃丸中君药佛手的质量。结果,3批舒肝和胃丸中这5种成分的平均含量分别为0.424、0.239、0.305、0.180、0.459 mg/g(n=2)。
3.2 色谱条件的選择
首先,本课题组前期以甲醇-水作为流动相进行洗脱,结果待测成分色谱峰严重拖尾、峰形较差,佛手柑内酯峰与相邻色谱峰的分离度很差。考虑到待测成分具有一定的弱酸性,所以在水相中加入0.1%磷酸以改善色谱峰峰形,效果较好。其次,由于待测成分化学性质差别较大,在色谱柱上具有不同的保留行为,故本研究采用梯度洗脱的方式,并对梯度洗脱程序进行优化,以确保全部待测成分均实现基线分离。最后,考虑到5种待测成分具有不同的紫外吸收特征,本课题组前期采用二极管阵列检测器,对5种待测成分的紫外吸收波长进行扫描,发现在270 nm波长处5种成分均具有较强的紫外吸收,故本研究选择270 nm作为检测波长。
3.3 提取方式的选择
本课题组前期分别考察了索氏提取法、超声提取法、加热回流提取法提取舒肝和胃丸的效果。结果,超声提取法和加热回流提取法提取效率均略低于索氏提取法,且提取过程需要消耗大量的提取溶剂;索氏提取法采用少量的提取溶剂即可以将待测成分全部转移到提取溶剂中,提取效率较高。因此,本研究采用索氏提取法进行样品提取。舒肝和胃丸由13味中药组成,所含有的成分非常复杂,尤其是水溶性糖类成分对分离效果的影响很大,并且还会严重缩短色谱柱的使用寿命。因此,为了减少其他成分对待测成分的干扰,本研究采用D101型大孔吸附树脂对待测成分进行富集[10-14],尽可能地去除其他成分,尤其是强极性的糖类成分。通过D101型大孔吸附树脂分离以后,水溶性干扰成分明显减少。
综上所述,本研究以君藥佛手为研究对象,成功建立了同时测定舒肝和胃丸中7-羟基香豆素、6,7-二甲氧基香豆素、5,7-二甲氧基香豆素、欧前胡素、佛手柑内酯等5种成分含量的HPLC法,可为舒肝和胃丸的质量控制提供方法支撑。
参考文献
[ 1 ] 国家药典委员会.中华人民共和国药典:一部[S]. 2015年版.北京:中国医药科技出版社,2015:178、1603.
[ 2 ] 陈锐.舒肝和胃丸临床应用解析[J].中国社区医师,2011,27(24):11.
[ 3 ] 赵永艳,张军银,彭腾,等.不同产地佛手的挥发油成分比较分析[J].中国药房,2020,31(4):423-428.
[ 4 ] 赵永艳,胡潮文,彭腾,等.佛手的化学成分药理作用及开发应用研究进展[J].时珍国医国药,2018,29(11):2734-2736.
[ 5 ] 严玮.佛手化学成分和药理作用研究进展[J].实用中医药杂志,2015,31(8):788-190.
[ 6 ] 黄思睿,何志权,覃亮. HPLC法测定舒肝和胃丸中橙皮苷的含量[J].今日药学,2014,24(4):237-239.
[ 7 ] 王桢旭.高效液相色谱法测定舒肝和胃丸中芍药苷含量[J].中国药业,2017,26(3):25-27.
[ 8 ] 胡丹,尹明,曹红,等.舒肝和胃丸质量标准研究[J].药学实践杂志,2019,37(6):532-536.
[ 9 ] 单婷婷,曹红,陈玉敏,等.舒肝和胃丸挥发性成分GC指纹图谱研究[J].解放军药学学报,2017,33(5):435-437.
[10] 宋基正,李凌军,孙鹏,等.丹参总酚酸双向调节酪氨酸酶机制及大孔树脂分离丹酚酸B研究[J].中南药学,2016,14(4):402-406.
[11] 杨茹,刘聪燕,许婷,等. 5种大孔吸附树脂对淫羊霍总黄酮的吸附特性考察[J].中国实验方剂学杂志,2020,26(6):113-120.
[12] 刘丹,吴叶红,李玮桓,等.大孔吸附树脂在天然产物分离纯化中的应用[J].中草药,2016,47(15):2764-2770.
[13] 刘岩,陈伟豪,亢迪,等.大孔树脂分离富集生物碱类成分研究进展[J].中草药,2020,51(6):1650-1659.
[14] 王亚芳,张忠立,左月明.延龄草甾体皂苷的大孔树脂纯化工艺研究[J].中药材,2019,42(7):1352-1355.
(收稿日期:2020-04-09 修回日期:2020-06-03)
(编辑:邹丽娟)

