铜,硫掺杂对铁氮碳氧还原催化剂性能的提升作用
王跃民,孟庆磊,王 显,葛君杰,刘长鹏,邢 巍
(1.中国科学院长春应用化学研究所,长春130022;2.中国科学技术大学应用化学与工程学院,合肥230026)
氧还原反应是燃料电池和金属空气电池等能量转换过程中重要的电化学反应[1~4].目前,在氧还原反应中广泛使用的铂基催化剂虽然性能优异,但由于价格和储量的影响,其规模化应用受到限制.因此,寻找非贵金属碳基氧还原催化剂引起了许多研究者的兴趣.近年来,氧还原非贵金属碳基催化剂的研究取得了重要进展[5~12],其中,非金属碳基催化剂的催化性能较金属氮碳催化剂(M-N-C,M 为Fe,Co,Mn 等)仍有较大差距,Fe-N-C 由于其优异的催化性能引起了研究者的广泛关注[7,13].
为了进一步提高 Fe-N-C 催化剂氧还原催化性能,研究者将其它金属元素,如钴[14]、锰[15,16]和镍[17]等,掺杂到Fe-N-C 催化剂中,通过协同作用来提高催化剂性能.Wu 等[8]采用二次热解铁钴掺杂聚苯胺体系的方法,通过铁和钴的协同作用制备了具有高活性和显著稳定性的金属氮碳催化剂.Koshikawa等[18]发现热解的Cu-N-C 催化剂具有较好的活性及稳定性,计算结果表明,铁-铜协同作用有利于提高催化剂的催化性能.除了金属掺杂外,硫、磷或氟等非金属掺杂也能够提高Fe-N-C 催化剂的氧还原性能[19~23].多种掺杂可导致电荷和电子自旋密度的重新分布,通过协同效应调变催化剂的活性,被认为是一种获得高性能催化剂的有效途径[24].
本文将铜和硫元素掺杂到Fe-N-C 催化剂中,制备了一系列非贵金属氧还原催化剂,表征了催化剂的形貌和结构,并研究了其催化性能.
1 实验部分
1.1 试剂与仪器
三聚氰胺(C3H6N6,试剂纯)和硫氰化钾(KSCN,分析纯),购于阿拉丁试剂(上海)有限公司;六水合三氯化铁(FeCl3·6H2O)和三水合硝酸铜[Cu(NO3)2·3H2O]均为分析纯,购于西陇化工股份有限公司;高氯酸(HClO4,分析纯),购于 Alfa Aesar 公司;浓硫酸(H2SO4)、浓硝酸(HNO3)和乙醇(CH3CH2OH)均为分析纯,购于北京试剂厂;超导电BLACK PEARLS 2000(BP 2000)炭黑购于美国Cabot 公司.
日本电子公司JEOL JEM-2010 透射电子显微镜(TEM,工作电压为200 kV);德国Bruker 公司D8 Advance X 射线衍射仪(CuKα射线源,λ=0.15405 nm);美国 Thermo-VG Scientific 公司 ESCALAB 250 X 射线光电子能谱仪(XPS);美国Thermo Fisher Scientific 公司电感耦合等离子体原子发射光谱仪(ICP-AES);上海辰华仪器有限公司750E Bipotentiostat 电化学工作站;美国Pine 公司旋转环盘电极装置系统.
1.2 催化剂的制备
氧化BP-2000(MOBP)由BP 2000 根据文献[25]的方法进行处理获得.向水和乙醇(体积比1 ∶1)的混合溶液中加入 0.1 g MOBP、1 g 三聚氰胺、18 mg FeCl3·6H2O、16.1 mg Cu(NO3)2·3H2O 和19.4 mg KSCN,超声搅拌8 h 后在50 ℃下旋转蒸发.得到的固体在氮气氛围下以5 ℃/min 升温速率升温至900 ℃并保持1 h,热解产物用稀硝酸洗涤搅拌8 h,以除去材料中的金属纳米颗粒,再抽滤、干燥,即得到样品FeCu-S-N-C.按照同样的合成及处理方法,当前驱体为MOBP、三聚氰胺和FeCl3·6H2O 时,得到样品 Fe-N-C;当前驱体为 MOBP、三聚氰胺、FeCl3·6H2O 和 Cu(NO3)2·3H2O 时,得到样品 FeCu-N-C;当前驱体为 MOBP、三聚氰胺、FeCl3·6H2O 和 KSCN 时,得到样品 Fe-S-N-C.
1.3 电化学性能表征
将5 mg 催化剂分散于50 μL 5%(质量分数) Nafion 溶液和950 μL 乙醇的混合溶液中,超声分散30 min 配制成催化剂墨水;用移液枪数次将催化剂墨水均匀滴于直径为5 mm 的旋转圆盘电极或直径为5.61 mm 的旋转环盘电极上,旋转晾干,其中催化剂的载量为0.5 mg/cm2.
采用传统的三电极体系,其中饱和甘汞电极(SCE)作为参比电极,碳棒作为对电极,涂覆催化剂的旋转圆盘电极或旋转环盘电极作为工作电极,电解液为0.1 mol/L 高氯酸溶液.在0.2 ~1.1 V 的电势窗口内,以10 mV/s 的扫描速率和1600 r/min 的转速,分别在饱和氮气和饱和氧气的电解液中进行线性扫描,饱和氧气条件下测得的数据扣除饱和氮气条件下测得的背景,即为所需要的氧还原线性扫描数据.旋转环盘测试中,环电极的电势设置为1.3 V(vs.RHE),环电极的过氧化氢收集系数为0.37.
利用如下公式计算氧还原反应过程中的电子转移数(n)和过氧化氢产率(Yield of H2O2,%).

式中:ID(A)为盘电极电流,IR(A)为环电极电流,N为环电极的过氧化氢收集系数.
在所有的电化学测试结果中,电势值均转换为相对于可逆氢电极(RHE)电势.从相对于饱和甘汞电极(SCE)的电势转换为相对于可逆氢电极的电势通过测量SCE 与RHE(该电极为浸入H2饱和的同一电解质溶液中的Pt 黑电极)之间的电势差来完成.所用电解质溶液为0.1 mol/L HClO4溶液,测得的电势差为0.305 V.
根据文献[26]报道的方法计算催化剂活性位点的周转率(TOF).在0.5 mol/L 醋酸盐缓冲液和-0.35~0.45 V(vs.RHE)的电势窗口内,将吸附在电极表面的亚硝酸根离子还原,通过积分亚硝酸根还原电流(扣除背景电流)计算催化剂的活性位点密度,结合催化剂在氧还原反应中的动力学电流,计算活性位点的TOF.
2 结果与讨论
2.1 催化剂的表征
通过 ICP-AES 测试,Fe-N-C,FeCu-N-C,Fe-S-N-C 和 FeCu-S-N-C 的 Fe 含量(质量分数)分别为0.581%,0.62%,0.621%和0.5816%,FeCu-N-C 和FeCu-S-N-C 的Cu 含量分别为0.15%和0.24%,金属掺杂浓度较低(表S1,见本文支持信息).通过TEM 观测了催化剂的形貌、结构.所有材料均未见金属纳米颗粒形成(图S1,见本文支持信息),与ICP 中较低的金属含量一致.由TEM 照片、高度环形暗场-扫描透射电子显微镜(HAADF-STEM)照片和相应的元素分布图(图1)可见,FeCu-S-N-C 材料中,Fe,Cu,S,N 和O 元素均匀分散在碳载体中,这有利于金属氮配位的活性位点的形成.

Fig.1 TEM images(A,B),HAADF-STEM image(C) and EDX elemental maps of C(D),Cu(E),Fe(F),N(G),O(H) and S(I) of FeCu-S-N-C
如图2(A)所示,所有的催化剂均有两个宽衍射峰(在25°和45°附近),其归属于碳材料,同时X 射线光电子能谱[图2(B~D)]中未观察到明显的Fe2p和Cu2p峰.N1s峰可分峰为吡啶氮、吡咯氮、石墨氮和氮氧化物的峰.在N1s的精细XPS 谱(图3)中,FeCu-S-N-C 催化剂的吡啶氮含量最高,其它3 种催化剂的吡啶氮含量相近.需要指出的是,铜掺杂和硫掺杂后,吡啶氮的含量都相应增加(表S1,见本文支持信息).由S2p的精细XPS 谱(图4)可见,FeCu-S-N-C 比Fe-S-N-C 具有更高的硫和—C—S—C—含量,其中—C—S—C—的含量是影响氧还原性能的重要因素[27~29].

Fig.2 XRD patterns(A),survey(B) and Fe2p(C) XPS spectra of Fe-N-C,FeCu-N-C,Fe-S-N-C,FeCu-S-N-C and Cu2p XPS spectra of FeCu-N-C and FeCu-S-N-C(D)

Fig.3 XPS spectra of N1s peaks for Fe-N-C(A),FeCu-N-C(B),Fe-S-N-C(C) and FeCu-S-N-C(D)
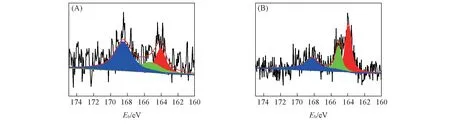
Fig.4 XPS spectra of S2p peaks for Fe-S-N-C(A) and FeCu-S-N-C(B)
2.2 铜,硫掺杂对催化剂性能的影响
首先,考察了铜掺杂对催化剂性能的影响.如表S2(见本文支持信息)所示,当铜掺杂时,与Fe-N-C相比,FeCu-N-C 的半波电势有微弱提升[图5(A)].同时,Tafel 斜率均在 50 mV/dec 左右[图5(B)],表明氧还原反应在铜掺杂后反应速率基本不变.与Fe-N-C 催化剂相比,FeCu-N-C 的过氧化氢产率从<2.5%降低到<2%,过氧化氢产率约为Fe-N-C 的80%,铜掺杂有效提高了催化剂的选择性[图5(C)].同时,在加速老化测试(ADT)中,FeCu-N-C 催化剂具有较小的半波电位衰减,说明铜掺杂对催化剂稳定性有提升作用[图6(A),(B)].
如表S2(见本文支持信息)所示,硫掺杂后,Fe-S-N-C 的半波电势相对于 Fe-N-C 正移6 mV[图5(A)],并且催化剂的选择性大幅度提高,但其过氧化氢产率仅为Fe-N-C 的28%,过氧化氢产率衰减程度远大于铜掺杂的催化剂[图5(C)].通过比较加速老化测试中催化剂的半波电势衰减发现,硫掺杂对催化剂的稳定性也未表现出明显提升作用[图6(A),(C)].

Fig.5 Electrochemical oxygen reduction performance of Fe-N-C,FeCu-N-C,Fe-S-N-C and FeCu-S-N-C in 0.1 mol/L HClO4 solution

Fig.6 LSV curves for Fe-N-C(A),FeCu-N-C(B),Fe-S-N-C(C) and FeCu-S-N-C(D)before and after 5000 and 10000 cycles ADTs
最后,研究了铜,硫双掺杂对于铁氮碳氧还原催化剂性能的影响.TOF 是基于催化剂的单位活性位点,而不是基于催化剂的整体来研究催化活性,因此能更准确地衡量催化剂的本征活性.催化剂的TOF 是通过计算在弱酸性条件下基于亚硝酸根还原的得失电子数目和氧还原反应动学电流(ik)得到的[26].FeCu-N-C,Fe-S-N-C 和 FeCu-S-N-C 的 TOF 分别是 Fe-N-C 的 1.118,1.693 和 1.791 倍(表1).显然,硫掺杂能够提高催化剂的TOF,这与文献[27]报道一致.硫掺杂通过调变Fe-Nx位点的电子结构可使两电子步骤生成的H2O2迅速反应生成水,提高Fe-Nx位点的TOF 和反应选择性;Fe-Nx位点附近的铜基位点也能将H2O2催化生成H2O,从而提高铜掺杂催化剂的TOF 并降低过氧化氢产率;FeCu-S-N-C催化剂的TOF 和H2O2产率分别是Fe-N-C 催化剂的的1.791 倍和22%,硫掺杂活化的Fe-Nx位点和邻近的铜基位点协同参与氧还原反应,从而提高了催化剂活性和选择性.对Fe-N-C 和FeCu-S-N-C 催化剂进行10000 次加速老化测试后[图6(A),(D)],其半波电势分别衰减了28 和16 mV,表明铜和硫掺杂后催化剂的稳定性获得了有效提高.
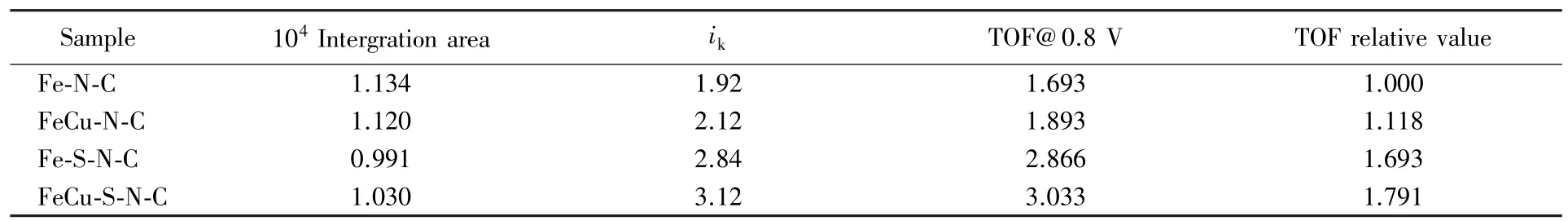
Table 1 TOF values for Fe-N-C,FeCu-N-C,Fe-S-N-C and FeCu-S-N-C
值得注意的是,影响催化剂稳定性的因素较多,过氧化氢并不是影响催化剂稳定性的唯一因素,微孔水淹、活性位点质子化、脱金属化以及碳载体氧化等都会导致催化剂稳定性的衰减[1,14].无论铜掺杂还是硫掺杂,过氧化氢产率都有一定程度降低,且硫掺杂对于过氧化氢产率的降低幅度大于铜掺杂的,因此铜掺杂和硫掺杂对催化剂稳定性的影响仍需深入研究.
3 结 论
分别以 FeCl3·6H2O、Cu(NO3)2·3H2O、KSCN、氧化 BP-2000 和三聚氰胺作为铁源、铜源、硫源、碳源和氮源,制备了一系列非贵金属氧还原催化剂.研究发现,硫掺杂比铜掺杂能更大程度地提高催化剂的TOF 值,并有效降低过氧化氢产率;铜,硫双掺杂的FeCu-S-N-C 催化剂比Fe-N-C 催化剂本身具有更高的TOF 和更低的过氧化氢产率,硫掺杂活化的Fe-Nx位点和邻近的铜基位点协同参与氧还原反应,从而提高了催化剂的活性和选择性.因此,无论是金属或非金属掺杂,通过构建级联反应或调控活性位点的电子结构,均是高性能非贵金属基氧还原催化剂的发展方向.
支持信息见http:/ /www.cjcu.jlu.edu.cn/CN/10.7503/cjcu20200155.

