基于金属卟啉2DMOFs仿酶催化的过氧化氢比色法检测
谢兴钰,赵雅香,赵莉芝,李日舜,吴迪昊,叶 卉,辛清萍,李 泓,张玉忠
(天津工业大学省部共建分离膜与膜过程国家重点实验室,材料科学与工程学院,天津 300387)
过氧化氢(H2O2)作为廉价有效的氧化剂、漂白剂及防腐剂,被广泛应用于化工、航空航天、漂白杀菌、食品和医疗等领域.但过量的过氧化氢会造成环境污染,其分解生成的活性自由基会破坏细胞器、蛋白质结构,断裂DNA分子链,使生物体受到损害,并威胁人类健康[1].因此,建立高效的过氧化氢检测方法具有重要意义.目前,常用的过氧化氢检测技术有化学滴定法[2]、比色传感法[3,4]、高效液相色谱法[5]和电化学法[6]等.其中,比色传感法具有成本低、操作简单、检测速度快且结果可视化等优点,是分析化学和环境监测领域常用的检测手段[7].比色传感法通常是在过氧化氢的氧化作用下,利用底物光学性质(吸收或发射)的变化作为检测信号,从而实现对过氧化氢的检测,因此选择高效的催化剂成为关键.
过氧化物酶是一种生物催化剂,能高效催化H2O2氧化多种底物[8,9].然而,天然酶的稳定性差、成本高且不易保存,限制了其进一步应用[10].因此,寻求成本低、稳定性好且具有天然酶特性的仿生酶成为研究热点[11].过氧化物酶的辅基是基于铁卟啉的结构,是酶催化活性中心[12],因此铁卟啉成为一类重要的仿生酶.但单独的铁卟啉易发生氧化降解或不可逆的聚集反应,使催化活性降低[13].研究[14,15]发现,金属有机骨架(MOFs),尤其是具有二维结构的MOFs纳米片,是构建铁卟啉仿生体系的理想材料之一:铁卟啉通过金属离子连接以单分子态存在,彼此互相分离,避免了聚集;与块体MOFs 材料相比,纳米片具有更大的比表面积和更多的表面活性位点,可提高其催化活性.
本文以四(4-羧苯基)铁卟啉(FeTCPP)为有机配体,铜离子为金属节点,利用溶剂热法制备了二维纳米片(Cu-FeTCPP 2DMOFs)和三维块体(Cu-FeTCPP 3DMOFs)金属有机骨架材料,通过催化氧化反应证明了其仿过氧化物酶活性;利用Cu-FeTCPP 2DMOFs 纳米片与色源底物3,3′,5,5′-四甲基联苯胺(TMB)构建了过氧化氢比色传感检测体系,在较宽的浓度范围内表现出良好的线性关系,实现了对过氧化氢的微量检测.
1 实验部分
1.1 试剂与仪器
四(4-羧苯基)铁卟啉(FeTCPP,纯度98%)、聚乙烯吡咯烷酮(PVP,Mw=40000)和三氟乙酸(纯度99%)购于北京百灵威科技有限公司;三水合硝酸铜[Cu(NO3)2·3H2O,A.R.级],3,3′,5,5′-四甲基联苯胺(TMB,纯度99%)和过氧化氢(H2O2,质量分数为30%)购于上海阿拉丁生化科技股份有限公司;N,N-二甲基甲酰胺(DMF,A.R.级)和无水乙醇(A.R.级)购于天津科密欧化学试剂有限公司;实验用水均为18.2 MΩ超纯水(Milli-Q超纯水系统,美国Thermo Fisher公司).
TU-1901型紫外-可见分光光度计(北京普析通用仪器有限责任公司);SEM500型热场发射扫描电子显微镜(SEM,德国Gemini 公司);H7650 型透射电子显微镜(TEM,日本日立公司);Nicolet 6700 型傅里叶变换红外光谱仪(美国Thermo Electron 公司)和D8 Discover 型X 射线粉末衍射仪(德国Bruker公司).
1.2 Cu-FeTCPP MOFs的制备
1.2.1 Cu-FeTCPP 2DMOFs 的合成 称取Cu(NO3)2·3H2O(0.01 mmol)和 PVP(10.0 mg)溶解于 12 mL DMF和无水乙醇的混合液(体积比3∶1)中,记为溶液I.取FeTCPP(0.005 mmol)溶于4 mL DMF和无水乙醇混合液中,记为溶液Ⅱ.将溶液Ⅱ滴加到溶液I中,随后加入20 μL 1.0 mol/L三氟乙酸.在80 ℃下反应3 h后,加入适量无水乙醇,在8000 r/min转速下离心10 min,得到Cu-FeTCPP 2DMOFs纳米片,用乙醇重复洗涤3次后,分散在乙醇中保存[16].
1.2.2 Cu-FeTCPP 3DMOFs 的合成 与上述二维纳米片的合成过程类似,将Cu(NO3)2·3H2O(0.02 mmol),FeTCPP(0.01 mmol)及20 μL 1.0 mol/L 三氟乙酸溶解于2 mL DMF 和无水乙醇的混合液(体积比3∶1)中,于80 ℃反应24 h 后,加入适量无水乙醇,在8000 r/min 转速下离心10 min,得到Cu-FeTCPP 3DMOFs,用乙醇重复洗涤3次后,分散在乙醇中保存[16].
1.2.3 Cu-FeTCPP MOFs 的结构分析 利用 SEM 和 TEM 观察了 Cu-FeTCPP 2DMOFs 和 3DMOFs 的形貌,采用 XRD 分析了 2 种 MOFs 的晶体结构;用 FTIR 分析 2 种 MOFs 的化学结构,并与 Cu(NO3)2·3H2O,PVP 及 PVP/Cu(NO3)2·3H2O 作对比,其中 PVP/Cu(NO3)2·3H2O 为 Cu(NO3)2·3H2O 和 PVP 的混合物,通过二者混合溶液冷冻干燥后制得.
1.2.4 Cu-FeTCPP MOFs 溶液浓度的计算 Cu-FeTCPP MOFs 溶液的浓度以骨架中FeTCPP 单元的摩尔浓度来表示.首先以乙醇为溶剂建立FeTCPP 标准曲线,根据朗伯-比尔定律计算出摩尔吸光系数为ε415=1.09×105L·mol-1·cm-1;然后测定合成Cu-FeTCPP MOFs 后离心所得上层清液在 415 nm 处的吸光度,计算未参与反应的FeTCPP的量,结合MOFs合成时FeTCPP的总量及所配制Cu-FeTCPP MOFs溶液的体积计算MOFs的浓度.
1.3 过氧化氢检测条件的优化
在TMB溶液中依次加入Cu-FeTCPP MOFs和H2O2溶液,显色10 min后,测试溶液的紫外-可见吸收光谱,分析Cu-FeTCPP MOFs对显色反应的催化作用,样品分别记为TMB+H2O2+2DMOFs和TMB+H2O2+3DMOFs.对照实验中,在TMB 溶液中仅加入Cu-FeTCPP 2DMOFs 或H2O2溶液,样品分别记为TMB+2DMOFs和TMB+H2O2.
根据Cu-FeTCPP MOFs 催化H2O2氧化TMB 发生显色反应来实现对H2O2的检测.对不同温度(20~45 ℃)、溶液pH(0.1 mol/L 醋酸缓冲溶液,pH=3.0~5.8)、催化剂浓度(3~47 μmol/L)和TMB 浓度(0.03~0.45 mmol/L)等实验参数进行了优化;然后在最佳条件下对比了2种MOFs及FeTCPP的催化活性,并建立H2O2的比色检测方法.
1.4 标准检测曲线的绘制
以pH=3.7的0.1 mol/L醋酸缓冲液为溶剂,配制系列浓度的H2O2的标准溶液.将H2O2标准溶液加入到含有TMB和Cu-FeTCPP 2DMOFs纳米片的溶液中,最终混合溶液中的H2O2浓度为3~1000 μmol/L,TMB浓度为0.12 mmol/L,Cu-FeTCPP 2DMOFs纳米片浓度为30 μmol/L.待混合溶液显色10 min后,测定其在650 nm处的吸光度,根据吸光度值与H2O2溶液的浓度建立标准曲线.
(3)对于过程中产生的有机硫,应优化各级催化剂组合方式,在硫磺回收单元不断叠加水解,同时通过控制工艺条件,避免生成新的有机硫,控制克劳斯尾气中的有机硫含量,最后保持加氢水解单元高效转化,可将进入灼烧炉的有机硫含量降至最低。
1.5 自来水中过氧化氢的比色传感检测
取自来水作为过氧化氢检测的实际水样,将其作为溶剂制备H2O2的加标样品,然后将加标样品加入到含有TMB 和Cu-FeTCPP 2DMOFs纳米片的醋酸缓冲溶液(pH=3.7)中,最终混合溶液中的TMB浓度为0.12 mmol/L,Cu-FeTCPP 2DMOFs纳米片浓度为30 μmol/L,H2O2浓度分别为10,20和40 μmol/L.显色10 min后,测定反应液在650 nm处的吸光度值.
2 结果与讨论
2.1 Cu-FeTCPP MOFs的制备与表征
Cu-FeTCPP MOFs 形成过程中,每个FeTCPP 配体与4 个双核轮桨式次级结构单元[Cu2(COO)4]首尾连接,形成二维的层状结构,而片层间的进一步堆叠会导致晶体各向同性增长,形成三维块体结构(Cu-FeTCPP 3DMOFs)(见Scheme 1).采用表面活性剂辅助合成二维纳米片时,表面活性剂附着在MOFs 表面,阻碍了片层间的进一步堆叠,晶体各向异性生长,最终获得超薄的纳米片层状结构(Cu-FeTCPP 2DMOFs).
通过SEM 和TEM 探究了Cu-FeTCPP MOFs 的结构与形貌,可见Cu-FeTCPP 3DMOFs 呈现块状,表现出明显的不规则片层堆积结构[图1(A)],而Cu-FeTCPP 2DMOFs 呈片层结构[图1(B)和(C)],边缘具有自发卷曲的趋势.从图1(D)所示TEM照片可以观察到CuTCPP 2DMOFs超薄的二维结构,且呈现出褶皱特点,因此其比表面积更大.由BET 测试结果可知,Cu-FeTCPP 3DMOF 的比表面积为20.127 m2/g,而2DMOF纳米片的比表面积为36.284 m2/g,这将有利于其在催化反应中提供更多的活性位点.

Fig.1 SEM image(A) of Cu-FeTCPP 3DMOFs and SEM(B) and TEM images(C, D) of Cu-FeTCPP 2DMOFs nanosheets
由图2(A)所示XRD谱图可见,Cu-FeTCPP 3DMOFs在2θ=7.6°,9°和19.2°处出现特征峰,可分别归属于MOFs的(110),(002)和(004)晶面,表明金属卟啉形成了结晶MOFs结构[16].CuTCPP 2DMOF纳米片的XRD谱图与块体的主体结构基本一致,表明了2种MOFs骨架的晶体结构相同,但2DMOFs的衍射峰偏弱,这可能是由于表面活性剂PVP的存在所致.
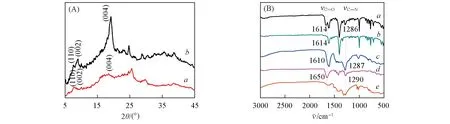
Fig.2 XRD patterns(A)and FTIR spectra(B)of different samples
图2(B)为 Cu-FeTCPP MOFs 及原料 Cu(NO3)2·3H2O 和 PVP 的 FTIR 谱图.可见,Cu-FeTCPP 2DMOFs 纳米片[图2(B)谱线a]在1286 cm-1出现了C—N 的伸缩振动峰,而在3DMOFs 的FTIR 谱线[图2(B)谱线b]上则观察不到C—N伸缩振动峰,表明PVP附着在2DMOFs纳米片表面;并且与纯PVP[图2(B)谱线d]的C—N 伸缩振动峰1290 cm-1相比,该吸收峰出现了红移,进一步证明PVP 与Cu-FeTCPP 2DMOF纳米片之间存在相互作用.由于PVP与FeTCPP均含有C=O官能团,难以辨别PVP附着在纳米片上C=O伸缩振动峰的偏移现象,所以通过PVP与Cu(NO3)2·3H2O混合物的FTIR谱图来分析PVP 与Cu2+的相互作用.由图2(B)谱线c可见,两者混合之后,PVP 的C=O 伸缩振动峰从1650 cm-1移至1610 cm-1处,表明PVP上吡咯环中的C=O基团与金属Cu2+之间发生了较强的配位作用.FTIR光谱分析结果表明,表面活性剂PVP 与金属Cu2+之间的配位作用使其在晶体生长过程中附着于MOFs表面,导致晶体各向异性增长,这也是PVP常被用作2DMOFs结构控制剂的原因.
2.2 Cu-FeTCPP MOFs的仿酶催化活性
在H2O2氧化下,无色的TMB可生成亚胺自由基阳离子的氧化产物,进而与母体化合物形成蓝色电荷转移复合物[17],其显色机理如Scheme 2所示.基于此,可以利用TMB溶液的显色程度来评价催化剂的仿酶催化活性.
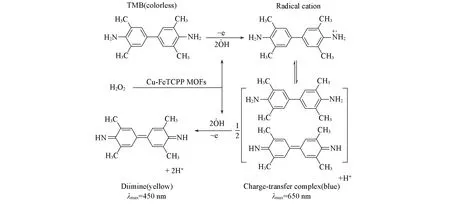
Scheme 2 Scheme of colorimetric mechanism of Cu-FeTCPP MOFs catalyzed reactions
不同体系的紫外-可见光谱及溶液颜色如图3 所示,可见,仅氧化剂H2O2或催化剂Cu-FeTCPP MOFs存在时,TMB均无显色,在500~800 nm波长范围内无明显吸收峰[图3(A)谱线b和c].而当二者同时存在时,体系在650 nm处出现强吸收峰[图3(A)谱线d和e],溶液呈蓝色[图3(B)右侧照片],表明TMB被氧化为电荷转移复合物,Cu-FeTCPP MOFs具有仿过氧化物酶活性.Cu-FeTCPP MOFs的催化特性主要归功于其骨架中铁卟啉的结构,因此本文以FeTCPP 为基元来计算仿酶催化剂的浓度,便于进行催化活性的比较.由图3(A)可见,当催化剂浓度相同时,Cu-FeTCPP 2DMOFs催化得到的氧化产物的特征吸收峰比3DMOFs的强,表明纳米片的仿酶催化能力优于三维块体,这是由于二维纳米片的比表面积更大,在催化过程中暴露的活性位点更多.
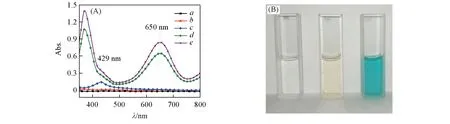
Fig.3 UV-Vis absorption spectra(A) of TMB(a), TMB+H2O2(b), TMB+2DMOFs(c), TMB+H2O2+3DMOFs(d),TMB+H2O2+2DMOFs(e)and visual color image(B)
Cu-FeTCPP MOFs的水溶液呈浅橙色[图3(B)中间照片],其吸收峰位于429 nm处,而650 nm处的吸光度非常低,当浓度为30 μmol/L时,吸光度值小于0.015[图3(A)谱线c],因此对TMB蓝色氧化产物吸光度的检测及对溶液颜色的观察均影响不大.故Cu-FeTCPP 2DMOFs可作为有效的过氧化物模拟酶,用于H2O2的比色传感检测.
2.3 检测条件的优化
仿酶的催化活性通常依赖于溶液pH值、检测温度、TMB 浓度和催化剂浓度,为了能够得到最佳的检测效果,以Cu-FeTCPP 2DMOFs为催化剂,对上述因素进行了优化.
由图4(A)可知,随着pH值的增大,反应体系在650 nm处的吸光度值先增大后减小,当pH=3.7时对应的吸光度值最大,即在此条件下显色最明显,酶促反应效率最高.温度对显色过程的影响相对较小,在25 ℃时显色吸光度值最大.
图4(B)示出了体系在650 nm 处的吸光度随TMB 浓度变化的结果,可见,随着TMB 浓度增大,体系的吸光度先呈线性增大趋势,当TMB浓度大于0.15 mmol/L后,吸光度变化趋于平缓,表明此时底物TMB过量,氧化产物浓度不再增加.Cu-FeTCPP 2DMOF催化剂浓度的优化结果如图4(C)所示,可见催化剂浓度的增加导致体系在650 nm的吸光度呈线性上升,这是由于催化剂浓度增加使催化活性位点增多,进而加快了TMB的氧化.由图4(D)中还可见,当催化剂浓度过高时,体系在650 nm处的吸收峰并未增强,且体系开始生成450 nm左右的黄色产物二亚胺(Scheme 2).为避免显色的干扰因素,催化剂浓度应不高于30 μmol/L.
2.4 Cu-FeTCPP 2DMOFs仿酶活性的动力学分析
为了进一步确定Cu-FeTCPP 2DMOFs 的仿过氧化物酶活性,对其进行了稳态酶促反应动力学分析.动力学参数由米氏方程(Michaelis Menten equation)得出[18]:

式中:v为初始反应速度(mol·L-1·s-1);vmax为最大反应速度(mol·L-1·s-1);[S]为底物(TMB或H2O2)浓度(mol/L);Km为米氏常数(mol/L).Km值为反应速度等于最大反应速度的一半时底物的浓度,是酶的特征常数,Km值越低表明酶与底物的结合亲和力越大,达到最大酶促反应速率所需的底物浓度越低,即酶的活性更高.
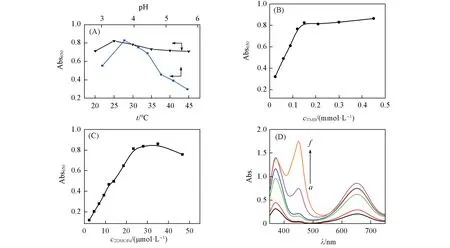
Fig.4 Absorbance of reaction solutions at 650 nm at different pH and temperatures(A), different concentrations of TMB(cH2O2=1 mmol/L, c2DMOFs=30 μmol/L)(B) and different concentrations of Cu-FeTCPP 2DMOFs(cH2O2=1 mmol/L, cTMB=0.12 mmol/L)(C), and UV-Vis absorption spectra of reaction solutions at different concentrations of Cu-FeTCPP 2DMOFs(cH2O2=1 mmol/L,cTMB=0.12 mmol/L)(D)
为便于计算对米氏方程两侧均取倒数,则得到Lineweaver Burk直线方程式[19]:
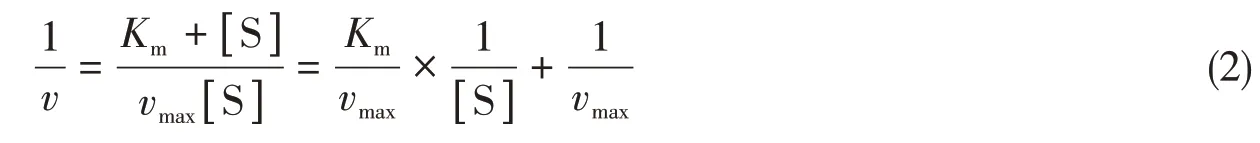
采用优化后的反应条件进行了稳态动力学分析,即在pH=3.7,Cu-FeTCPP 2DMOFs催化剂浓度为30 μmol/L 的条件下,分别改变底物TMB(0.03~0.15 mmol/L)与H2O2(0.4~1 mmol/L)浓度,记录反应5 min内体系的吸光度变化,根据吸光度曲线斜率及朗伯比尔定律计算初始反应速率,代入米氏方程由双倒数作图法(图5)计算得到Km与vmax.同时,以Cu-FeTCPP 3DMOFs和游离的FeTCPP为催化剂,在相同条件下作对照实验.表1列出了这3种催化剂以及基于MOFs的其它仿酶材料的动力学参数,对比可知,无论是以H2O2为底物还是TMB为底物,本文中Cu-FeTCPP MOFs催化得到的Km值均比游离FeTCPP的低,表明FeTCPP与铜离子形成MOFs结构后对底物的亲和力增加,仿酶催化活性增大.而具有相同骨架结构的二维纳米片较三维块体的Km值更低,进一步表明Cu-FeTCPP 2DMOFs 纳米片催化活性更高.与文献[20,21]报道的参数相比,Cu-FeTCPP 2DMOFs也表现出更低的Km值,甚至低于过氧化物酶(HRP)的Km值,因此其具有更高的催化活性,在H2O2的比色传感检测中可以代替天然酶.
2.5 过氧化氢的比色传感检测
基于Cu-FeTCPP 2DMOFs 纳米片良好的仿酶性质,构建了H2O2的比色传感检测平台.图6(A)和(B)分别示出了最优的检测条件下,在650 nm 处TMB 的吸光度-H2O2浓度的线性拟合曲线及显色结果.可见,在3~1000 μmol/L 的H2O2浓度范围内,吸收峰的强度随着H2O2浓度的增大而升高,表现出良好的线性关系,相关系数R2=0.9991.根据信噪比公式[23](S/N>3)计算出检出限(LOD)为2.08 μmol/L.与文献[24~27]报道的仿酶构建的H2O2传感检测参数(表2)相比,Cu-FeTCPP 2DMOFs/TMB比色传感检测体系展现出较高灵敏度以及更宽的线性范围,在水体过氧化氢定量检测中具有良好的应用前景.
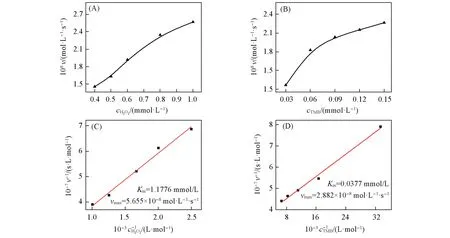
Fig.5 Steady-state kinetic analysis using Michaelis Menten model(A,B)and Lineweaver Burk model(C,D)for Cu-FeTCPP 2DMOFs by varying the concentrations of H2O2(A,C)and TMB(B,D)
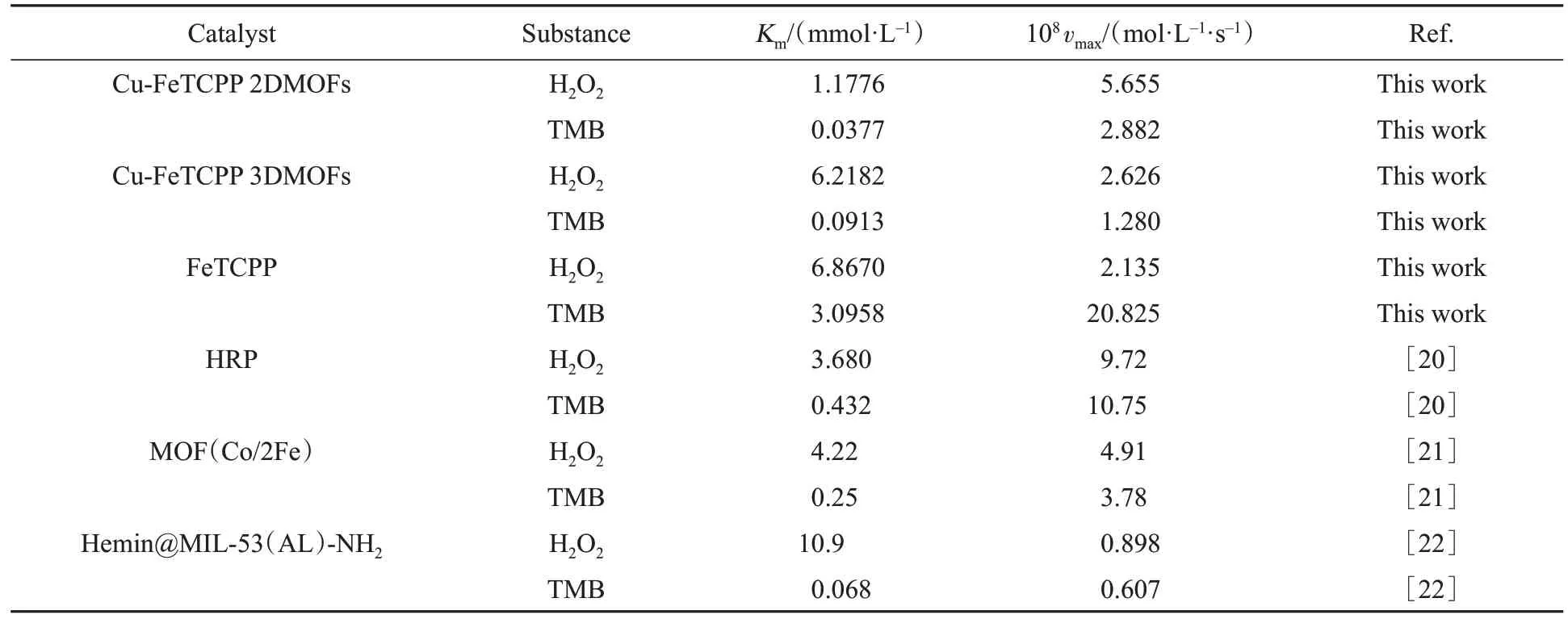
Table 1 Kinetic parameters of enzymatic reactions catalyzed by Cu-FeTCPP MOFs, FeTCPP and other MOFs-based peroxidase mimetics
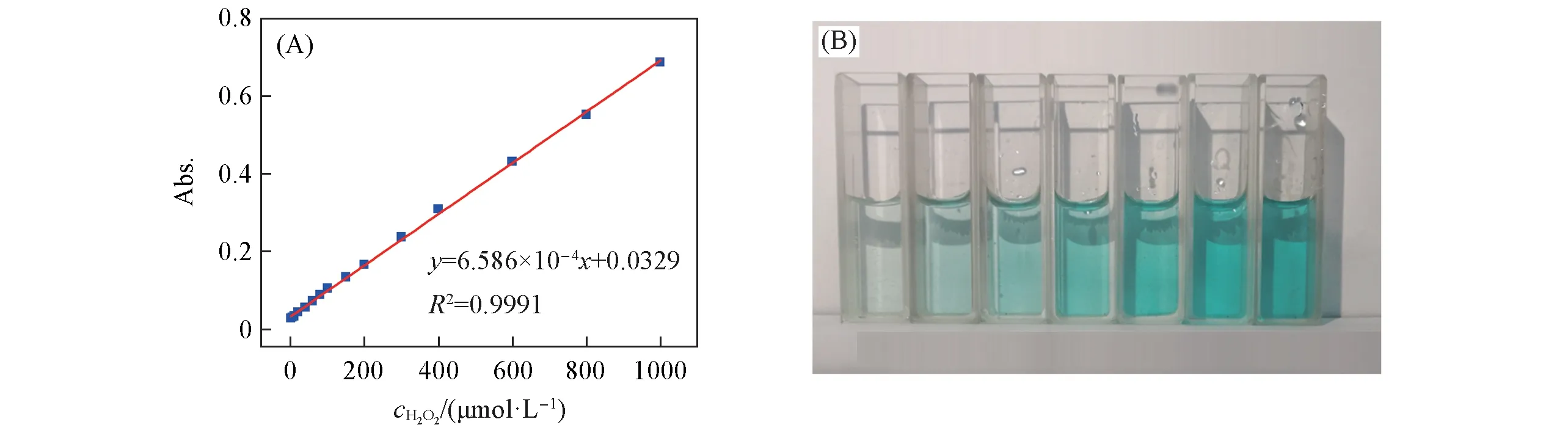
Fig.6 Linear calibration plot between the absorbance at 650 nm and the concentration of H2O2(A)and visual color response of TMB to different concentrations of H2O2(B)
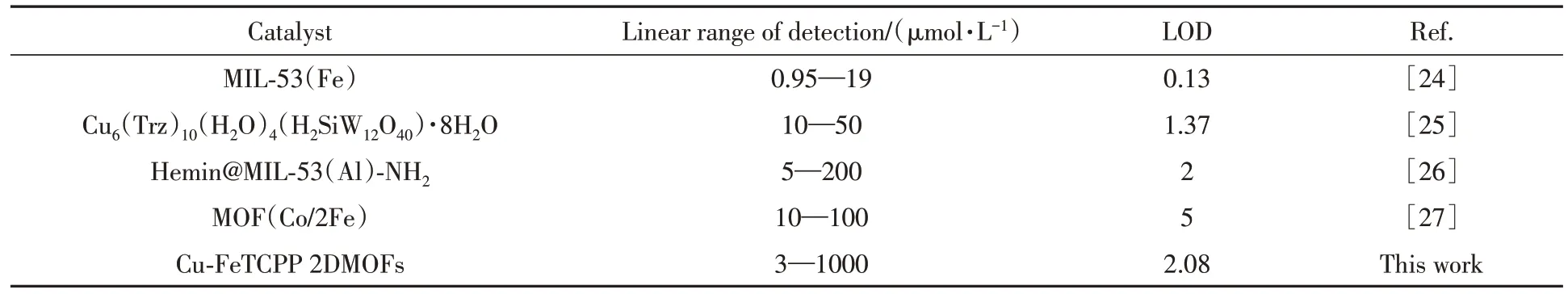
Table 2 Comparison of available methods for H2O2 colorimetric detection based onenzyme mimic of MOFs
由于过氧化氢在工业、医疗和食品等领域中的应用广泛,导致其极易通过污水排放等途径污染水环境,因此评估该比色传感体系在实际水环境中的检测性能具有重要意义.由于采集于实验室水龙头的自来水中过氧化氢的浓度太低,实验采用加标回收法进行检测.在水样中分别加入浓度为10.0,20.0,40.0 和80.0 μmol/L 的H2O2制备模拟水样,在最佳检测条件下重复测定3 次,结果如表3 所示.通过计算得出H2O2的平均回收率在97.3%~105.4%之间,相对标准偏差RSD<2.53%,表明该比色传感方法具有良好的再现性和精密度,可用于实际水样中H2O2的检测.

Table 3 Spiked recoveries of detecting H2O2 in tap water samples(n=3)
3 结 论
利用表面活性剂辅助的方法合成了Cu-FeTCPP 2DMOFs二维超薄纳米片,与三维块体3DMOFs相比,该纳米片比表面积大、活性位点可及性高,在催化H2O2氧化TMB的显色反应中,表现出更优异的仿过氧化物酶活性.基于Cu-FeTCPP 2DMOFs的仿酶催化性质,根据TMB显色产物的吸光度与H2O2浓度之间的关系建立了H2O2的比色检测方法,在H2O2浓度为3~1000 μmol/L范围内具有良好的线性关系(R2=0.9991),检出限为2.08 μmol/L,可有效检测水中H2O2含量.

