甲酸与乙酸溶解壳聚糖的溶液性质比较
陈玄墨,宁晚娥,彭泽冶,黄继伟,*,林海涛
(1.广西科技大学生物与化学工程学院,广西柳州545006;2.广西糖资源绿色加工重点试验室,广西柳州545006;3.广西高校糖资源加工重点试验室,广西柳州545006)
壳聚糖是一种来源十分广泛的生物质高分子资源,具有安全、无毒、生物相容性好、微生物可降解等特点[1-2],被广泛应用于食品、药品和精细化学品等的加工与制造[3-5],在环境污染治理、重金属提取与回收及生物医学工程等领域也被广泛的关注[6-8]。壳聚糖的加工与应用有赖于其溶解行为及适宜的溶液性质。众所周知,壳聚糖是自然界唯一的碱性多糖[9],难溶于水而易溶于酸。大量的研究关注了壳聚糖在酸溶液中的溶解行为及溶液性质特点,特别是以乙酸为溶剂的壳聚糖溶解研究较多,包括乙酸的浓度、溶解过程的温度以及壳聚糖本身的分子量等对壳聚糖溶解行为和溶液性质影响的研究[10-12]。甲酸也是一种有机酸,与乙酸一样可以溶解壳聚糖[13],且其具有更大的酸度,更高的电导率,更强的溶解能力,但其作为壳聚糖溶剂的研究与应用较少,特别是其对壳聚糖溶液性质的影响鲜有报道。因此,通过对比分析的方式,以甲酸与乙酸为壳聚糖的溶剂,在不同温度和时间的条件下,研究不同酸浓度对溶解不同质量分数的壳聚糖及其溶液性质的影响,以期进一步拓展对壳聚糖在不同酸溶液中溶解及溶液性质的认识,使壳聚糖基材料的制备有更多的溶剂选择。
1 材料与方法
1.1 试验材料
壳聚糖(脱乙酰度为80%~95%):国药集团化学试剂有限公司;甲酸(浓度为98%):西陇化工股份有限公司;乙酸(浓度为99.5%):广东光华科技股份有限公司;上述试剂均为分析纯。
DDS-307A电导率仪:上海仪电科学仪器股份有限公司;NDJ-8S数显黏度计:邦西仪器科技有限公司;PH值S-25 pH值计:上海班特仪器制造有限公司;PR124ZH/E电子天平:奥豪斯仪器有限公司;DF-101S集热式恒温加热磁力搅拌器:巩义市予华仪器有限责任公司;DK-98-电热恒温水浴锅:泰斯特仪器有限公司;HH-6六孔同温异步磁力搅拌水浴锅:常州市金坛区金城富威试验仪器厂。
1.2 试验方法
1.2.1 酸浓度的配置
分别针对甲酸和乙酸,选取1%、2%、3%、4%、5%5个酸浓度(即酸在溶液中的质量分数)开展试验研究,指定酸浓度的溶剂均采用高浓度酸加水的方式进行配置。
1.2.2 壳聚糖溶液的制备
分别称取 0.5、1、1.5、2、2.5、3 g壳聚糖加入到指定酸浓度的溶剂中进行溶解,配置成壳聚糖浓度为0.5%、1%、1.5%、2%、2.5%、3%的甲酸或乙酸溶液。溶解过程在恒温水浴锅中进行,持续2 h,溶解过程中由磁力搅拌转子缓慢搅拌,各溶液的搅拌速度相同,约为100 r/min。所制备的壳聚糖溶液共60份,即上述6种壳聚糖浓度,每个壳聚糖浓度10份,分2种酸,每种酸又有5个不同的酸浓度。
1.2.3 pH值、电导率和黏度的测定
分别采用pH值计、电导率仪和黏度计测量每份完全溶解后壳聚糖溶液的pH值、电导率和黏度,其中对于不同温度条件的指标测量,采用水浴锅逐步加热至指定温度,在该温度下稳定1 h后进行测量。本文研究的温度包括 30、40、50、60、70 ℃ 5个设置。对于放置时间影响的研究,壳聚糖溶液封口放置在恒温(30℃)、避光的环境处,前6 h每隔1 h测量一次,之后每隔24 h测量一次。记录并整理测量数据,通过绘制不同酸浓度与壳聚糖浓度下的pH值、电导率和黏度变化曲线图以及参数值变化,分析3种参数的变化规律。
2 结果与分析
2.1 壳聚糖浓度对其溶液性质的影响
分别以1%~5%的甲酸或乙酸为溶剂,在30℃下溶解壳聚糖,获得浓度为0.5%~3%壳聚糖溶液,并对其完全溶解后的溶液pH值、电导率和黏度进行测量,其结果见图1。
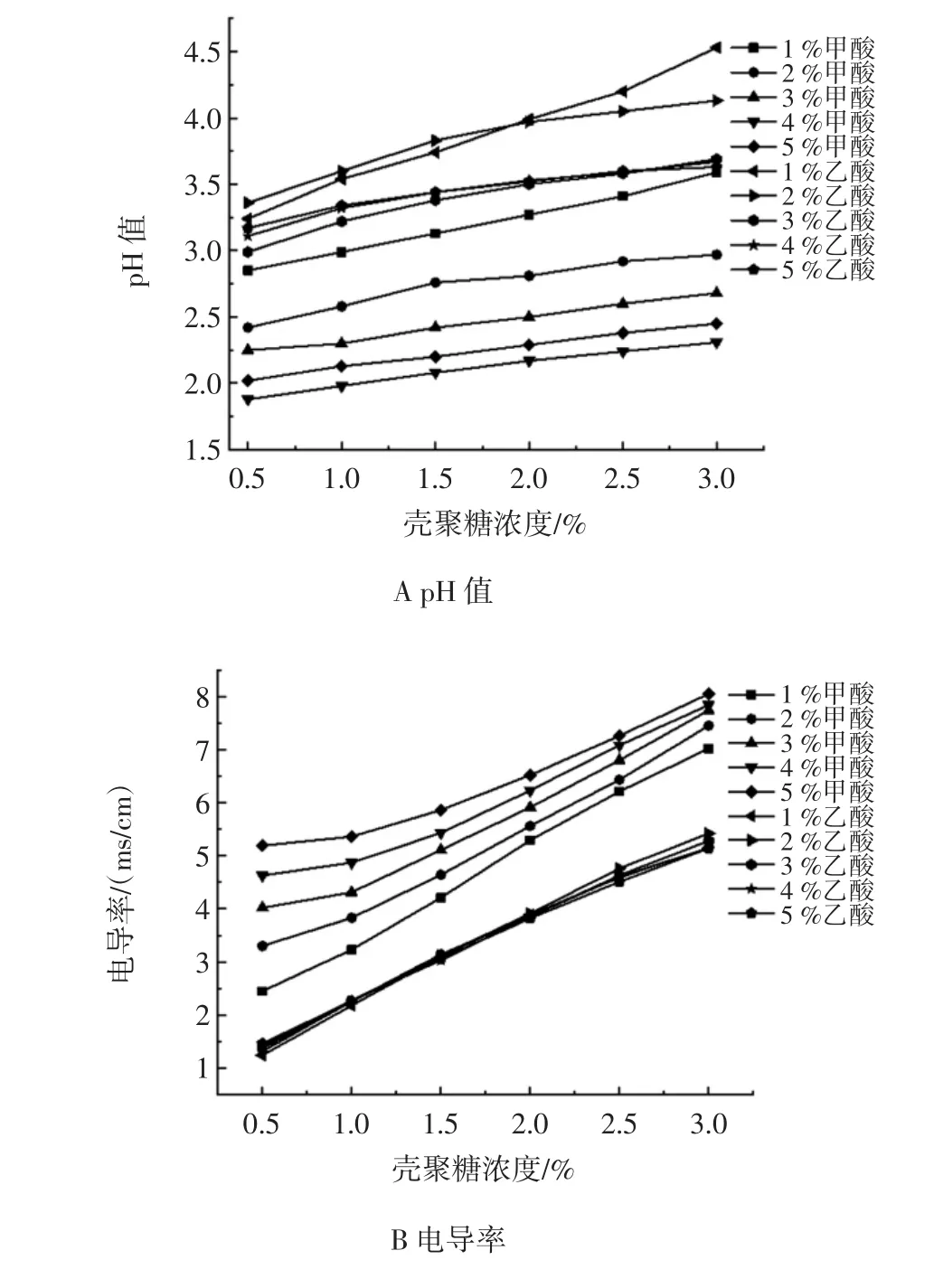
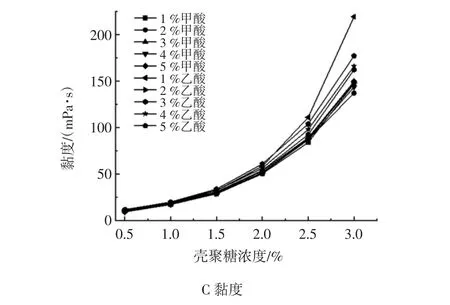
图1 壳聚糖浓度对其溶液的pH值、电导率和黏度的影响Fig.1 The effect of chitosan concentration on pH值,conductivity and viscosity
由图1A可知,在酸浓度相同的情况下,以甲酸为溶剂的壳聚糖溶液pH值更大;两种酸的壳聚糖溶液pH值随着酸浓度的增大而下降,其中甲酸的壳聚糖溶液pH值下降幅度更大,这说明甲酸pH值与其酸浓度之间的关系较乙酸敏锐。上述结果与两种酸自身的性质基本一致;而就溶液pH值与壳聚糖浓度的关系而言,对所有酸浓度的甲酸和乙酸,均呈现出pH值随壳聚糖浓度的增加而逐渐增加的趋势。分析认为:溶液的pH值取决于溶液中游离H+和OH-的浓度,而壳聚糖的溶解机理是由于壳聚糖上的氨基发生质子化,使之成为水溶性阳离子聚电解质[14],换言之,壳聚糖溶液pH值的变化可以表示出溶液中游离H+的量,从而间接表示壳聚糖氨基的质子化程度,即壳聚糖的溶解程度。而从图1A可以看出,由于壳聚糖的质子化,在酸浓度恒定比例的条件下,壳聚糖浓度的增加导致更高的溶液pH值,而在恒定的壳聚糖浓度比例下,酸浓度的增加则导致更低溶液pH值,这与Hamdine等[15]的试验结果是一致的。由于相同溶液环境下甲酸拥有更高的电离常数,能释放出更多的H+,因此甲酸的pH值值更低,且随着浓度的提升,溶液pH值下降更为明显,从而更有利于壳聚糖的溶解。
由图1B可知,无论是何种酸浓度的壳聚糖溶液,其电导率都随壳聚糖浓度的增加而增加。分析认为:在甲酸和乙酸溶液中,存在着解离的羧酸根离子、氢离子和未解离的羧酸分子,当壳聚糖溶解于这两种有机酸时,氨基首先结合游离的氢离子质子化,这时,由于静电作用携带运转电荷的自由离子与携带正电荷的壳聚糖链相互排斥,使得壳聚糖大分子趋于舒张。当游离的氢离子完全结合后,随着壳聚糖浓度的增加,更多的壳聚糖与未解离的羧酸分子相互作用,使羧酸分子解离,从而提高了壳聚糖溶液的电导率[15]。同时,从图1B可以看出,在壳聚糖浓度相同的条件下,以甲酸为溶剂的壳聚糖溶液电导率随酸浓度的增加而增加,而乙酸组电导率则随酸浓度增加基本保持不变。分析认为:甲酸的电离常数比乙酸大,使得在恒定的壳聚糖浓度比例下乙酸的电导率随酸浓度的变化并没有甲酸的明显。
由图1C可知,初始温下(30℃)无论是何种酸浓度的溶液,其黏度都随壳聚糖浓度的增加而增加。分析认为:随着壳聚糖浓度的提升,当溶液中的酸足以使壳聚糖溶解,而溶液中残余的酸不多时,壳聚糖分子内-HN3+基团产生的静电作用,使得大分子趋于舒张,从而得到较高的黏度值[16]。而当溶液中壳聚糖浓度恒定时,溶液黏度随着酸的浓度的增加略提升。这是由于酸浓度的增加,使得溶液中的离子强度增大,-HN3+离子周围聚集的酸负离子增多,降低了大分子内-HN3+的静电作用,从而使带电大分子趋于卷曲,降低溶液的黏度[17]。其中乙酸浓度为1%的溶液黏度突出,这可能是由于低浓度的乙酸并未使高浓度的壳聚糖完全溶解造成的[18]。
2.2 壳聚糖溶解温度对其溶液性质的影响
分别以1%~5%的甲酸或乙酸为溶剂,在试验设计的温度下溶解壳聚糖,获得浓度为0.5%~3%壳聚糖溶液,并对其完全溶解后的溶液pH值、电导率和黏度进行测量。壳聚糖溶液pH值随溶解温度的变化情况结果见图2。


图2 壳聚糖溶液pH值随溶解温度的变化情况Fig.2 The pH value curves along with dissolving temperature
由图2可知,当壳聚糖溶液中的酸浓度相同时,随着温度的升高,以乙酸为溶剂的壳聚糖溶液pH值随乙酸浓度的增加略有下降;而以甲酸为溶剂的壳聚糖溶液pH值随温度并没有明显的变化;同时,由图2(A)和(B)可以看出,在低浓度的甲酸溶液中,pH值会先下降,后保持在一定的数值范围内。而由图2(A)和(C)可知,高浓度的甲酸溶液中,pH值会先上升后下降。分析认为:温度的升高有利于壳聚糖分子的舒展[19],并促进弱酸的电离平衡向电离方向移动,从而释放出氢离子,降低溶液的pH值。而随着温度和酸浓度的进一步提升,温度对甲酸、乙酸的电离常数和壳聚糖分子的舒展程度皆存在不同程度的影响,使得pH值变化存在差异。
壳聚糖溶液电导率随溶解温度的变化情况见图3。

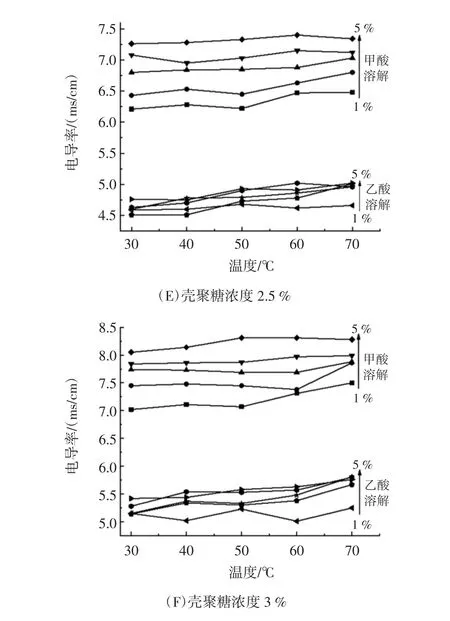
图3 壳聚糖溶液电导率随溶解温度的变化情况Fig.3 The conductivity curves along with dissolving temperature
由图3可知,在当壳聚糖浓度比例相同的条件下,不同乙酸浓度的壳聚糖溶液电导率变化相对稳定,且随温度的增加略有上升。图3(A)~(C)可以看出,当温度逐渐增加时,在低浓度壳聚糖溶液中,甲酸浓度越高,电导率越低,这是由于弱酸的电离常数随温度的升高而下降,电离的氢离子减少,且满足低浓度壳聚糖的溶解需求,使得电导率随着甲酸浓度的升高而下降[15]。而图 3(D)~(F)可知,随着温度的增加,以甲酸为溶剂的壳聚糖溶液电导率随着甲酸浓度的下降略有增加。可以看出,此时溶液的电导率仍取决于壳聚糖的浓度,壳聚糖分子的舒展与有机酸的电离平衡移动导致电导率逐渐上升。通过上述分析可以得知,温度对两种酸为溶剂的壳聚糖溶液可能起到了相似的作用。
壳聚糖溶液黏度随溶解温度的变化情况见图4。


图4 壳聚糖溶液黏度随溶解温度的变化情况Fig.4 The viscosity curves along with dissolving temperature
由图4可知,在酸浓度相同的条件下,两种酸的壳聚糖溶液黏度变化趋势是一致的,都随着温度升高而降低。这是由于温度升高,壳聚糖分子的运动加剧,分子间相互作用减弱,分子流动阻力降低,因而黏度下降[20]。从图 4(B)~(E)可以看出,当酸浓度为 1%时,初始温度下(30℃),以乙酸为溶剂的壳聚糖溶液黏度更高,且随着壳聚糖浓度的提升,两者的黏度差距逐渐增大。当温度逐渐增加时,二者的黏度呈现下降趋势且差距逐渐减小,当温度大于50℃后,黏度差异不明显,证明温度对两种酸为溶剂的壳聚糖溶液具有相同的作用效果,使黏度随着温度的升高而降低。值得注意的是,在图4(A)中,初始温度下,以乙酸为溶剂的高浓度壳聚糖溶液(>3%)相较与甲酸组其黏度尤为突出,这也证实了在乙酸浓度为1%的壳聚糖溶液中,低浓度的乙酸并未使高浓度的壳聚糖完全溶解的事实。
2.3 壳聚糖溶液放置时间对黏度的影响
为进一步表征壳聚糖溶液的稳定性,分别以1%~5%的甲酸或乙酸为溶剂溶解壳聚糖,获得浓度为0.5%~3%壳聚糖溶液。按照试验预定的间隔时间对溶液的黏度进行测量,其结果见图5,图中每条曲线代表一种溶液的黏度随时间变化的情况。
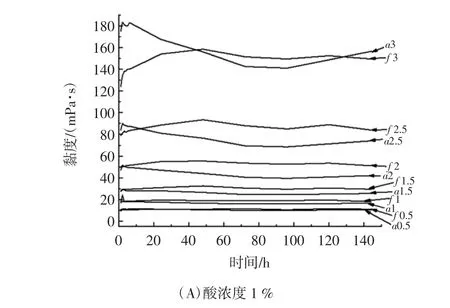

图5 壳聚糖溶液黏度随放置时间的变化Fig.5 The viscosity curves along with preserve time
由图5可知,不同酸浓度的壳聚糖溶液黏度随着存放时间的增加具有相似的变化。在起初的6 h内,壳聚糖溶液黏度有所上升,这是由于溶液温度和溶液状态未稳定引起的变化。在之后的6 d黏度检测中,壳聚糖溶液黏度均有所下降,随着时间的延长,最终趋于平缓。分析认为:壳聚糖分子中缩醛结构的存在,在酸性溶液中会缓慢降解,分子量降低,溶液的黏度随之降低[13,20],直至保持在相对稳定的状态。进一步地,图5(B)~(E)可知,当酸的浓度大于1%时,以甲酸为溶剂的壳聚糖溶液黏度比乙酸大,且随着时间的延长,下降幅度较小,且这种黏度上的差距随壳聚糖浓度的增加而增加。分析认为:随着壳聚糖分子在两种酸溶液中的降解反应,甲酸和乙酸进一步电离以维持电离平衡,但过多的酸根离子会屏蔽聚电解质分子间的静电斥力,因而造成分子链收缩,链与链之间的缠结减弱,最终使得壳聚糖在乙酸中的黏度低于甲酸[12],随着酸浓度的增加,相同浓度下的乙酸溶液电离出更多的酸根离子,使得两种壳聚糖溶液的黏度差距逐渐增大。
3 结论
通过改变甲酸与乙酸在壳聚糖溶液中的浓度,对不同质量分数、溶解温度和存放时间条件下壳聚糖溶液的pH值、电导率和黏度进行对比分析,结果表明:以甲酸为溶剂的壳聚糖溶液体系中含有更多的H+,提高了壳聚糖氨基的质子化速度,从而加快了壳聚糖的溶解。溶解温度的升高有利于壳聚糖分子的舒展和有机酸的电离,从而使壳聚糖溶液的黏度下降,而当溶解温度大于50℃时,壳聚糖浓度下降速率相同。在存放时间方面,当溶液中酸浓度大于1%时,以甲酸为溶剂的壳聚糖溶液具有更高的黏度,且保持在相对稳定的范围内,而以乙酸为溶剂的壳聚糖溶液黏度则随存放时间的增加有所下降,且随着壳聚糖浓度的增加,甲酸组的溶液黏度较乙酸组有更为明显的提升。综上所述,通过分析、比较两种酸为溶剂的壳聚糖溶液性质,甲酸更适合用于壳聚糖溶液制备。

