静态顶空气相色谱法测定脱细胞基质类产品中有机溶剂残留量
1 深圳兰度生物材料有限公司 (广东 深圳 518107)
2 广东省医用高分子植入材料工程技术研究中心 (广东 深圳 518107)
内容提要:开发了一种快速准确检测脱细胞基质类产品中有机溶剂残留的顶空气相色方法,即先将脱细胞基质类待测样品在密闭的顶空瓶中用1mol/L硫酸在75℃下完成酸解,然后再用静态顶空气相色谱法检测其中的有机溶剂残留量,并对该检测方法进行系统的方法学验证。结果表明,正己烷与丙酮分离度良好,正己烷和丙酮分别在0.5~100μg/5mL与5.0~1000μg/5mL浓度范围内呈良好的线性关系,线性相关系数(R2)分别为0.9997和0.9995,定量限分别为0.5μg/5mL与4.0μg/5mL,回收率为93.9%~102.01%,相对标准偏差(RSD)为1.55%~2.89%。该方法灵敏度高,重现性好,适用于脱细胞基质类医疗器械产品中有机溶剂残留的检测分析。
近年来,由于脱细胞基质类产品独特的生物相容性与生物活性,越来越多的脱细胞基质类产品被广泛应用于临床各个科室如皮肤或烧伤科、口腔科、神经外科、疝外科、整形美容科等[1]。在脱细胞产品制备过程中会使用到酮类如丙酮或烷烃类如正己烷等有机溶剂[2]。目前为止,国内外还没有关于脱细胞基质类产品中有机溶剂残留量的检测方法或标准,也鲜有相关的文献报道。本研究以一定浓度的硫酸作为介质,将脱细胞基质类产品完全酸解后采用顶空气相色谱法检测该产品中的有机溶剂残留量,该方法准确、灵敏度高、重现性好,能够为该类产品中有机溶剂残留量检测提供参考依据。
1.材料与方法
1.1 仪器与试剂
Agilent 7890B气相色谱仪配FID检测器、Agilent7697A顶空进样器(美国Agilent公司),SGH-3000高纯氢发生器配SGK-2LB低噪音空气泵(北京东方精华苑科技有限公司)。
正己烷标准品(GC级,阿拉丁),丙酮标准品(GCS,沃凯),硫酸(AR,国药),N,N-二甲基甲酰胺(DMF,GC级,阿拉丁),实验用水为Milli-Q超纯水系统(美国Millipore公司)制备的超纯水。脱细胞基质待测样品由深圳兰度生物材料有限公司提供(包括有机溶剂处理与未用有机溶剂处理两种样品)。
1.2 方法
1.2.1 标准溶液配制
混合标准储备溶液:分别准确称取适量的正己烷与丙酮标准品与50mL容量瓶中,用DMF定容至刻度,配制成正己烷质量浓度为1000mg/mL,丙酮质量浓度为10000mg/mL的混合标准液,于4℃冰箱储存。
混合标准工作液:将混合标准储备液用DMF分别稀释2倍、10倍、100倍,配制成三种不用浓度的混合标准中间液。然后取适量混合标准中间液加入到含5mL 1mol/L硫酸溶液的20mL顶空瓶中,密封,制备成不同浓度的混合标准工作液。
1.2.2 样品前处理
称取适量脱细胞基质待测样品,剪碎后加入到20mL顶空瓶中,加入5mL 1mol/L硫酸溶液,密封,置于75℃烘箱中至样品完全酸解后,冷却至室温,待测。
1.2.3 加样回收率样品的制备
称取适量未用有机溶剂处理的脱细胞基质待测样品,剪碎后加入到100mL蓝盖瓶中,并按照1.3中比例加入适量1mol/L硫酸溶液,置于75℃烘箱中至样品完全酸解后,冷却至室温,作为加样回收率样品的空白基底,取5mL空白基底溶液加入到20mL顶空瓶中,并加入适量混合标准中间液,密封,配制成待测的加样回收率样品。
1.3 顶空-气相色谱条件
顶空条件:顶空平衡温度80℃,定量环温度100℃,传输线温度105℃,进样时间0.5min,定量环1mL。
气相色谱条件:色谱柱HP-5毛细管柱(30m×0.32mm×0.25μm),进样口温度250℃,FID检测器温度260℃,柱温40℃保持6min,载气N2,柱流量2mL/min,氢气流量30mL/mL,空气流量400mL/min,分流比20:1。
2.结果与讨论
2.1 酸解介质的选择
正己烷不溶于水,在15.5℃的水中的饱和溶解度仅为0.014%,即140μg/mL,5mL水中最多可溶解700μg。参考药典规定,产品中正己烷的残留量应低于0.029%(290μg/g),控制待测样品取样量完全可以将顶空瓶中的正己烷总量控制在正己烷的溶解范围下,因此可以直接采用无机酸溶液进行样品酸解的前处理。考虑对色谱柱与检测器的保护,应采用高沸点的,难挥发的酸进行样品酸水解处理。本研究采用一定浓度的硫酸溶液,在硫酸浓度的选择上兼顾酸解时间与测试仪器的损伤风险。本研究尝试了高于2mol/L硫酸能在75℃温度下能短时间内(1h)将样品酸解,但是浓度高对色谱柱与仪器的损害风险越高。而低于0.75mol/L硫酸需要较长时间(4h以上)才能将样品酸解,在较高温度下(75℃)时间长了顶空瓶的气密性可能会受到影响。综合试验后采用1mol/L硫酸溶在75℃下进行样品酸解处理,一般情况下样品可以在1h完全酸解。
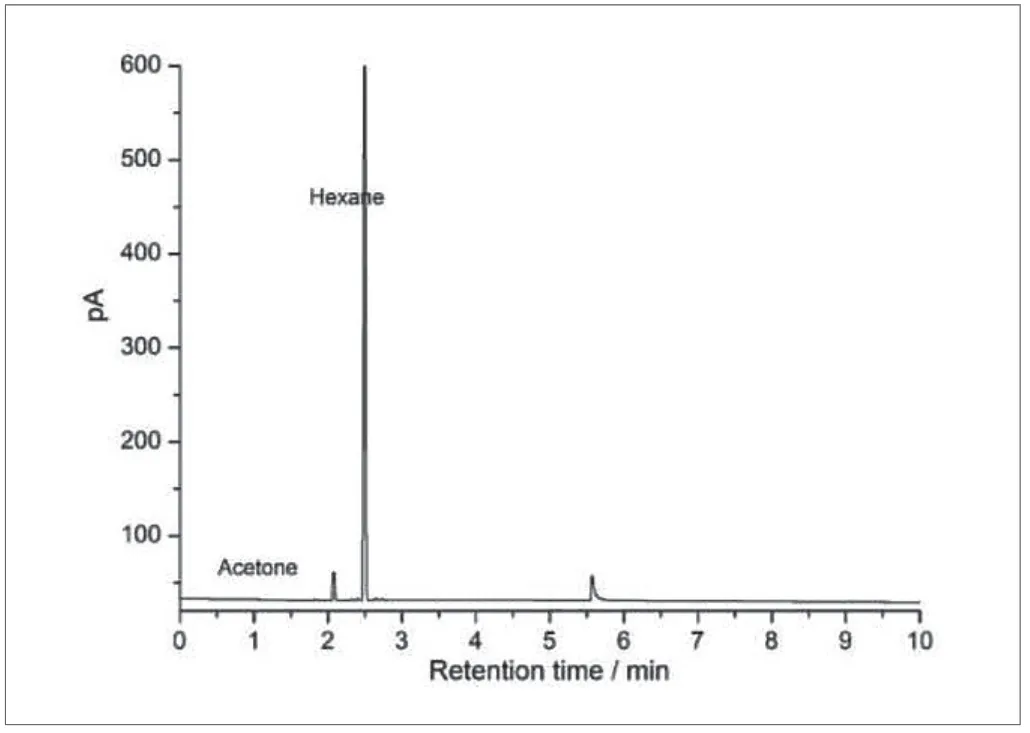
图1.混合标准溶液的GC色谱图
2.2 色谱柱的选择
根据《中国药典》2015版0861溶剂残留测定法附表2可知正己烷与丙酮能够在非极性中分析开,因此本研究采用通用的HP-5毛细管色谱柱对两种溶剂的混合标准溶液进行检测,检测结果见图1,在本实验条件下,丙酮保留时间为1.732min,正己烷保留时间为2.081min,丙酮与正己烷的峰形尖锐且对称,二者分离度良好,互不干扰,均具有良好的专属性。
2.3 定量限于检测限
根据药典中规定,一般以信噪比大于3:1时对应的进样浓度或进样量为检测限,以信噪比大于10:1时对应的进样浓度或进样量为定量限。本研究分别测试低浓度的丙酮与正己烷的峰面积,利用安捷伦气相色谱工作站OpenLAB CDS数据处理软件计算出不同浓度的丙酮与正己烷对应的信噪比,结果显示,丙酮浓度为2.0μg/5mL时对应信噪比约为9.0,在此浓度下相对标准偏差RSD为2.76%,符合精密度要求,确定丙酮的检测限为2.0μg/5mL。丙酮浓度为4.0μg/5mL时对应信噪比约为18.3,在此浓度下相对标准偏差RSD为5.69%,符合精密度要求,确定丙酮的定量限为4.0μg/5mL。正己烷浓度为0.2μg/5mL时对应信噪比约为13,对应峰高小于0.5,能够定性检测出正己烷,且此浓度下相对标准偏差RSD为4.91%,符合精密度要求,但正己烷浓度再降低,正己烷的峰高与基线难分辨,因此确定正己烷的检测限为0.2μg/5mL。正己烷浓度为0.5μg/5mL时对应信噪比约为30,在此浓度下相对标准偏差RSD为2.9%,符合精密度要求,确定正己烷的定量限为0.5μg/5mL。

表1.正己烷与丙酮的线性范围、线性方程与相关系数

表2.正己烷与丙酮的回收率与精密度(n=5)

表3.正己烷与丙酮的线性范围、线性方程与相关系数(%)
2.4 线性范围
根据正己烷与丙酮的定量限,并结合样品中正己烷与丙酮的残留限量要求,设定合适的标准工作曲线测试范围,并测试各自范围内浓度与峰面积的线性关系。分别以良好总有机溶剂的峰面积(y)为纵坐标,对应质量浓度(x,µg/5mL)为横坐标绘制标准曲线,结果如表1显示,在0.5~100μg/5mL范围内,正己烷浓度与峰面积具有良好的线性关系,线性回归方程y=39.906x-3.9191,线性相关系数R2为0.9997;在5.0~1000μg/5mL范围内,丙酮浓度与峰面积具有良好的线性关系,线性回归方程为y=0.9087x+1.7598,线性相关系数R2为0.9995。
2.5 方法回收率与精密度
采用加标回收的方法,即通过在待测样品(本实验中为未经有机溶剂处理的脱细胞基质样品)中分别添加不同水平的有机溶剂混合标准溶液,测定各自浓度下的回收率与精密度。为了检测更宽浓度范围的加样回收率与精密度,本实验设置了3个加标水平,分别为1/10限量、限量与2限量,每个加标水平做5个平行试验,计算加样回收率和精密度。表2为空白脱细胞基质样品中正己烷与丙酮的平均回收率与精密度,由表2可知,在本实验条件下,两种有机溶剂的加样回收率为93.9%~102.01%,RSD为1.55%~2.89%。不同加样浓度下的回收率与精密度均满足方法学验证要求。
2.6 方法重现性
取深圳兰度生物材料有限公司制备的可吸收胶原膜产品(批号20170601)按照本实验方法分别进行实验室检测与委托北京医疗器械检验所进行检测,检测结果如表3所示,不同实验室检测结果无显著性差异,产品中正己烷与丙酮残留量满足药典规定要求,其中北京医疗器械检验所检验报告编号为W-W-0512-2019。检测结果表明本实验方法具有良好的重现性。
3.结论
根据《中国药典》2015版规定,丙酮属于三类有机溶剂,对人体或环境的危害小,产品中残留量应控制在0.5%(5000ppm)以下,正己烷属于二类控制有机溶剂,该类有机溶剂具有神经毒性与致畸性,产品中残留量应控制在0.029%(290ppm)以下[3]。同时《中国药典》2015版第四部0861溶剂残留测定法中只规定了药品中溶剂残留测定时样品的大致前处理方法与检测方法。药品一般可通过研磨成粉末后均匀分散或溶解于水或有机溶剂介质中,因此药品样品的前处理相对容易,但是对于脱细胞基质类医疗器械产品,通常很难研磨成粉末,也很难直接溶解于常用有机溶剂介质中,常用样品前处理方法是浸提[4,5]。但是浸提一方面存在浸提时间长,拉长检测周期,另一方面存在浸提不充分而导致检测结果偏低的风险。按充分释放残留溶剂的思路,不能将待测样品均匀分散或溶解,那可以采用溶剂介质在一定条件下分解样品中使样品中的残留溶剂全部释放,然后用顶空气相色谱法检测[6,7]。
本文开发了一种快速准确检测脱细胞基质类产品中溶剂残留的顶空气相色方法,即先将脱细胞基质类待测样品在密闭的顶空瓶中用1mol/L硫酸在75℃下完成酸解,然后再用静态顶空气相色谱法检测其中的溶剂残留量。该方法操作简单、结果准确、重复性好,且灵敏度高,满足脱细胞基质类产品中溶剂残留的测试要求,可为今后脱细胞基质类医疗器械产品中有机溶剂残留检测提供参考依据。

