纳氏试剂分光光度法测定水中氨氮的探讨
唐韧锋 党翔宇 杜 永 兰 盾
(十堰市环境保护监测站,湖北 十堰442000)
氨氮(NH3-N)指水中以游离氨(NH3)或铵盐(NH4+)形式存在的氮。两者的组成比取决于水的pH 值和水温,当pH 值偏高时,游离氨的比例较高。反之,则铵盐的比例高,水温则相反[1]。
水中氨氮的来源主要为生活污水中含氮有机物的分解产物,某些工业废水,如焦化废水和合成氨废水以及农田排水[2]。此外,在无氧环境中,水中存在的亚硝酸盐亦可受亚硝化细菌的作用,还原为氨,在有氧环境中,水中氨亦可转变为亚硝酸盐,甚至继续转变为硝酸盐[3]。鱼类对水中氨氮比较敏感,当氨氮含量高时会导致鱼类死亡[4]。因此,测定水中各种形态的含氮化合物,对于评价水体被污染和“自净”状况十分重要。
目前测定水质氨氮的方法主要有纳氏试剂光度法,水杨酸分光光度法,蒸馏和滴定法和气相分子吸收光谱法等[3]。其中纳式试剂分光光度法是目前最常用的方法。其原理是碘化汞和碘化钾的碱性溶液与氨反应生成淡红棕色胶态化合物,此颜色在较宽的波长内具强烈吸收。通常测量用波长在410~425nm 范围。但是在用纳氏试剂光度法测定水中氨氮时存在一些问题。本文将针对这些问题进行一些探讨和研究。
1 试剂的影响
1.1 显色剂
纳氏试剂的配制方法通常有两种,一种是二氯化汞法由二氯化汞、碘化钾、氢氧化钾配制而成,另一种是碘化汞法由碘化汞、碘化钾、氢氧化钠配制而成。第二种配制方法较简单,但是配制出来的纳氏试剂空白值比第一种方法高出一倍。纳氏试剂必须低温避光保存,否者会导致试剂颜色加深,影响空白值的稳定性。一般常用第一种方法配置,该方法关键在于把握HgCl2的加入量,这决定了反应生成显色集团含量的多少,进而影响方法的灵敏度。但方法标准未给出HgCl2确切加入量,需要根据试剂配制过程中的现象加以判断,经验性较强,难以把握。林小琪用经验总结出HgCl2与KI 的用量比为0.44:1 时(8.8gHgCl2溶于20gKI 溶液)效果很好[5]。《国家地表水环境质量监测网监测任务作业指导书》中要求该方法曲线斜率范围在0.0060-0.0078 之间,截距范围±0.005 之间,所以HgCl2的投加量也有了相应的控制,根据实验结果HgCl2投加量在8.35-9g 之间也就是用量比在0.417-0.45 之间基本能满足作业指导书要求,半年做的近40条曲线的截距和斜率结果见表1。
由于HgCl2溶解较为缓慢,为提高配药效率,可以将配好的KI 溶液放到微波清洗器中分批次投加称量好的HgCl2固体超声溶解,以此比例配置的纳氏试剂经长期实验检验,灵敏度,斜率,截距均能达到要求。
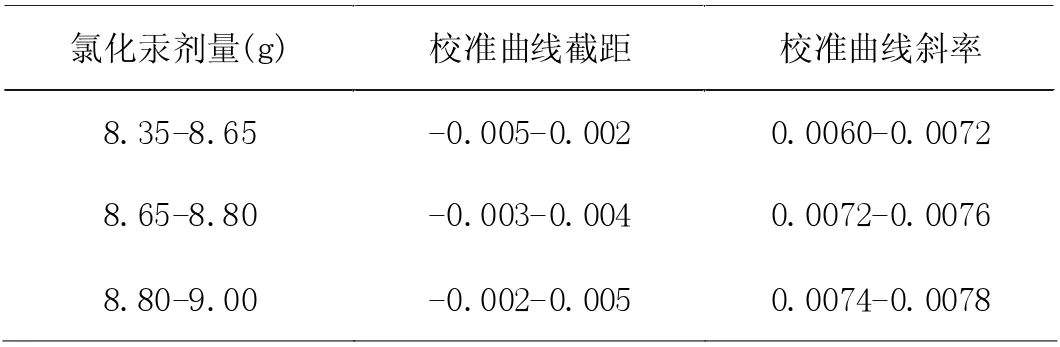
表1 氯化汞剂量对校准曲线截距、斜率的影响
1.2 掩蔽剂
纳氏试剂分光光度法使用酒石酸钾钠作为掩蔽剂。市售酒石酸钾钠通常含有氨盐,因此,在配制掩蔽剂过程中一定要加热煮沸蒸发掉超过一半的水分后冷却定容;否则掩蔽剂中的氨盐会带入样品会导致空白值偏高,或者其掩蔽效果降低使样品呈混浊进行干扰测定。部分含氨量特别高的酒石酸钾钠,直接加热沸腾空白测定依然很高,处理的方法有两种:
(1)向定容后的酒石酸钾钠中加入5mL 纳式试剂,沉淀后取上清液使用;
(2)向酒石酸钾钠中加入少量的碱,煮沸蒸发至50mL 后冷却定容至100 毫升。
由于酒石酸钾钠生产工艺的原因,不同厂家酒石酸钾钠的掩蔽效果不同,使实验过程中存在不稳定风险,肖翔群, 毛予捷,伍丽平提出,用六偏磷酸钠或乙酸钠代替酒石酸钾钠作为掩蔽剂以提高掩蔽效果[6],在实际使用过程发现六偏磷酸钠保存期较短尽量现配现用,否者会导致空白值偏高。
2 过程控制
2.1 显色温度
温度影响纳氏试剂与氨氮的反应速度,进而影响测定结果[7]。反应温度为5~10 ℃时,显色不完全,样品吸光值无显著变化;反应温度为20~25℃时,显色最完全,且吸光度值比较稳定;当温度达到30℃或更高时,溶液显色不稳定,当温度大于35℃时,溶液开始褪色,吸光度偏低。因此显色温度应控制在20~25℃。
2.2 显色时间
显色温度应控制在20~25℃时,放置10min(当采用商品化试剂时,根据显色情况调整可调显色时间)后比色。显色时间不足10min,溶液显色不完全,吸光度随显色时间的增加而增大;显色时间在10~25min,吸光度几乎无变化,显色较稳定;显色时间在25~80min,吸光度总体成增大趋势。因此显色时间应在10~25min 之间,一般选择10min 后为宜。因而,用纳氏试剂比色法测定水中氨氮时,显色时间应控制在10~25min,尽量不要超过35 min。比色过程注意控制时间,以达到分析的精密度和准确度。
2.3 显色前溶液的pH 值
使用纳氏试剂分光度法对水中的氮氨进行测定,应注重在样品显色之前要将水样的pH 调至6~8。加入纳氏试剂后溶液显色的pH 适宜范围为12(11.8)~13(13.6),pH 低于11,反应向反方向进行,不产生显色反应,实验证明,当显色溶液的pH 值不足时,溶液吸光度随着pH 值的增加而增加,当超过一定值时吸光度逐渐稳定。纳氏试剂显色原理为增加溶液的pH 值促进显色反应向生成有色物质的方向移动。但pH 高于13(13.6),溶液中产生大量NH2HgIO,溶液变浑浊无法比色。
2.4 样品稀释
对于氨氮浓度较高的水样,前处理后要对水样进行稀释,稀释倍数根据样品来源和氨氮浓度进行调整,根据标准方法HJ535-2009 氨氮曲线的最高点测定浓度值为2mg/L,高于2mg/L 的样品都要进行稀释处理。要说明的一点是氨氮显色后生成的淡红色胶状化合物较为稳定,若实验过程中稀释倍数不够造成吸光度超出曲线,可以进行事后稀释比色。事后稀释的条件是首先样品浓度值不能过高,超过曲线最高点5 倍以上建议重新取样事前稀释复测,其次事后稀释的样品应尽快测量光度值,保证实验显色时间在30 分钟内完成。经实验室20 组数据平行比对,事后稀释与事前稀释样本在无其他干扰条件下,相对误差能保证在10%的范围内。
3 不同类型样品前处理
3.1 Ca2+,Mg2+等金属离子含量较低清洁的地表水
这类地表水因为清洁,干扰比较少,可以直接调节样品pH值在6~8 之间(并非必要步骤,针对添加保护剂或pH 值不在此范围内的样品,下同)直接加药比色,絮凝沉淀和蒸馏前处理过程繁琐,也会造成氨氮偏离真实值。
3.2 Ca2+,Mg2+等金属离子含量较高的清洁的地表水
此类样品氨氮含量低,由于Ca2+、Mg2+等金属离子含量较高,无法通过稀释样品降低金属离子的干扰,酒石酸钾钠的掩蔽效果有限,容易产生酒石酸钙、酒石酸镁等沉淀从而干扰测定。这种情况下可对水样进行絮凝沉淀处理,实际操作中絮凝沉淀所使用的滤纸含有铵盐应使用大量无氨水清洗。推荐用稀盐酸浸泡的0.45μm 的醋酸乙酯纤维滤膜过滤样品[8]。日常监测工作中,有絮凝沉淀后加入酒石酸钾钠样品混浊的情况出现,这种混浊不溶物用离心无法去除,这种情况可以考虑更换掩蔽剂(如六偏磷酸钠、乙酸钠等)替代酒石酸钾钠。另一种方法是,取pH 值调至中性的水样50mL 加入配制好的酒石酸甲钠溶液1mL 摇匀,盖上玻璃塞静置30-60 分钟,静置时间以样品澄清为宜,再加入纳式试剂静置10 分钟,加入纳氏试剂后尽量不要再摇动样品保持样品静置,取上清液比色。为确保显色效果建议加入纳氏试剂后显色时间可以稍微延长,控制比色时间在30 分钟内完成。
3.3 污染源废水
由于污染源样品成分复杂,前处理过程也要根据实际情况进行选择。此类样品可以根据样品来源、表观或者加入掩蔽剂、显色剂后待测样品的表观来判断采用相应的前处理方法。色度和浊度较低的样品,调节pH 值取适量样品进行显色测定,稀释过程也可以降低或者消除色度、金属离子等干扰。色度、浊度较高的样品或加入掩蔽剂后待测样品呈浑浊或加入显色剂后待测样品的颜色异于标准曲线点试样颜色,可采用絮凝沉淀法或蒸馏法消除样品干扰。对于水质比较浑浊的样品絮凝沉淀后,可以进一步的离心处理后再加药比色,高氯废水样品(氯离子浓度>1100mg/L)用絮凝前处理无法解决其干扰问题,用蒸馏前处理法可以达到满意的效果。
有机物产生的色度较高且絮凝沉淀或稀释无法完全消除色度干扰时,需要用蒸馏前处理法进行处理,蒸馏过程若采用的硼酸吸收液,蒸馏完成后要将馏出液用1mol.L-1NaOH 约14ml 调整到pH 值10 左右,pH 值太低会有红色碘化汞析出导致数据偏低,pH 值太高导致样品混浊数据偏高,也可用pH 值大于2 的盐酸、硫酸溶液当做吸收液此时可省去调节馏出液pH值过程[9]。当样品中含有丙酮、芳香氨、醛类等易挥发的还原性干扰物质存在时,絮凝沉淀和蒸馏前处理方法都不能去除干扰。可以尝试水样稀释后直接加纳氏试剂比色,或者将水样酸化加热除去干扰后再加药进行比色[10]。
4 结论
由实验和讨论可知,纳氏试剂分光光度法测量水中氨氮应注意和解决以下3 种常见问题:
(1)选购合格试剂,正确配制掩蔽剂和显色剂并在合适的环境中保存,同时注意控制因实验用水、试剂和滤纸等试料引入的空白。
(2)控制样品pH 值、显色温度和显色时间在最佳的条件下进行试验环境温度确保实验过程在最佳条件下进行。
(3)针对实际水样根据不同情形选择合适的方法消除干扰。注意高硬度水样的前处理方法,较浑浊样品絮凝沉淀后可进一步进行离心处理,注意蒸馏前处理的吸收液pH 值的调节。

