基于生命/影像组学的精准组学放射治疗研究进展
蔡凯 黄贵华

摘要:恶性肿瘤的发病率和死亡率均较高,基因组测序为肿瘤精准医疗带来了革命性的变化。本文从国内外的研究现状出发,介绍生命组学技术、影像组学的概念和方法框架与人工智能(AI)技术引领的新技术革命。分析精准组学放射治疗的技术优势和全球的研究进展。对基因组学及或影像组学技术可获得肿瘤和个体的遗传信息和生物学特征进行综述,以期为放射治疗适应证评估、治疗方案的制定和放射剂量分配更加准确的提供参考。
关键词:生命组学;影像组学;人工智能;放射治疗
中图分类号:R730.55 文獻标识码:A DOI:10.3969/j.issn.1006-1959.2020.14.010
文章编号:1006-1959(2020)14-0027-05
Research Progress of Precise Omics Radiotherapy Based on Life/Imaging Omics
CAI Kai,HUANG Gui-hua
(Radiotherapy Center,the First Affiliated Hospital of Guangxi University of Traditional Chinese Medicine,
Nanning 530021,Guangxi,China)
Abstract:The morbidity and mortality of malignant tumors are relatively high, and genome sequencing has brought revolutionary changes to precision medical treatment of tumors. Based on the current research situation at home and abroad, this article introduces the concepts and method framework of life omics technology, imaging omics and the new technology revolution led by artificial intelligence (AI) technology. Analyze the technical advantages of precision omics radiotherapy and global research progress. The genomics and/or imaging technology can obtain the genetic information and biological characteristics of tumors and individuals, in order to provide a more accurate reference for radiotherapy indication evaluation, treatment planning and radiation dose allocation.
Key words:Life omics;Imaging omics;Artificial intelligence;Radiotherapy
肿瘤是极其复杂的系统性疾病,人类基因组测序为精准医学时代铺平了道路,使得为患者提供最佳治疗方案成为可能。人工智能(AI)放射治疗计划模型的建立和基于“Internet+医疗”的远程智能放射治疗质量控制系统正在进行中。智能医学将改变未来的医学模式,生命组学和影像组学的发展将给放射治疗带来革命性的变化,现综述如下。
1背景
1.1生命组学技术 肿瘤涉及DNA、RNA、蛋白质和代谢产物水平的多种异常,是一种复杂的系统性疾病。从中心定律衍生的组学方法有基因组学、蛋白质组学、代谢组学和转录组学[1]。基因组学的发展离不开DNA测序技术的进步。目前主要的测序技术有全基因组测序(WGS)、全外显子测序(WES)和染色体微阵列分析(CMA)。前两种主要识别基因组变化,后两种主要识别基因拷贝数变化,循环DNA(cfDNA)和循环肿瘤细胞(CTCs)是一个新的研究领域。肿瘤基因组学的应用主要包括以下4个方面:①驱动突变的识别;②与杂合性丢失相关的CNVs和拷贝数(LOH);③cfDNA来源于凋亡或坏死的肿瘤细胞,其突变代表了细胞起源的遗传背景,其水平与肿瘤分期有关;④遗传种系变异,遗传种系变异与肿瘤基因体细胞突变有关,提示特异的种系背景可能影响肿瘤的发生。高效、高通量测序技术的应用,显著提高了基因组学的分析效率,揭示了肿瘤突变基因的更多内容,为肿瘤的准确诊断和治疗奠定了基础[2]。
1.2基因检测技术 随着分子生物学的飞速发展,揭示肿瘤进展中分子特征变化的分子诊断技术已经广泛应用于遗传性疾病诊断、肿瘤突变基因检测,伴随诊断和预后评估等领域,尤其在肿瘤的诊断和治疗中起到越来越重要的作用[3],但仍存在许多挑战。多组学分析集成了不同的组学数据,复杂的大数据量对生物信息平台的分析能力提出了更高的要求;多组学技术在临床和医疗中的应用还存在很多问题,例如多组学方法提供了许多潜在的生物标记物和治疗靶点,但要探索显著提高早期发现率和总体生存率的方法还有很长的路要走。
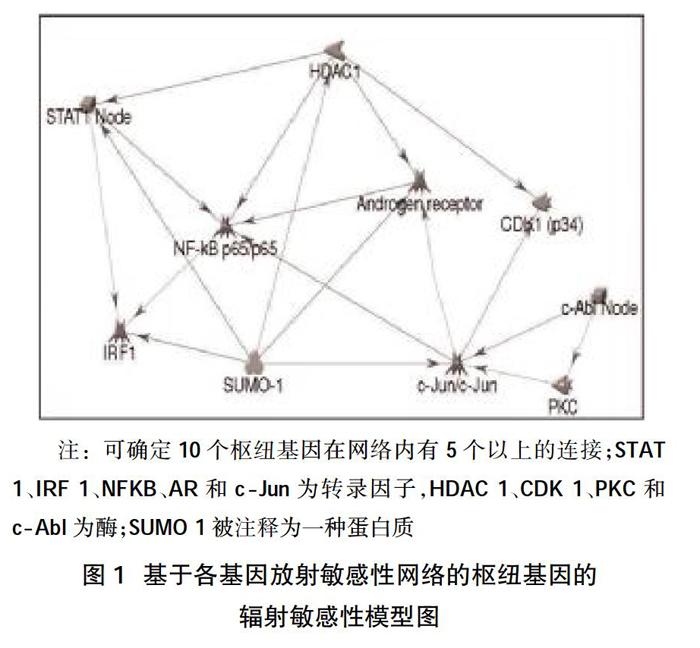
3.2肿瘤放射敏感性模型的建立 建立肿瘤放射敏感性模型是精准组学放射治疗的基础。在恶性肿瘤中发现新的生物标志物以更好地诊断和治疗该疾病是分子医学时代基本原则[18]。在放射肿瘤学临床实践中,很难完全确定各种恶性肿瘤的特异性生物标记基因;在“组学”时代,高通量数据集的产生为从不同角度识别恶性肿瘤的标记基因提供了机会,调控通路被认为类似万维网的复杂交互网络。因此,了解调控通路网络的第一步是定义其组成和组织。为了解恶性肿瘤内在放射敏感性,有学者基于生物学或临床的基础建立了一个系统的放射敏感性模型[19]。该模型正确地预测22/35细胞系的细胞放射敏感性(SF2,1rbapa48,rgs19,r5pia,P=0.002)与恶性肿瘤的放射敏感性密切相关,其过度表达提示三种肿瘤细胞系的放射敏感性更高[20];此外,过度表达也导致细胞在细胞周期的G2/M期和AKT的去磷酸化中所占的比例更高。研究小组使用类似的方法来定义路径/调控48个肿瘤细胞系的数据库中的网络大小,高连接性基因被认为是网络的最重要组成部分[21]。该研究通过检查5个以上的连接中枢,确定了10个与肿瘤细胞放射敏感性相关的基因[c-jun,HDAC1,RELA(NFKB的p65亚单位),pkcβ、sumo-1、c-abl、STAT1、AR、CDK1和IRF1],见图1。在10个基因中,HDAC1、pkcβ、NFKB、c-abl、STAT1、AR和CDK1已被开发为放射增敏剂的靶 点[22,23],这与接受化疗和/或放疗的乳腺癌患者的临床结果相关[24]。
研究表明[25],这10个基因的表達可以用于预测恶性肿瘤细胞的内在辐射敏感性。为了找到决定乳腺癌RT治疗效益的生物变量,有研究者[26]开发了一种基于检测这10基因[c-Jun, HDAC1, RELA (p65subunit of NFKB ),PKC-beta,SUMO-1,c-Abl,STAT1,AR,CDK1 和IRF1]在恶性肿瘤病灶中的表达情况来估计恶性肿瘤细胞的放射敏感性的模型。使用该模型可以预测一个与肿瘤放射抵抗成正比的放射敏感性指数(RSI)和肿瘤细胞存活率(SF2)。目前有一些能够预测辐射敏感性的系统生物学模型逐渐被开发出来[27-29]。Speers C等[30]在Moffitt的前瞻性临床试验中,验证该模型可作为两个独立(食管和直肠)癌症患者病理反应的预测因子,并认为该模型在放射肿瘤学的个性化治疗中可能起着核心作用。致力于研究建立一个量化肿瘤细胞中放射敏感度指数(RSI)的方法,并根据不同肿瘤患者的RSI确定精确的辐射剂量,推动精准组学放疗在临床恶性肿瘤治疗中的应用,将是今后的研究热点。
3.3放射肿瘤学临床试验框架 放疗剂量调整模型(GARD)为设计基因导向的放射肿瘤学临床试验提供框架。
在放疗的临床实践中,放疗的治疗效果不仅与放疗敏感性相关,还与放疗的剂量、分割次数等因素相关,为了将这些因素一起考虑进去。有研究者将广泛应用的线性平方模型(linear quadratic equation,L-Q公式)与RSI相结合,提出了基因表达校正的放疗剂量(GARD)的概念[31]。GARD是糅合了个体基因表达信息,同时将放射治疗的放疗剂量和分割次数考虑在内,与肿瘤治疗预后相关的一种模型,该研究结果发现GARD值越高,放射治疗效果越好,临床预后更好,GARD与RSI呈非线性相关[32],见图2。GARD是一种新的辐射剂量处方范式,为优化和个性化放射剂量以匹配单个肿瘤的放射敏感性提供了第一次机会。GARD被认为是放射肿瘤学中基因组驱动的个性化方法的第一次机会,也是该领域的研究重点[33,34]。
Scott JG等[31]研究发现,GARD不仅与辐射剂量有关,而且与肿瘤特异性辐射敏感性有关。根据放疗剂量的不同以及接受相同放疗剂量的不同肿瘤,GARD值的分布也不同,该研究通过五组不同来源的肿瘤数据库(包括2组乳腺癌数据以及胶质母细胞瘤、肺癌、胰腺癌数据)进行验证,发现GARD值均与临床的预后独立相关。GARD值在不同个体以及不同肿瘤类型中都不同,这也许能提示临床不同个体对治疗反应的异质性。GARD为我们提供了一种针对不同个体肿瘤放疗敏感性来调整放疗剂量的模型,为精准化放射治疗开启了新的篇章。
5总结及展望
精准医学时代下,放射治疗需要根据肿瘤生物学个体化特性来匹配相应的治疗剂量,以期提供最优的治疗方案。大数据和人工智能正在给肿瘤放射治疗带来颠覆性的变化,治疗的准确性和有效性将得到提高,智能组学放射治疗有望解决多年来放射治疗面临的问题。精准组学放射治疗在临床上的应用和推广,有利于推动该技术和其他放射治疗技术、治疗方法的全面发展。研究基于基因组学的精确放射治疗技术,使临床上更准确地制定个体化肿瘤患者的放射治疗方案,必将加快攻克肿瘤的研究进程,最终造福更多肿瘤患者。但是,精准组学放射治疗的广泛应用并非易事,最大的挑战之一就是跨多个中心的图像和相关元数据的管理以及在多中心临床试验中进行前瞻性验证,以证明新发现的成像标记物的临床有效性和实用性。对于精准放疗,在大数据人工智能时代,精准组学放射治疗仅仅是开始。
参考文献:
[1]Yoo BC,Kim KH,Woo SM,et al.Clinical multi-omics strategies for the effective cancer management[J].J Proteom,2018(188):97-106.
[2] 张为家,刘孝荣,李官成,贺智敏.人源性抗HER2胞外段Fab噬菌体抗体库的构建及筛选[J].细胞与分子免疫学杂志,2011,27(03):297-300.
[3] 王洁琼.弥漫大B细胞淋巴瘤预后因素的研究[D].上海:上海交通大学,2014.
[4]霍文禮,王希海,卢再鸣.放射组学在宫颈癌中的应用[J].现代肿瘤医学,2019,27(24):4467-4471.
[5]李惠明,张军.基于影像组学的人工智能在脑胶质瘤MRI诊断中的应用[J].国际医学放射学杂志,2019,42(5):531-534,546.
[6] 刘培进.伽玛射线立体定向放射治疗早期原发性肝癌的临床价值研究[J].智慧健康,2018,4(30):7-8.
[7]Shamsi M,Sedaghatkish A,Dejam M,et al.Magnetically assisted intraperitoneal drug delivery for cancer chemotherapy[J].Drug Delivery,2018,25(1):846-861.
[8]Hosny A,ParmarC,QuackenbushJ,et al.Artifice cialintelligence in radiology[J].Nat Rev Cacer,2018,18(8):500-510.
[9]Nwankwo O,Mekdash H,SihonoDSK,et al.Knowledge-based radiation therapy(KBRT)treatment planning versus planning by experts:validation of a KBRT algorithm for prostate cancer treatment planning[J].Radiate Oncol,2015,10(1):111.
[10]Saw CB,Li S,Battin F,et al.External beam planning module of Eclipse for external beam radiation therapy[J].Med Dosim,2018,43(2):195-204.
[11]Ibragimov B,Xing L.Segmentation of organs-at-risks in head and neck CT images using convolutional neural networks[J].Med Physics,2017,44(2):547-557.
[12]Liu Y,Stojadinovic S,Hrycushko B,et al.A deep convolutional neural network-based automatic delineation strategy for multiple brain metastases stereotactic radiosurgery[J].PLoS One,2017,12(10):e0185844.
[13]李益民,兰美,张佳瑜,等.人工智能:肿瘤放疗的机遇与挑战[J].中华放射肿瘤学杂志,2019,28(6):476-480.
[14] 汪弋汀. 基于TCGA数据和体外实验探索NSCLC放疗敏感性机制[D].上海交通大学,2018.
[15]王卫东,郞锦义.基于生命/影像组学和人工智能的精确放射治疗:思考与展望[J].中国肿瘤临床,2018,45(12):604-608.
[16]Hatt M,Tixier F,Visvikis D,et al.Radiomics in PET/CT:More Than Meets the Eye[J].Journal of Nuclear Medicine,2017,58(3):365-366.
[17]Zhou M,Scott J,Chaudhury B,et al.Radiomics in Brain Tumor:Image Assessment,Quantitative Feature Descriptors,and Machine-Learning Approaches[J].AJNR Am J Neuroradiol,2018,39(2):208-216.
[18]Konig IR,Fuchs O.What is precision medicine[J].Eur Respir J,2017,50(4):236-237.
[19]Dalton WS,Friend SH.Cancer biomarkers--an invitation to the table[J].Science(New York,NY),2006,312(5777):1165-8.
[20]Torres-Roca JF,Eschrich S,Zhao H,et al.Prediction of radiation sensitivity using a gene expression classifier[J].Cancer Res,2005,65(16):7169-7176.
[21]Eschrich SA,Pramana J,Zhang H,et al.A gene expression model of intrinsic tumor radiosensitivity:prediction of response and prognosis after chemoradiation[J].Int J Radiat Oncol Biol Phys,2009,75(2):489-496.
[22]Jeong H,Mason SP,Barabasi AL,et al.Lethality and centrality in protein networks[J].Nature,2001,411(6833):41-42.
[23]Deng X,Hofmann ER,Villanueva A,et al.Caenorhabditis elegansABL-1 an-tagonizesp53-mediated germline apoptosis after ionizing irradiation[J].Nat Genet,2004,36(8):906-912.
[24]Wang QE,Zhu Q,Wani G,et al.DNA repair factor XPC is modified by SUMO-1 and ubiquitin following UV irradiation[J].Nucleic acids research,2005,33(13):4023-4034.
[25]Cerna D,Camphausen K,Tofilon PJ.Histone deacetylation as a target for radi-osensitization[J].Current topics in developmental biology,2006(73):173-204.
[26]Weichselbaum RR,Ishwaran H,Yoon T,et al.An interferon-related gene signa-ture for DNA damage resistance is a predictive marker for chemotherapy and radiation for breast cancer[J].ProcNatl Acad Sci USA,2008,105(47):18490-18495.
[27]Torres-Roca JF,Eschrich S,Zhao H,et al.Prediction of Radiation Sensitivity Using a Gene Expression Classifier[J].Cancer Research,2017,65(16):7169-7176.
[28]Torres-Roca JF,Fulp WJ,Caudell JJ,et al.Integration of a Radiosensitivity Molecular Signature into the Assessment of Local Recurrence Risk in Breast Cancer[J].Int J Radiat Oncol Biol Phys,2015,93(3):631-638.
[29]Yamazaki H,Takagi S,Ogi N,et al.Radiosensensitivity Index Shows Promise for Predicting Outcomes With Adjuvant Radiation in Resected Pancreatic Cancer Patients[J].Int J Radiat Oncol Biol Phys,2014,90(1):S174.
[30]Speers C,Shuang GZ,Liu M,et al.Development and Validation of a Novel Ra-diosensitivity Signature in Human Breast Cancer[J].Clin Cancer Res,2015,21(16):3667-3677.
[31]Scott JG,Berglund A,Schell MJ,et al.A genome-based model for adjusting radiotherapy dose (GARD):a retrospective,cohort-based study[J].The Lancet Oncology,2017,18(2):202-211.
[32]Eschrich SA,Pramana J,Zhang H,et al.A Gene Expression Model of Intrinsic Tumor Radiosensitivity:Prediction of Response and Prognosis AfterChemoradiation[J].Int J Radiat Oncol Biol Phys,2009,75(2):489-496.
[33]Poortmans P,Kaidar-Person O,Span P.Radiation oncology enters the era of in-dividualised medicine[J].The Lancet Oncology,2017,18(2):159-160.
[34]Jaffee EM,Dang CV,Agus DB,et al.Future cancer research priorities in the USA:a Lancet Oncology Commission[J].The Lancet Oncology,2017,18(11):e653-e706.
收稿日期:2020-06-16;修回日期:2020-06-23
編辑/肖婷婷
基金项目:1.广西卫生健康委员会科研课题(编号:Z20201201);2.广西贵港市科技攻关项目(编号:贵科攻1407014)
作者简介:蔡凯(1972.11-),男,广西贵港人,硕士,副主任医师,主要从事肿瘤放射治疗、中西医结合综合治疗的临床研究

