不同干燥和炮制方法对天麻品质的影响*
张玮玮,郑司浩,王永辉,王 伟,张志鹏,蔡翠芳
(1. 山西药科职业学院 太原 030031;2. 山西中医药大学 榆次 030600;3. 中国中药有限公司 北京 100195;4. 山西国新晋药集团有限公司 太原 030032)
天麻为兰科天麻属植物天麻Gastrodia elataBl.的干燥块茎[1],是我国的名贵中药材之一,也是重要的药食两用中药材。具有平抑肝阳、息风止痉、祛风通络的功效[1]。其主要成分有天麻素、天麻苷元等酚类化合物及多糖类、甾醇、有机酸等[2-4]。现代药理研究表明天麻具有镇静、抗惊厥、促进睡眠和神经保护作用等作用[5-9]。临床上用于治疗高血压、偏头痛及心脑血管等疾病[10-11]。天麻炮制方法始于《雷公炮炙论》记载用蒺藜煨法,后经改良为酒浸和加热等方面[12],目前加工方法多采用蒸制法或水煮法,起到“杀酶保苷”的作用[13],不同的炮制方法会导致天麻素成分的部分损失,不同的产地加工和干燥方式也会影响药材品质的形成[14-15]。此外,目前对天麻品质考察多基于测定天麻素及羟基苯甲醇的含量[16-17]。本研究分别采用晒干、热风干燥、冷冻干燥、减压干燥处理方式对新鲜天麻切片进行干燥加工,以及进行煮制、微波炮制、蒸制、酒制、姜制、蜜制等炮制加工,建立HPLC 法同时测定天麻中天麻素、对羟基苯甲醇、巴利森苷A、巴利森苷B、巴利森苷C、巴利森苷E 等6 种化合物有效含量,以及通过苯酚-硫酸法测定多糖含量变化,旨在观察不同干燥方法和炮制工艺的差异,同时为天麻的产地加工提供有效方法。
1 仪器与试药
Agilent 1200-液相色谱仪(Agilent 公司,包括四元梯度泵、在线脱气机、DAD 检测器);METTLER AB135-S 型电子天平(瑞士);Agilent HC-C18 色谱柱(4.6 × 250 mm,5 μm);KQ-500DE 型超声波清洗器(昆山市超声仪器有限公司);SL-500A 型高速多功能粉碎机(北京恒瑞森科技开发有限责任公司);101-0AB 型电热鼓风干燥箱、DRT-TW 型调温电热套(北京中兴伟业仪器有限公司);DZF-6050 型真空干燥箱(上海博迅实业有限公司);LGJ-10型真空冷冻干燥机(宁波新艺超声设备有限公司);L5 型紫外-可见光分光光度计(上海仪电分析仪器有限公司);GL-20G-Ⅱ型离心机(上海安亭科技仪器厂);P70D20TL-D4 型微波炉(广东格兰仕集团有限公司)。
天麻素对照品(批号16081941,纯度98.0%),购自上海同田生物技术有限公司、对羟基苯甲醇照品(批号111910-201501,纯度98.5%),D-无水葡萄糖对照品(批号110833-201506,纯度99.9%)购自中国食品药品检定研究院;巴利森苷A、B、C、E(实验室自制,纯度≥98%),乙腈、甲醇(色谱纯,美国Fisher 公司);其他试剂均为分析纯。天麻药材采自贵州道真县,经山西药科职业学院蔡翠芳教授鉴定为兰科植物天麻Gastrodia elataBl.的干燥块茎。
2 样品制备
2.1 不同干燥方法
取大小均匀且等级为100-150 g/支的新鲜天麻2000 g,手 工 切1-2 mm 的 薄 片,得1911 g(得 率95.55%),备用。按照以下四种干燥方法处理后,每种方法取新鲜天麻片100 g 左右,重复3 次。①晒干:日光下常温晾晒至干;②减压干燥:放于60℃真空干燥箱里烘干;③冷冻干燥:冰箱预冻2小时后放入冷冻干燥机中48 h,真空抽干;④热风干燥:放于100℃干燥箱里干燥。
2.2 不同炮制方法
取大小均匀且等级为100-150 g/支的新鲜天麻2000 g,手 工 切1-2 mm 的 薄 片,得1918 g(得 率95.90%),备用。按照以下六种炮制方法处理后,每种方法取新鲜天麻片100 g 左右,重复3 次。①煮制:放入沸水中煮5 min,再于60℃烘箱热风干燥;②蒸制:在蒸锅上蒸10 min,再于60℃烘箱热风干燥;③微波炮制:放于微波炉(功率800 W)加热1 min,然后隔水蒸10 min,取出60 ℃烘干;④酒制:与黄酒拌匀,放置闷润过夜,然后隔水蒸10 min,取出60 ℃烘干;⑤姜制:与姜汁拌匀,闷润过夜,隔水蒸10 min 后取出60 ℃烘干;⑥蜜制:用蜜汁包裹均匀,然后隔水蒸10 min,取出60 ℃烘干。
2.3 含量测定
2.3.1 对照品溶液制备
精密量取天麻素、对基苯甲醇、巴利森苷A、巴利森苷B、巴利森苷C、巴利森苷E对照品适量,置25 mL容量瓶中,加乙腈-水(3∶97)稀释至刻度,摇匀,分别制成 0.0819、0.1631、0.0862、0.1007、0.0984、0.0917 mg·mL-1的混合对照品溶液。
2.3.2 供试品溶液制备
精密称取0.5 g 天麻粉末,置入具塞锥形瓶,精密加入25 mL 稀乙醇,称重,超声30 min(功率300 W,频率25 Hz),放置室温后再称重,用稀乙醇补足重量,过滤,精密量取10 mL续滤液,浓缩至干,残渣加乙腈-水(3:97)混合液溶解,移至10 mL 容量瓶中定容,摇匀,过滤,即得[1]。
色谱条件采用Agilent HC-C18(4.6 mm×250 mm,5 μm);以乙腈(A)-0.05% 磷酸(B)为流动相,梯度洗脱(0 - 10 min,2% - 10% A;10 - 60 min,10% - 40%A),检测波长220 nm,体积流量1 mL·min-1,柱温30 ℃,进样体积10 μL,理论塔板数以天麻素计算不低于3000[1]。
2.3.3 苯酚-硫酸法测定多糖的含量
葡萄糖对照品溶液的制备:精密称取D-无水葡萄糖对照品加纯水溶解,摇匀,得到1 mg·mL-1的对照品溶液,备用。分别吸取该贮备液0.1、0.2、0.5、1、2 mL于10 mL 量瓶中,加纯水定容至刻度,摇匀[18]。再分别吸取1.0 mL 不同浓度梯度的葡萄糖溶于具塞试管中,加5%苯酚溶液1.0 mL,摇匀;加5.0 mL 浓硫酸,摇匀静置10 min 后,沸水浴15 min,冷却至室温,空白溶液调0,在490 nm波长下测定吸光度[18]。
天麻多糖的提取:分别精密称取不同处理方法的天麻饮片粉末0.5 g,置于烧瓶中加80%乙醇50 mL,回流2 次,每次60 min,趁热过滤,弃去滤液,残渣挥去乙醇,残渣加纯水100 mL 提取2 次,每次60 min,趁热过滤,放冷后移入500 mL 量瓶,加纯水至刻度作为天麻多糖提取液,备用。
天麻多糖的含量测定:分别精密吸取上述天麻多糖的提取液0.2 mL,置具塞试管中加蒸馏水至1.0 mL,摇匀,分别加入5%苯酚溶液1.0 mL,摇匀后迅速滴加浓硫酸5.0 mL,摇匀后放置10 min,置沸水浴中加热15 min,取出冷却至室温,每种方法提取液3 次平行显色,采用分光光度法490 nm 处测定。由于蜜制天麻在加工中添加了蜜汁辅料,会对天麻多糖含量的测定造成干扰,因此蜜制天麻的多糖含量测定结果仅做参考。
3 结果
3.1 方法学考察
3.1.1 标准曲线的绘制
分别精密量取混合对照品贮备液并置入10 mL容量瓶中,加乙腈-水(3∶97)稀释至刻度,摇匀,配制成一系列不同质量浓度的对照品溶液。分别吸取10 μL不同浓度的对照品溶液及原浓度储备液,按“2.3.2”项下色谱条件进行检测,记录各化合物色谱峰面积。按照横坐标(X)为质量浓度(μg·mL-1)、纵坐标(Y)为峰面积绘制标准曲线,最终计算得出各化学成分的回归方程(见表1)。6 种化学成分的r值均>0.9990,表明其在各自线性范围内呈良好线性关系。

表1 六种化学成分的回归方程
3.1.2 精密度试验
分别精密吸取10 μL同一对照品溶液,连续进样6次,按照“2.3”项下方法测定天麻素、对羟基苯甲醇、巴利森苷A 等6 种化学成分的色谱峰面积,经计算6 种化学成分的RSD 值分别为0.8%、0.5%、0.4%、0.4%、0.6%、0.4%,结果表明仪器具有良好的精密度。
3.1.3 重复性试验
取6 份同一样品(S1),按“2.3”项下方法进行供试品溶液制备和含量测定,记录天麻素、对羟基苯甲醇、巴利森苷A 等6 种化学成分的色谱峰面积,经计算6种化学成分的RSD 值分别为1.0%、0.9%、0.7%、0.8%、1.6%、1.4%,结果表明该方法具有良好的重复性。
3.1.4 稳定性试验
取一份天麻药材粉末(S1)按“2.3.2”项下方法进行供试品溶液制备。供试品溶液在室温下放置0、2、4、8、12、24 h 后,按照时间梯度进样测定天麻素、对羟基苯甲醇、巴利森苷A 等6种化学成分的色谱峰面积,经计算6 种化学成分的RSD 值分别为0.2%、0.4%、0.3%、0.2%、0.2%、0.3%,结果表明供试品溶液在24 h内稳定。
3.1.5 加样回收率试验
精密称定9 份0.5 g 已知含量的同一样品(S1),置入锥形瓶分别精密加入低、中、高3个浓度水平的混合对照品,每个剂量平行3份,按“2.3.2”项下方法制备供试品溶液并进行检测,经计算得出6 种化学成分的加样回收率均在95%-105%且RSD值<3%,见表2。

表2 六种化学成分加样回率收试验结果
3.2 不同干燥方法处理的天麻中6 种化学成分含量测定
取不同干燥方法处理后的天麻,按照“2.3”项下方法制备供试品溶液并按其色谱条件进样测定,混合对照品及天麻样品HPLC 色谱图见图1。按“3.1”项下回归方程计算天麻素、对羟基苯甲醇、巴利森苷A、巴利森苷B、巴利森苷C 及巴利森苷E 的含量,结果见表3。由表可知,采取冷冻干燥处理的天麻中天麻素、对羟基苯甲醇、巴利森苷A、巴利森苷B、巴利森苷C及巴利森苷E六种化学成分的含量均高于经晒干、热风干燥、减压干燥处理后的天麻。
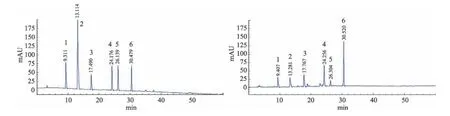
图1 天麻HPLC色谱图(左图为混合对照品,右图为样品)
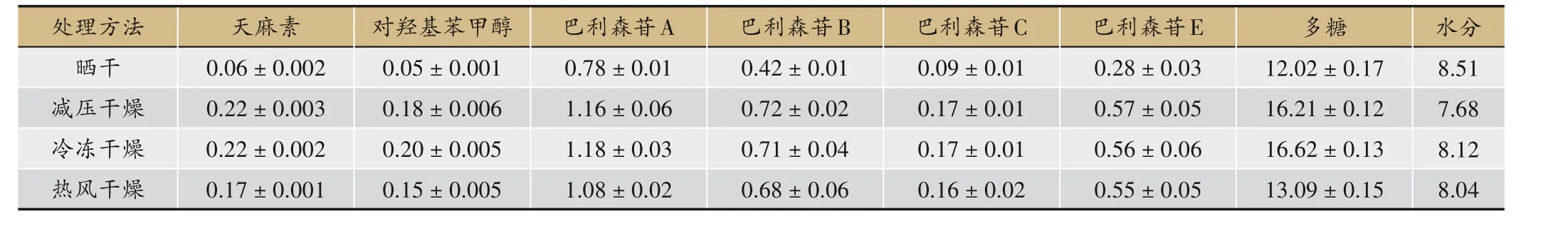
表3 不同干燥方法处理的天麻样品中六种化学成分及多糖含量(单位:%;n = 3)

表4 不同炮制方法处理的天麻样品中六种化学成分及多糖含量(单位:%;n = 3)
3.3 不同炮制方法处理的天麻中6 种化学成分含量测定
取不同炮制方法处理后的天麻,按照“2.3”项下方法制备供试品溶液并按其色谱条件进样测定,并按“3.1”项下回归方程计算6个化学成分的含量,结果见表4。由表可知,在微波炮制、煮制、蒸制、酒制、姜制、蜜制等六种炮制方法中,经微波炮制处理的天麻中天麻素、对羟基苯甲醇、巴利森苷A、巴利森苷B、巴利森苷C及巴利森苷E等六种化学成分的含量均高于其他五种炮制方法处理后的天麻。
3.4 不同加工方式处理的天麻中多糖含量测定
按“2.3.3”项下方法,以质量浓度(X,μg·mL-1)为横坐标,吸光度(Y)为纵坐标绘制标准曲线,得回归方程Y=31.621X+0.0362(r=0.9990,n=6),表明葡萄糖浓度在0 - 200 μg/mL 内呈现良好的线性关系。每份天麻样品粉末称取2份,按“2.3.3”项下方法测定,并计算不同工艺条件下天麻中多糖的含量。4种不同干燥方法条件下天麻中多糖含量见表3,结果表明经冷冻干燥的天麻中多糖含量最高为16.62%。6种不同炮制方法条件下天麻中多糖含量见表4,结果表明经微波炮制的天麻中多糖含量最高(16.56%),蒸制天麻(15.58%)多糖含量次之。
4 讨论
中药材产地加工干燥方法对其有效成分含量和外观具有显著影响,而中药炮制是传统中医药体系的重要组成部分,也是中药现代化的的关键环节,两者均影响中药饮片质量稳定和中药治疗的效果[19-21]。本研究以天麻素、对羟基苯甲醇、巴利森苷A、巴利森苷B、巴利森苷C、巴利森苷E和多糖作为主要指标,评估不同干燥方法和炮制方法处理后天麻药材的品质。研究发现天麻不同干燥品的指标成分含量存在差异性,其中晒干处理的天麻样品未能够达到2015 版《中华人民共和国药典》规定(含天麻素和对羟基苯甲醇的总量不得少于0.25%),仅为0.11%;减压干燥、冷冻干燥、热风干燥处理后的天麻样品均达到2015 版《中华人民共和国药典》规定且差异较小,为0.32% -0.42%。减压干燥和冷冻干燥的样品中天麻素的含量高于其他处理方式。文献报道巴利森苷类成分不稳定,在不同温度、溶剂条件下,含量差别很大,与天麻素之间存在相互转化见图2[22]。在冷冻干燥时,低温状态下可降低相关酶的活性从而阻止活性成分降解;减压干燥时,真空状态容易破坏细胞结构,从而减少酶促反应的发生,且利于活性成分的溶出;热风干燥时,天麻随着温度的增加,其相关酶活性逐步增加然后降低直至失去活性,由于热风干燥耗时较短,因此其活性成分降解程度较低;而在晒干时,耗时较长,常温状态有利于化学成分之间酶促反应的形成,不能起到“杀酶保苷”的效果,导致活性成分发现降解,从而各项指标均较低。减压干燥和冷冻干燥这两种方法可在保护活性成分的流失的同时,还能使得加工的样品保持较好的外观品相,是干燥天麻的理想之法。
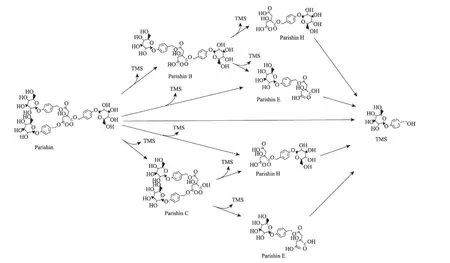
图2 巴利森苷降解途径
目前,为减少天麻有效成分损失,达到“杀酶保苷”的效果,实际生产中其炮制多以蒸法为主。本研究在比较天麻不同炮制方法(煮制、蒸制、微波炮制、酒制、姜制、蜜制)的指标成分含量时,发现不同炮制品的指标成分含量存在差异性,天麻素和对羟基苯甲醇总量为0.27% - 0.52%变幅较大,但均符合2015年版《中华人民共和国药典》规定。本研究表明,微波炮制所得天麻样品中的6种化学成分和多糖含量较其它炮制方法高,其次为蜜制、煮制、蒸制,最后为酒制、姜制,与文献报道一致[23]。酒制、姜制对天麻前处理时需要闷润过夜,再行隔水蒸。而在闷润过夜这一较长的前处理过程,天麻内部的活性成分在酶的活性作用下发生转化和分解,使得酒制、姜制天麻样品检测到的成分含量较低;煮制、蒸制、蜜制前处理过程较短,便煮或蒸,可以及时的进行加温处理,经过高温使酶类失活,最大程度上保护了活性成分不被酶水解,但缓慢的加热过程也不可避免活性成分被酶水解,直至高温使得酶类失活。而微波炮制的原理是利用短波长、高频率的电磁波使以水分子为主的极性分子振动摩擦而产生大热量,并以热的形式在物料内表现出来,从而使物料在短时间内加热、干燥或熟化[24]。对天麻进行的微波炮制,将鲜天麻进行1 min 微波加热处理后再隔水蒸,而微波能量集中稳定、加热效率高的特点,有利于在很短的时间内破坏天麻的酶活性,阻碍各化学成分间的转化,同时微波其穿透力强的特点更有利于化学成分的溶出,Fan 等的研究表明微波炮制可以提高天麻中天麻素、对羟基苯甲醇等成分的含量[25],故微波炮制所得天麻样品中的天麻素、对羟基苯甲醇、巴利森苷和多糖含量较其它炮制方法高。因此,基于未来新型设备的发展,微波干燥可作为天麻产地加工的发展方向。
以上实验表明,最佳干燥方法为减压干燥和冷冻干燥,最佳炮制方法为微波炮制,可为天麻加工生产工艺的制定提供一定的方法学参考和科学理论支撑。为保证天麻的质量稳定,制定出天麻加工炮制规范,还需对天麻的加工和炮制过程进行量化,并从经济可行性的角度进行评价以确保能够匹配到实际生产应用。

