糖尿病患者维持性血液透析生存分析及预测模型构建
陈 颖 沈 毅 贾玉敏 沈 燕 戴厚永 吴建华 陈晓岚 范亚平 黄 希 袁 莉
根据国际糖尿病联合会(IDF)最新统计,2019年全球糖尿病患者约有4.63亿人,我国糖尿病患者人数约1.164亿,位居全球之首。全球约80% 的终末期肾病(ESRD)是由糖尿病、高血压或两者共同造成[1],糖尿病和慢性肾脏疾病(CKD)也与心血管疾病高度相关。临床实践研究证明,糖尿病患者进入透析后,由于心血管疾病等因素的协同作用,无论是给予透析治疗还是肾移植,远期预后均较非糖尿病透析患者差[2]。根据美国肾脏数据系统(USRDS)报告,2014年糖尿病ESRD患者开始透析后3年生存率为58.2%[3]。
风险预测模型作为一种预测终点事件发生概率的工具,可纳入所有已知的预测因素,客观系统地确定高风险人群,为病情评估、风险预判提供参考[4]。本研究回顾性分析糖尿病维持性血液透析(MHD)患者的病历资料,构建列线图为评估患者的死亡风险及制订相应的治疗方案提供相应的建议。
对象和方法
研究对象2013年1月至2016年12月在南通大学附属医院及南通大学第二附属医院肾内科行规律性血液透析的糖尿病ESRD患者,包括临床诊断为糖尿病肾病(DN)及合并糖尿病的CKD血液透析患者,透析时长均超过3个月。根据CKD-EPI公式估算的肾小球滤过率(eGFR)[5],进入透析时研究对象均处于CKD 4期或5期。
排除标准:(1)基本信息资料缺失,如性别、年龄、首次透析时间等;(2)透析时间≤3个月;(3)年龄<18岁;(4)无实验室数据或数据缺失严重。
研究因素利用医院的电子病历系统查询患者资料,建立信息数据库。采用回顾性方法收集患者的社会人口学信息(姓名、性别、年龄、身高、体重等),MHD情况(血管通路、透析开始时间),糖尿病情况(病程、胰岛素使用、糖化血红蛋白),心血管疾病包括冠状动脉粥样硬化性心脏病(冠心病)、外周血管疾病及脑血管疾病,进入透析前多项实验室指标(血常规、肝功能、肾功能、电解质、血脂、血清铁蛋白等),比较不同因素对患者生存时间的影响。共随访3年,研究截止日期为2019-12-31,通过电话随访患者的生存情况,期间若发生死亡,则视为终点事件。
统计学方法采用《SPSS 20.0》及《R 3.5.2》统计软件包进行数据处理与分析,计量资料采用均数±标准差或中位数(四分位间距)表示,两组间比较采用独立样本t检验或Mann-Whitney U检验。计数资料采用频数(百分比)表示,组间比较采用卡方检验。采用COX比例风险模型筛选影响预后的危险因素,为了避免漏掉重要因素,将单因素分析中显著性检验水准α放宽至0.2,并将某些可能的影响因素纳入多因素分析。根据COX回归结果,采用R软件rms、nomogramEx、survival等程序包构建患者预后生存风险列线图,并计算一致系数(C-index)作模型评价,其值越接近1代表模型分辨度越好。P<0.05为差异有统计学意义。
结 果
基本情况及临床资料纳入186例患者,男性114例(61.3%),DN患者125例(67.2%),开始透析年龄27~84岁,平均年龄62±13岁,中位年龄64(54~73)岁,1年,2年和3年累积生存率分别为88.7%,74.2%,64.5%。180例(96.8%)患者合并高血压,中位病程为10(7~14)年。糖尿病中位病程为10(9~15)年,129例(69.4%)接受胰岛素治疗,90例(48.4%)发生心血管疾病。将研究对象按照生存状况分为生存组120例(64.5%)和死亡组66例(35.5%),基本情况见表1,两组患者的开始透析年龄、糖尿病病程、血管通路、心血管疾病患病情况之间差异有统计学意义(P<0.05)。

表1 生存组和死亡组患者基本情况比较
实验室检查比较生存组和死亡组患者透析前的多项实验室检查,结果如表2显示,死亡组超敏C反应蛋白水平高于生存组(P<0.05)。
COX比例风险模型分析结果随访3年,66例(35.5%)患者死亡。将COX单因素分析中有意义的变量绘制Kaplan-Meier生存曲线(Log-rank法),筛选P<0.2的预测变量,并纳入某些重要的临床指标进行多因素分析。单因素Kaplan-Meier曲线显示,糖尿病病程<10年、无心血管疾病、血管通路为动静脉内瘘、开始透析年龄<60岁的患者预后较好(P均<0.05)(图1)。考虑到混杂因素的影响,在多因素分析(LR逐步向前法)中调整性别及原发病,进入方程的因素为糖尿病病程、心血管疾病、血管通路及eGFR(表3)。
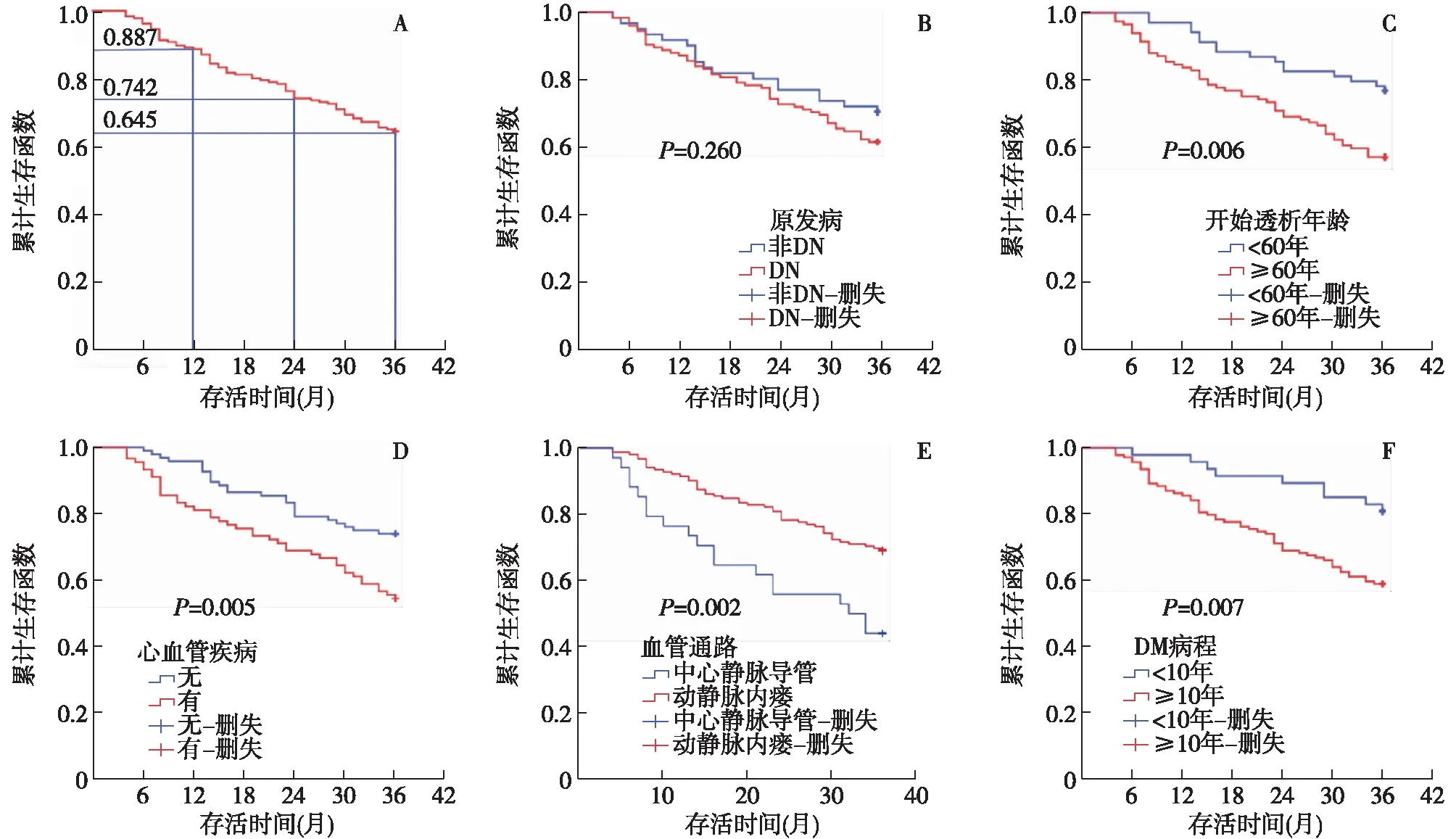
图1 COX单因素分析Kaplan-Meier生存曲线A:总体生存曲线;B:原发病(非DN/DN);C:开始透析年龄(<60岁/≥60岁);D:心血管疾病(无/有);E:血管通路(动静脉内瘘/长期中心静脉导管);F:DM病程(<10年/≥10年);DM:糖尿病;DN:糖尿病肾病

表3 不同指标对死亡风险影响的COX比例风险模型
糖尿病MHD患者生存分析列线图列线图C-index为0.670(95%CI 0.604~0.737),绘图后可知各因素在刻度尺上所对应的单项得分、总得分及1年、2年、3年生存概率(图2)。采用Bootstrap法内部检验1 000次,标准误为0.034,3年预测生存概率标准曲线显示模型预测的生存概率与实际结果之间具有较好的符合度(图3)。按各个预测指标在列线图中画上竖线计算各因素对应的得分,将各因素的得分累计相加得到总得分,总得分画下竖线与1年、2年、3年生存概率线相交即可得到该患者对应的预测概率。
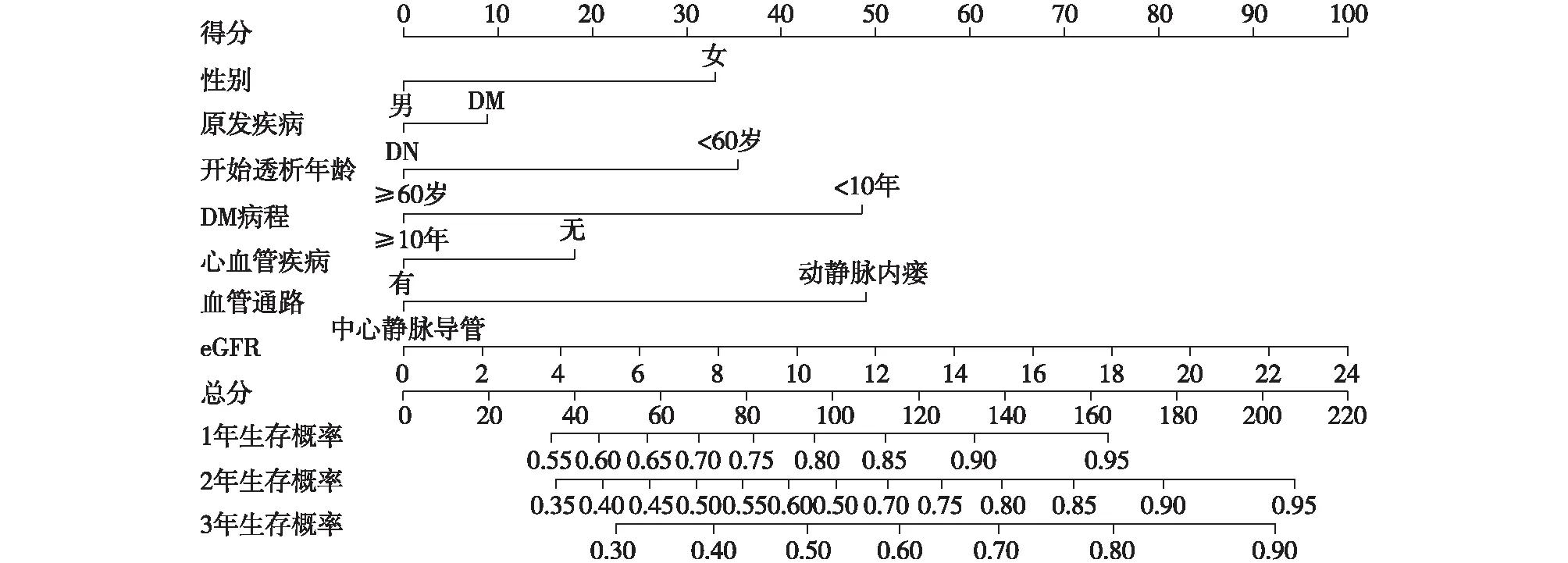
图2 糖尿病MHD患者生存概率预测列线图eGFR:估算的肾小球滤过率;MHD:维持性血液透析
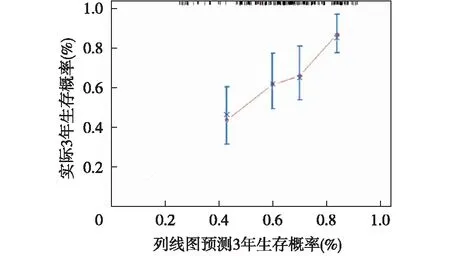
图3 列线图预测糖尿病MHD患者3年生存概率与实际3年生存概率标准曲线MHD:维持性血液透析;样本分为4组,每组47例,使用Bootstrap法自助抽1 000次
讨 论
根据USRDS的资料,糖尿病透析患者死亡率较非糖尿病透析患者高出1.3倍[6]。通过建立预测模型,可识别死亡风险增加的患者,提供有价值的预后信息,帮助临床医师有效识别高危患者,并加强护理和支持性治疗。本研究选择透析超过3个月的ESRD患者作为研究对象,主要考虑以下几点:首先,在3个月的肾脏替代治疗后,患者转为长期透析,血液透析或腹膜透析方式的选择将更明确;其次,将在3个月内排除因急性肾功能衰竭而恢复或死亡的患者,可建立一个更加稳健的模型。此外,在3个月时,患者的临床状况趋于稳定,有利于分析非急性期的预后相关问题[7]。
本研究中的糖尿病MHD患者1年、2年、3年生存率明显下降,分别为88.7%,74.2%,64.5%。Kaplan-Meier曲线显示,无心血管疾病、开始透析年龄<60岁、糖尿病病程<10年、MHD血管通路为动静脉内瘘的患者预后较好(P均<0.05)。经多因素COX分析后,最终进入模型的因素为心血管疾病、eGFR、糖尿病病程和血管通路。
心血管疾病是糖尿病CKD患者死亡的主要原因,占糖尿病ESRD患者死亡率的50%以上[8]。虽然透析技术的发展日新月异,但即使是最好的透析模式亦无法逆转透析前积累的心血管损伤[9]。Tsur等[10]对652例糖尿病透析患者进行回顾性研究,收集患者透析前12月及透析后6月的临床及生化指标,结果显示透析前心血管疾病与死亡风险明显相关。本研究亦发现心血管疾病是危险因素,提示在CKD的管理中,透析前的护理和治疗可能是更好、更有效的经济策略。
糖尿病ESRD患者由于存在不同程度高血压,心血管病变,胰岛素分泌异常易合并高血糖酮症酸中毒,水电解紊乱及贫血均较非糖尿病患者早,因此需较早开始血液透析。《中国血液净化标准操作规程(2010)》推荐,高风险患者(合并糖尿病)需结合临床症状适当提早开始透析治疗[11]。本研究选用,使用进入透析前肌酐估算eGFR,COX多因素分析显示开始透析时低eGFR是死亡的危险因素,提示专科医师需尽早评估糖尿病ESRD患者预后情况,适时透析。
糖尿病病程越长,多系统并发症的发生率越高,同时病情越重,已有多个研究证实糖尿病的病程与MHD患者死亡率正相关[7,10]。本研究中,糖尿病病程也是死亡的危险因素之一。血管通路是MHD患者的生命线,自体动静脉内瘘是最佳的长期血管通路,但糖尿病患者常合并高血压、动脉粥样硬化和脂质代谢异常等多种并发症,血管条件差,另外可能并发严重心力衰竭。在以上情况下,需要使用长期中心静脉置管作为血管通路。结果显示,长期中心静脉导管置入不良预后的风险是动静脉内瘘的2.184倍,此结果可能和该类患者的心血管并发症严重相关。
目前有多项研究均提示了糖尿病透析患者预后不良的相关风险因素[12-16],但鲜有研究提及糖尿病透析患者死亡预测模型[7]。相较于风险预测模型复杂的计算公式,列线图可以整合多个因素并将模型通过直观的图形展示,简化为单一的数值估计事件的概率[17],以提供更好的个体化预后风险评估。目前有少量报道将列线图应用于肾脏病研究,如狼疮肾炎患者预后分析[18],预测经肾活检证实的DN患者进入ESRD的风险等[19-20],但国内外尚未将其应用于预测糖尿病ESRD患者的生存概率。
本研究建立了糖尿病ESRD患者血液透析生存预测模型,提示糖尿病病程≥10年、有心血管疾病、血管通路为长期中心静脉导管、低eGFR是影响糖尿病MHD患者生存的独立危险因素。另外,3年标准曲线显示模型预测生存概率与实际情况有较好的符合度。列线图作为预测模型的可视化工具,临床操作性强,可协助医师早期识别预后不良的高危患者,并加强管理,及时监测相关重要指标,为患者制订个性化的诊疗方案,提供精准高效的医疗服务。
我们的研究也存在局限性。(1)研究对象来源于两个中心,数据有限,人群代表性不够,观察期较短。(2)单因素生存曲线显示15月后非DN组的生存优势逐渐明显,DN组与非DN组3年累计生存率分别为61.6%、70.5%,但两组累计生存情况差异无统计学意义,可能与样本量不足有关。同时,本研究中糖尿病透析患者多以临床鉴别诊断是否存在DN,不除外漏误诊的情况。(3)本研究还需前瞻性地在多中心大样本外部人群中进行验证,以提高临床实践过程中的高效性及实用性。(4)MHD患者的预后相关因素非常复杂,本文关注透析前的指标对预后的影响,未收集进入透析后尿素清除指数,透析间期体重增加,不同透析方案、饮食、运动和药物治疗等因素,且未探讨遗传因素、社会经济状况等,上述不足在今后的研究中将进行补充并进一步完善。

