早期干预对食物过敏婴儿其他过敏性疾病发生的预防作用
陈 昂, 王桂兰, 刘翔腾 ,张泉山
(1.广东省中山市博爱医院科教科,广东 中山 528403;2.南方医科大学第二临床医学院儿科,广东 广州 510280;3.广东省中山市博爱医院儿科,广东 中山528403)
食物过敏是指由食物引发的异常免疫反应。2009年在中国3个城市开展的0~2岁儿童流行病学调查[1]显示:食物过敏检出率为5.6%~7.3%。持续食物过敏的儿童在后期出现过敏性鼻炎和哮喘等其他过敏性疾病的风险较高[2-3],对经激发试验确诊的食物过敏患儿应进行早期干预,如严格回避诱发症状的食物,以阻止过敏性疾病的进程[4]。与以往多数回顾性研究不同,本文作者对出生于广东省中山市博爱医院的新生儿进行追踪,以食物过敏婴儿为研究对象,根据是否进行规范干预以及规范干预同时是否添加益生菌进行分组,随访6和12个月后过敏性疾病的发生情况,探讨食物过敏的早期干预对婴儿其他过敏性疾病尤其是哮喘进程的影响。
1 资料与方法
1.1 研究对象2017年1—10月广东省中山市博爱医院产科出生的新生儿在获得家长知情同意后进行问卷调查,共5 712名新生儿纳入队列研究,电话随访并告知家属有过敏表现的患儿回院复诊同时完善相关检查,同时进行食物及呼吸道过敏症状调查和儿童哮喘发病危险因素问卷调查。纳入标准:符合2011年“婴幼儿食物过敏诊治建议”[5],通过详细询问病史、临床表现、变应原皮肤点刺试验、血清特异性IgE检测、食物回避试验和食物激发试验等手段诊断,以食物激发试验为确诊依据;排除标准:资料不完整和依从性差的患儿。本研究通过广东省中山市博爱医院医学伦理委员会审批。
1.2 研究对象分组至2018年10月,共确诊食物过敏患儿313例,剔除随访期间失访的39例后,共有效纳入274例。根据是否进行规范干预以及规范干预(根据患儿家长的个人意愿以及实际干预情况)同时是否添加益生菌分为3组,同时选取同期正常体检无食物过敏婴儿187名作为对照组。①规范干预组(n=134):随访期间在医生指导下对患儿进行综合性管理,采取回避过敏原、深度水解配方奶饮食替代或纯氨基酸配方奶粉饮食替代等措施,做好营养评估及干预(儿童食物过敏的营养管理);②规范干预同时添加益生菌组(n=69):在规范干预的同时添加益生菌,添加双歧杆菌三联活性菌,每次1 g,每日2次,连续应用3个月;③不规 范或无干预组(n=71):患儿未进行规律的干预治疗、完全未干预或继续母乳喂养(母亲不回避过敏原)。剔除标准:对照组研究对象中后期研究中出现食物过敏现象或未能完成随访资料收集则退出本研究。
1.3 随 访纳入研究6和12个月后分别对各组研究对象进行随访,通过电话通知研究对象家属到医院复诊。调查研究对象过敏症状,观察过敏性疾病的发生情况。参照“儿童支气管哮喘诊断与防治指南”和“儿童变应性鼻炎诊断和治疗的专家共识”评价婴儿的过敏性湿疹、过敏性鼻炎和近半年反复喘息或咳嗽的症状,结合哮喘预测指数对儿童哮喘进行早期诊断[6-7],登记相关资料。在随访12个月后,对本组患儿抽取外周血检测嗜酸性粒细胞(eosinophil, EOS)百分率和转化生长因子β1(transforming growth factor-β1, TGF-β1)水平。问卷调查旨在了解研究对象一般情况和家庭环境等。对家中是否有宠物、家中是否装修过、家中是否有花草、家中是否有人吸烟和一级亲属有无过敏史进行调查。质量控制:由小儿呼吸科专科医生进行资料收集;双人复核,确保资料准确。
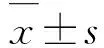
2 结 果
2.1 各组研究对象一般情况各组研究对象年龄、性别和家庭环境(家中是否有宠物、家中是否装修过、家中是否有花草、家中是否有人吸烟)比较差异均无统计学意义(P>0.05)。见表1和表2。
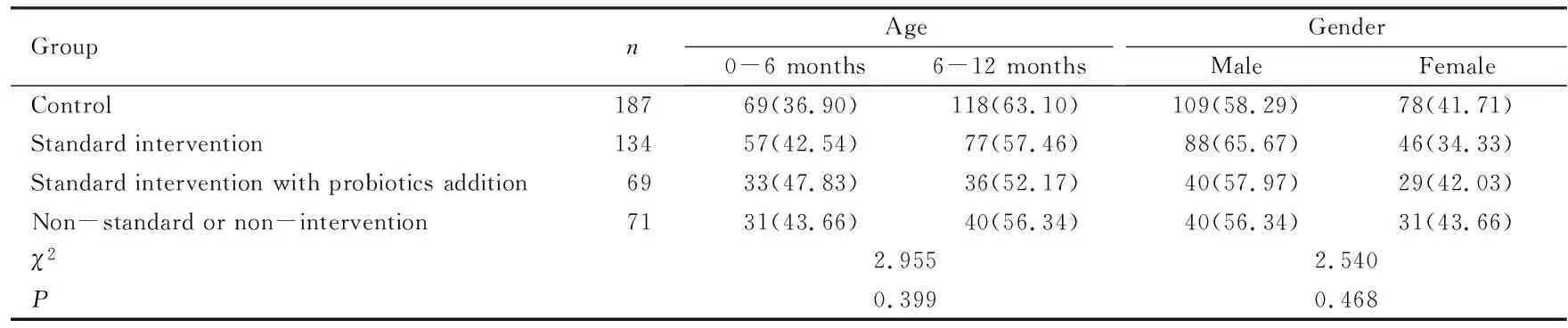
表1 各组研究对象年龄和性别分布
2.2 随访6和12个月后各组研究对象过敏性疾病发生情况随访6和12个月后,不规范或无干预组患儿湿疹、近半年喘息或持续咳嗽和哮喘发生率明显高于对照组(P<0.05),而规范干预组和规范干预同时添加益生菌组患儿与对照组比较差异无统计学意义(P>0.016 7)。随访6个月后,各组研究对象过敏性鼻炎发生率比较差异无统计学意义(P>0.016 7);随访12个月后各组研究对象过敏性鼻炎发生率差异有统计学意义(P<0.01),经两两比较,不规范或无干预组患儿过敏性鼻炎发生率明显高于对照组(P<0.016 7),而规范干预组和规范干预同时添加益生菌组与对照组比较差异无统计学意义(P>0.016 7)。见表3~6。
2.3 随访12个月后各组研究对象外周血EOS百分率和TGF-β1水平随访12个月后,各组研究对象外周血EOS百分率和TGF-β1水平比较差异均有统计学意义(P<0.01)。与对照组比较,其余各组患儿外周血EOS百分率和TGF-β1水平明显升高(P<0.05);与不规范或无干预组比较,规范干预组和规范干预同时添加益生菌组患儿外周血EOS百分率和TGF-β1水平明显降低(P<0.05)。见表7。
3 讨 论
食物过敏是婴儿最为常见的变应性疾病,调查结果[8-9]显示:婴幼儿食物过敏的检出率为7.0%~9.2%,而1岁以内婴儿牛奶过敏发生率为2.0%~7.5%。本研究随访结果显示:本组婴儿食物过敏发生率为4.79%(274/5 712)。研究[2,10-11]提示:婴幼儿期食物过敏可能会增加以后其他过敏性疾病(变应性疾病)的发生率。对1 218名新生儿的前瞻性队列研究[12]表明:鸡蛋过敏能明显增加研究对象婴幼儿时期吸入性过敏的发生。
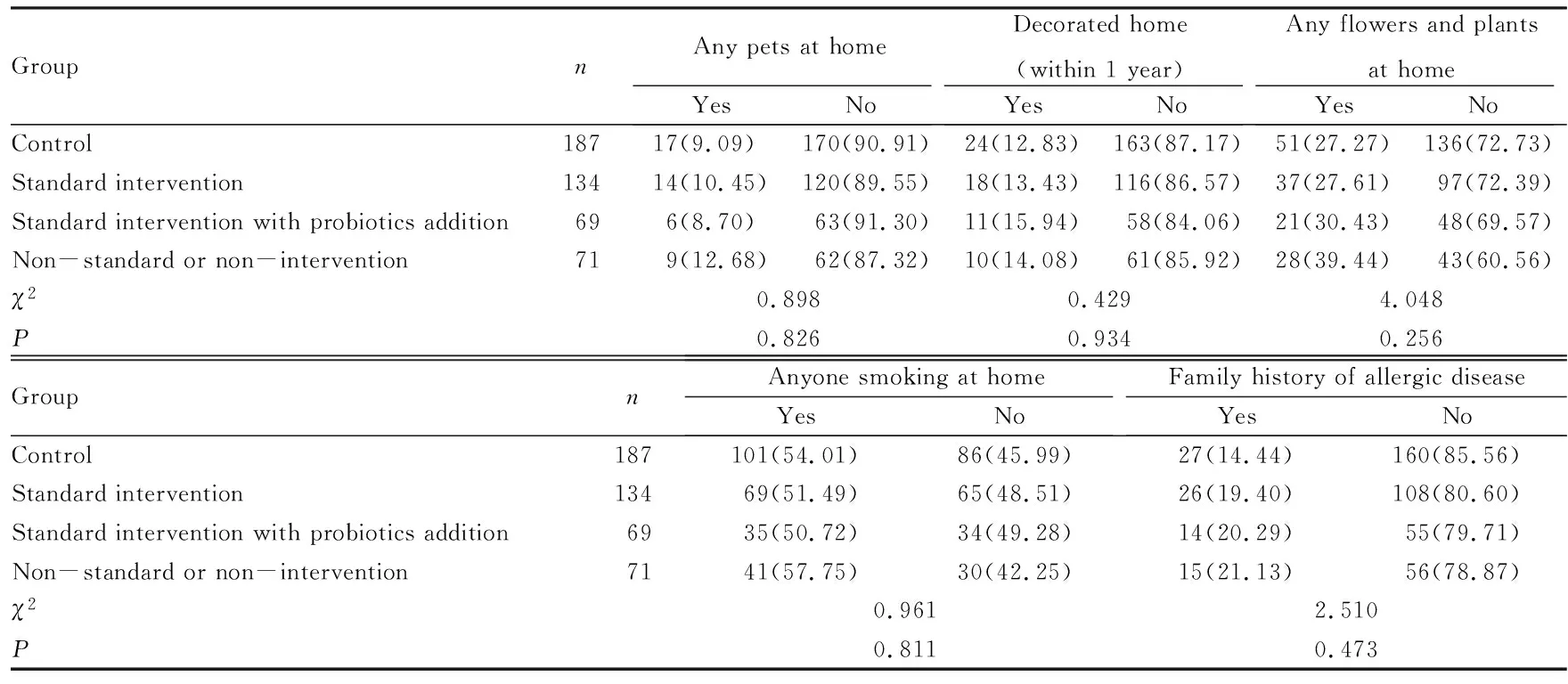
表2 各组研究对象家庭环境
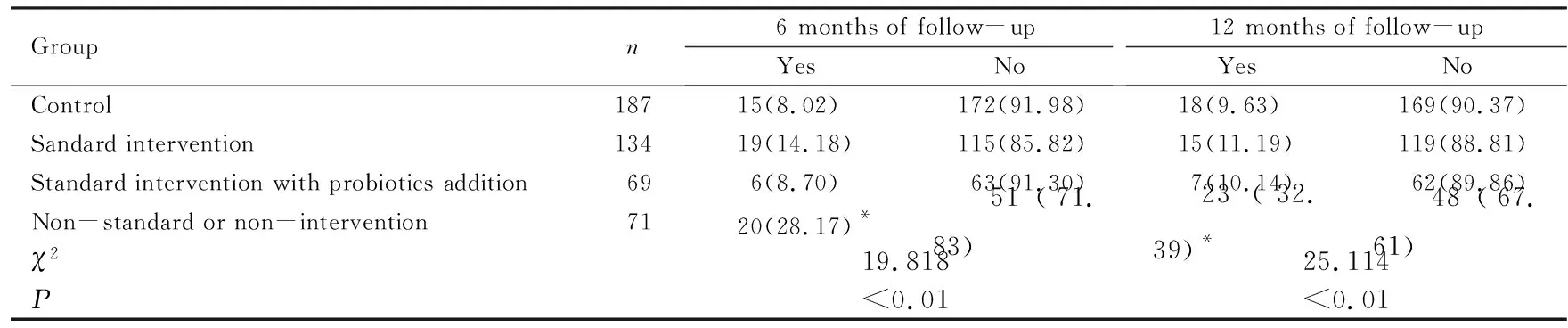
表3 随访过程中各组研究对象湿疹发生率
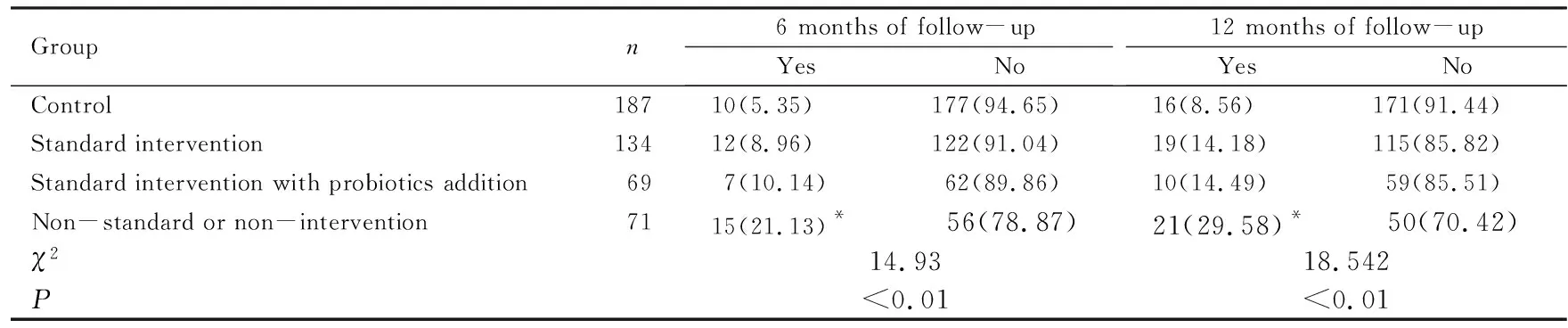
表4 随访过程中各组研究对象喘息或持续咳嗽发生率
本研究主要探讨了食物过敏引起其他过敏性疾病的风险,包括湿疹、近半年喘息或持续咳嗽、过敏性鼻炎和哮喘。Meta分析[13]结果显示:特应性体质、变应性鼻炎、湿疹史、食物过敏史和药物过敏史等过敏性疾病本身就是儿童哮喘的危险因素,69.01%的哮喘患儿伴发皮肤过敏、食物过敏或过敏性鼻炎[14]。
本研究结果提示:未进行干预或不规范干预的食物过敏婴儿较无食物过敏婴儿在未来1年内发生过敏性疾病的风险更高。食物过敏在皮肤表现为变应性皮炎或湿疹,并且年龄越小相关性越强,可出现剧烈瘙痒或局部红斑[15]。
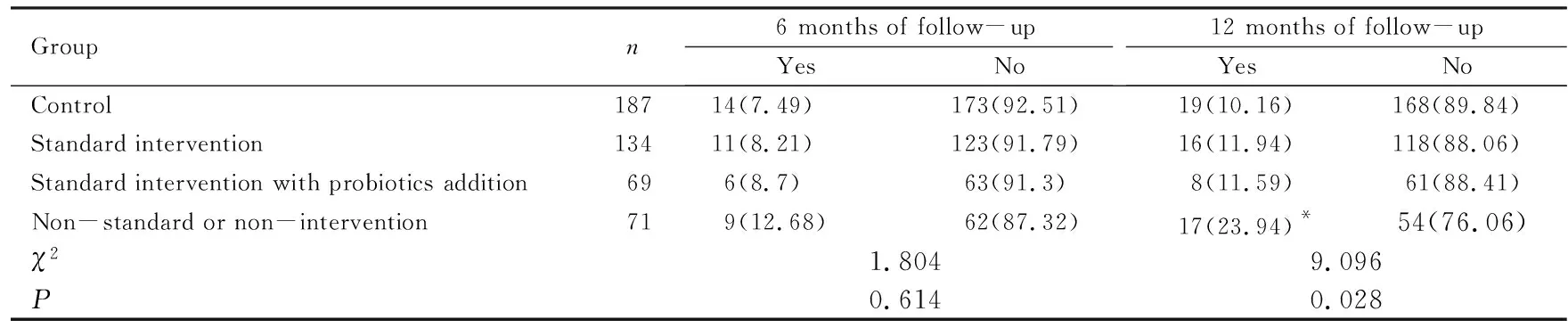
表5 随访过程中各组研究对象过敏性鼻炎发生率
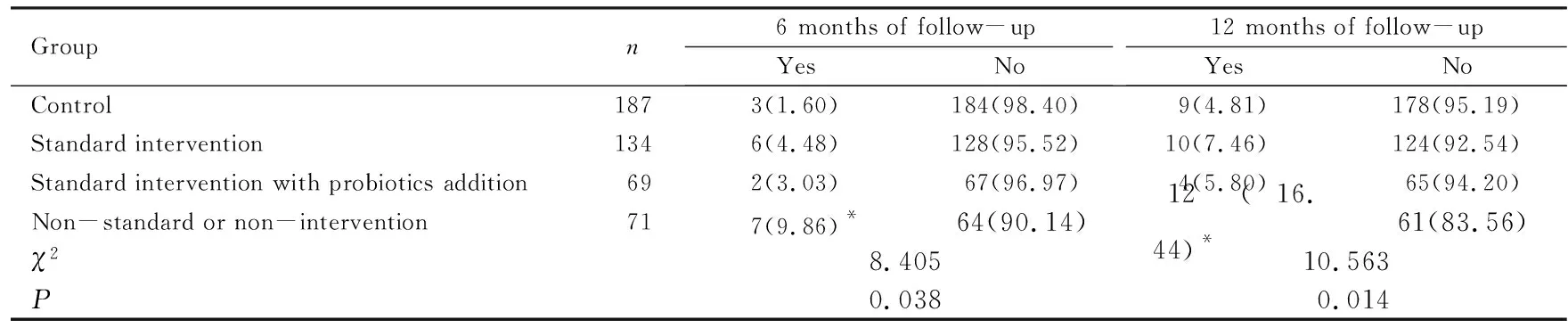
表6 随访过程中各组研究对象哮喘发生率
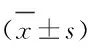
表7 随访过程中各组研究对象外周血EOS百分率和TGF-β1水平
食物过敏与过敏性鼻炎关系的报道较少,杨利桃等[16]研究发现:过敏性鼻炎儿童食入性过敏原以牛奶、虾、蟹和鸡蛋白为主;同时,儿童过敏性鼻炎会增加哮喘的发病风险[17]。食物过敏能够增加哮喘的发病率,并且过敏食物的种类越多,哮喘发病风险越高[3]。
有研究者提出“一个系统、一个疾病”的概念,即支气管哮喘、过敏性鼻炎、特应性皮炎、食物过敏等过敏性疾病具有相同或相似的发病机制,在不同靶器官可表现出不同的症状[18]。当患儿进食致敏食物时,咀嚼的食物小颗粒通过胃食管反流进入呼吸道,刺激气道肥大细胞,引起气道高反应发生[19];当食物过敏患儿进食致敏食物后,食物抗原被胃肠道吸收,引发胃肠道淋巴结炎症反应,引起腹泻等肠道症状,随之食物抗原可经血液循环或淋巴循环抵达身体各处,如到达肺部则可能导致哮喘[20]。
本研究结果显示:未规范干预或无干预组食物过敏婴儿1年后外周血EOS百分率和TGF-β1水平明显高于对照组,而EOS和TGF-β1可能与食物过敏引发过敏性疾病过程有关。外周血EOS检测可辅助诊断过敏性疾病以及监测其治疗后的临床疗效;过敏患儿外周血EOS常达较高水平,且与症状严重程度呈正相关关系[21-22]。TGF-β1被认为是最强的致纤维化因子,能够诱导气道炎症、破坏上皮细胞层、使杯状细胞增生、平滑肌细胞增殖以及促进血管重构,从而调控气道重塑的过程,其表达水平与哮喘严重程度有关[23-25]。
特应性进程是指儿童早期出现的某种特应性疾病往往预示着未来其他特应性疾病的发生。本研究结果提示:对于食物过敏婴儿进行早期规范干预,可能会有助于阻断其特应性进程,包括饮食回避、饮食替代治疗和益生菌补充等综合疗法。目前食物过敏尚缺乏根治办法,公认的办法仍然是饮食回避[26]。2009年MAAS等[27]对有过敏史儿童进行回避过敏原(回避吸入性过敏原及食物过敏原)后发现:该方法能有效推迟哮喘发生。饮食替代治疗包括:母乳喂养者继续母乳喂养,同时母亲回避致敏食物;牛奶蛋白过敏患儿的人工喂养,则用深度水解配方奶粉或氨基酸配方奶粉替代普通配方奶粉;如为其他食物过敏,则回避相关食物。益生菌补充用于防治过敏性疾病尚在研究探讨中,研究[21]显示:益生菌可用于预防湿疹,儿童早期肠道丰富的黏膜相关淋巴组织与大量肠道微生物相互作用有助于儿童免疫耐受达到适宜状态,肠道益生菌群可促进辅助性T细胞1倾向免疫应答,也可促进调节性T细胞发育及分泌抑制性细胞因子。因此对于食物过敏的患儿推荐采用益生菌辅助治疗[28-29]。
在治疗儿童食物过敏的同时,应重视是否存在与其他相关过敏性疾病。本文作者通过前瞻性的队列研究发现:婴儿食物过敏早期干预对其近期的过敏性疾病发生具有预防作用,可以考虑采取饮食回避、饮食替代治疗和益生菌补充等综合疗法对婴儿食物过敏进行早期干预从而阻断其特应性进程。

