超声引导下微波消融治疗特殊部位肝癌的临床观察
孙淑丽,李玉宏,陈菲
(锦州医科大学附属第一医院超声科,辽宁 锦州 121000)
原发性肝癌和肝转移癌是全球最常见的恶性肿瘤之一,每年可发生大量的新发病例和死亡病例,超声引导经皮微波消融由于定位准确,有效热场可调控,目前已成为治疗肝癌的一项重要技术。目前国际及国内专家推荐早期肝癌应首选消融治疗[1-3],但对于特殊部位的肿瘤由于安全范围受限容易引起周边组织器官的损伤,出现并发症。联合介入辅助技术(人工腹水、无水乙醇注射、人工胸水、实时测温等)及超声造影,使得热消融技术的应用范围不断扩大,特殊部位肿瘤的消融治疗应用越来越广泛[4]。本文主要对42个特殊部位肝癌病灶消融治疗效果作回顾性分析。
1 资料与方法
1.1 研究对象 入选标准:(1)病理诊断为肝癌或超声造影、增强MRI及肿瘤标志物检查中至少两项诊断为恶性肿瘤(依据2014年美国放射学会肝癌影像诊断规范);(2)血凝四项及血小板正常;(3)血常规正常,无发热,无胆系感染;(4)原发性肝癌无肝外转移;(5)无脏器功能衰竭(心、肺、肾功能不全)。
40例患者共计42个肿瘤病灶,靠近膈肌9例,肝表面6例,近胃肠12例,近右肾上腺3例,近胆囊3例,近肝门、总胆管5例,近肝静脉及门脉矢状部4例。所有患者临床资料,见表1。
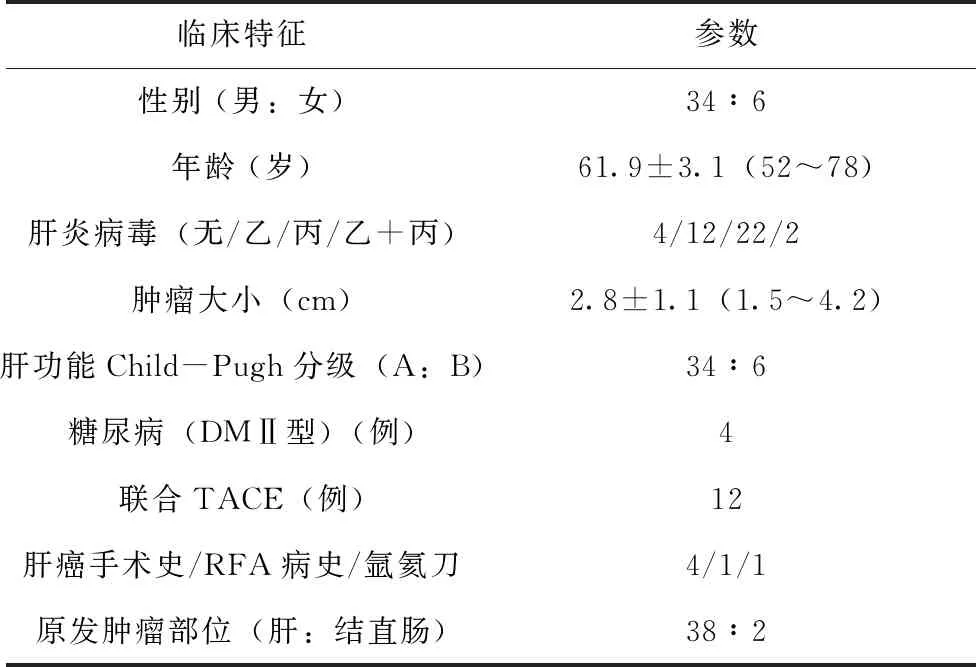
表1 40例患者临床资料
1.2 仪器与方法 使用GE Logiq-E9彩色多普勒超声诊断仪,C1-5探头,频率3.5~5 MHz,配有超声造影软件及穿刺引导装置。超声造影剂为声诺维(Sono Vue,意大利Bracco公司),使用前用5 mL生理盐水溶解,摇匀后形成微泡混悬液,每次造影抽2.4 mL经肘部浅静脉快速团注,后快速推注5 mL生理盐水冲管,同时启动计时器,连续观察5 min。微波仪使用南京康友KY2000微波消融治疗仪(2450 MHz,输出功率10~80 W),连续可调,微波针外径15 G,长度15 cm。消融过程中可实时监测温度。治疗前向病人说明病情并介绍微波治疗的意义及治疗过程可能发生的并发症及应对措施,签署知情同意书。糖尿病人术前血糖控制在8 mmol/L以下,TACE患者均间隔20 d,术前均做超声造影,选择最佳穿刺路径,采用静脉麻醉加局麻。
行人工腹水注水量约200~1000 mL,使膈顶部肿瘤远离膈肌,一边注水,一边消融;肿瘤近肝门、总胆管及肝内大血管侧缓慢注射无水乙醇5 mL,同时布控测温针,用以保护性测温。肿瘤远离危险部位侧微波消融。
消融后1、3、6、12个月进行超声造影、增强MRI,1个月后增强影像检查消融灶内及周边动脉期无异常强化提示为完全消融消融灶内局部动脉期有强化,提示肿瘤残留或消融不完全,治疗3个月后随访期内消融灶内或边缘出现强化区域为肿瘤局部进展[5]。同时检测AFP、肝功能。观察消融后腹腔积液吸收情况及是否出现消融副作用和严重并发症(出血、胃肠穿孔、血气胸、肝脓肿等)等情况。
1.3 统计学方法 应用SPSS 16.0统计学软件进行分析,计数资料用率(%)表示,应用χ2检验,以P<0.05表示差异有统计学意义。
所有患者治疗前均做超声检查,其中直径<3 cm的病灶大部分呈低回声,2例直肠癌转移病灶分别呈混合回声和强回声。超声造影大部分肝脏细胞癌表现为快进快出。42个病灶具体超声表现、造影增强特征及病理学检查,见表2。
42个病灶行人工腹水33个,联合无水乙醇注射9个,治疗后1个月超声造影及增强MRI检查,39个病灶完全坏死,完全消融率92.9%。消融后20 min立刻做超声造影显示3个病灶消融不完全,其1为直肠癌术后肝转移肿瘤明显突出于肝被膜,防止破裂出血,消融范围没覆盖整个瘤体;其余2个为肝脏术后胃体与肝脏及网膜粘连,人工腹水隔离不充分,见图1、2。治疗后所有病例均未出现严重并发症。出现局部疼痛6例,未予处理3 d后消失。治疗后3~10 d腹水均完全消失。其中39个完全坏死灶治疗后3、6、12个月随访结果,见表3。
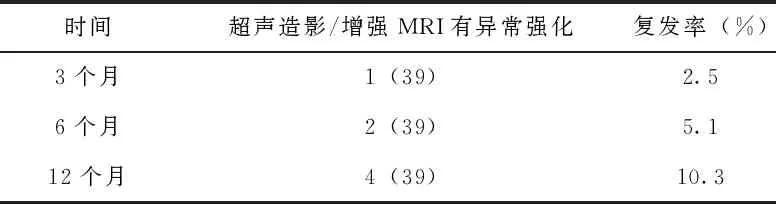
表3 微波消融治疗后随访情况

肝脏左内叶切除术后3年,左外叶肝癌临近胃壁
3 讨 论
目前,肝癌患者不愿意接受手术或存在手术禁忌,超声引导下的微波消融治疗已广泛应用于临床。随着肝癌介入治疗技术不断改进,目前治疗模式已从传统单一的治疗方法逐渐发展成为综合性治疗模式[6]。采用多种介入治疗方法联合治疗肝癌可实现优势互补,弥补单一治疗的不足,准确灭活肿瘤[7]。但特殊解剖部位肿瘤治疗效果易受位置影响,对临近脏器造成热损伤或穿孔等严重并发症[8]。
对于特殊部位肝癌,通过联合其他治疗增加有效性,比如,此研究中微波消融前有12例先行TACE,通过栓塞作用能有效降低肝癌组织的血液供应,使病灶实质疏松,为无水乙醇弥散创造条件[9],而微波消融可灭活TACE术后残存的肿瘤组织,联合应用可收到增加消融体积的效果,产生的热效应可增加肿瘤组织对化疗药物的摄取,同时提高肿瘤组织对化疗药物的敏感性,并增强机体抗肿瘤免疫功能[10]。对于肝门、胆管及大血管旁病灶联合无水酒精利用其热增敏效果同样起到增加消融范围的作用,从而改善临近肝门等重要脏器肿瘤消融不彻底的情况[11],注射无水乙醇可有效提高患者的远期疗效[12];二是利用人工腹水,不但排除胃肠气体干扰使病灶显示更清晰,更重要的是将膈肌、胃肠、肾上腺、胆囊等重要临近脏器隔离开,防止热消融损伤出现严重并发症,利用微波针间断辐射和测温针监控使消融达到安全有效,国外对人工腹水联合射频消融的研究发现人工腹水不会引起热沉效应[13]。
超声造影在特殊部位小肝癌微波消融治疗过程中发挥重要作用[14],肝癌的超声造影在动脉期呈高增强和在延迟期因造影剂廓清呈低增强,这些特征有助于清晰辨别常规超声难以辨别的小肝癌或肝癌局部治疗后的复发灶[15-19]。大量临床研究表明超声造影在对特殊部位肝癌患者的射频或微波消融治疗中可明显减少消融治疗并发症的发生[17,20-21]617-624。因超声造影能明显显示肝癌病灶和判断病灶范围[22],将其应用于常规超声显示困难肝癌的热消融治疗可降低治疗难度,提高疗效[23]。造影可清晰显示肿瘤浸润范围,确认荷瘤血管,为准确制订消融方案和治疗策略,整体灭活肿瘤提供可靠证据[24]。对于常规超声难以清晰显示的病灶,可在实时超声造影引导下进行消融针穿刺。消融后20~30 min微气泡散尽后立刻超声造影,如有不规则增强区(残癌区),马上进行补充消融,达到肿瘤完全坏死,实现在一次治疗中的完全灭活。由于微波消融灶周围组织热灼伤后发生充血水肿反应,即刻造影会出现环状强化带,如延迟期不退出且无增强的范围无扩大,则为正常炎性反应,如延迟期退出则有残留活性。
临近膈肌肿瘤微波消融时,注入人工腹水后,体位关系注水容易流走,需一边注水一边消融。近胆囊区病灶消融时,易发生胆心综合征,需严密观察患者的心律、血压、血氧饱和度等变化,必要时采取对症处理。
本研究由于样本量少,随访时间较短,存在一些局限性,尚需进一步加大样本量多中心临床实践。
综上所述,超声引导经皮微波消融联合超声造影及介入辅助技术治疗特殊部位肝癌具有良好的安全性、准确性和有效性。

