新型冠状病毒数字PCR检测方法建立
李彤 荆福祥 李宏志 邢晓星 赵金银 程迪 曲守方 刘琦★
2019年12月我国出现一种不明原因的肺炎疫情,2020年1月对肺炎患者样本进行测序,发现该肺炎病原体为一种先前未知的新型冠状病毒-严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2,又称新型冠状病毒)[1-2]。SARS-CoV-2是现在已知的第7种可以感染人的冠状病毒。PENG ZHOU和J-F CHAN等[3-4]通过全基因组测序发现SARS-CoV-2全基因组水平有79.5%以上与SRAS-CoV几乎相同,与蝙蝠冠状病毒的同源性达96.0%,且证实与SARS-CoV相同是通过与细胞表面血管紧张素转换酶2(angiotensin converting enzyme 2,ACE2)受体结合方式进入宿主细胞[5]。新型冠状病毒有极强传染性和传播力,临床表现为发热、乏力等全身症状,伴有干咳和呼吸困难等,可迅速发展为重症肺炎、呼吸衰竭、急性呼吸窘迫综合征等。冠状病毒主要通过直接接触分泌物或经气溶胶、飞沫传播[6]。目前主要采用荧光定量PCR技术进行检测,优点是快速且检测结果比较准确[7]。但是目前受到检测样品类型限制,荧光定量PCR对咽拭子样品核酸检测存在一定比例的假阴性,因此在实际检测中对于病原检测的灵敏度和特异性具有更高要求。
数字PCR(Digital PCR,dPCR)技术是一种新的核酸检测和定量方法,与传统定量PCR(Quantitative Real-time PCR,qPCR)技术不同,数字PCR采用绝对定量的方式,不依赖于标准曲线和参照样本,直接检测目标序列的拷贝数[8-9]。由于这种检测方式具有比传统qPCR更加出色的灵敏度、特异性和精确性,数字PCR迅速得到广泛的应用,在极微量核酸样本检测、复杂背景下稀有突变检测和表达量微小差异鉴定方面表现出的优势已被普遍认可。而且其在基因表达研究、microRNA研究、基因组拷贝数鉴定、癌症标志物稀有突变检测、致病微生物鉴定、转基因成分鉴定、高通量测序文库精确定量和结果验证等诸多方面也具有的广阔应用前景,已经受到越来越多的关注[10-12]。
1 材料和方法
1.1 材料
1.1.1 样本
样本RNA来自3例临床诊断为新型冠状病毒肺炎患者核酸RNA提取样本。人基因组RNA,来自于100个正常人的基因组RNA等体积混合而成,由大连晶泰生物技术有限公司提供。新型冠状假病毒质粒合成于生工生物工程(上海)股份有限公司,该假病毒质粒含有完整的Orf1ab基因序列。
1.1.2 试剂与仪器
QIAamp Viral RNA Mini Kit购自德国QIAGEN公司;HiScript IIIReverse Transcriptase逆转录酶购自南京诺唯赞生物科技有限公司;QS 3D DigitalL PCR V2 MMX 1.5ML Kit和QS 3D DQPCR V2 20K CHIP购自美国赛默飞公司。新型冠状病毒2019-nCOV核酸检测试剂盒(荧光PCR法)购自华大生物科技(武汉)有限公司。
数字PCR仪使用Thermo Fisher公司的Quant-StudioTM3D数字PCR系统。荧光定量PCR仪使用上海宏石公司的SLAN-96P荧光定量PCR仪。
1.2 方法
1.2.1 引物和探针的设计与合成
根据已公布新型冠状病毒(SARS-CoV-2)的基因组序列,利用DNAStar和Primer5.0软件设计扩增特异性引物及探针,新型冠状病毒Orf1ab基因上游引物:1AB-F:5′-CAAGGTAAACCTTTGGAATTTG-3′;新型冠状病毒Orf1ab基因下游引物:1AB-R:5′-TTGTCCTCACTGCCGT-3′;新型冠状病毒Orf1ab基因探针:1AB-P:5′-FAM-TGCCACTTCTGCTGCTCTTCAACC-BHQ1-3′。
根据GenBank中登陆的人基因组ACTB基因序列,利用DNAStar和Primer5.0软件设计扩增特异性引物及探针,内参基因ACTB上游引物:ACTB-F:5′-GTCTTCCCCTCCATCGTG-3′;内参基因ACTB下游引物:ACTB-R:5′-GTACTTCAGGGTGAGGATGC-3′;内参基因ACTB探针:ACTB-P:5′-VICAATCCTTCTGACCCATGCCCACC-BHQ2-3′。引物及探针由生工生物工程(上海)股份有限公司合成。
1.2.2 数字PCR反应体系和条件
PCR反应为一步法逆转录聚合酶链扩增法(Reverse Transcription-Polymerase Chain Reaction,RT-PCR)。新型冠状病毒Orf1ab基因上游引物、下游引物、新型冠状病毒Orf1ab探针、ACTB内参基因的上游引物、下游引物、ACTB内参基因探针按照其在数字PCR体系中的浓度分别为450、450、450、450、450、225 nM的最适比例进行混合,配置成20X的引物探针混合液。PCR反应体系为:QuantStudioTM 3D Digital PCR Master Mix v2(2×)7.3μL;新型冠状病毒引物探针混合液(20×)0.7 μL;HiScript III Reverse Transcriptase(200 U/μL)2μL;RNA模板4.5μL。将以上配置好的体系加入到数字PCR芯片中(QμantStμdioTM 3D Digital Chip v2),并用矿物油覆盖芯片,密封好并确保无泄漏。再把芯片放到PCR仪器(例如,ProFlex™PCR System)中,进行PCR反应,PCR反应条件:50℃,50 min;96℃,10 min;57℃,2 min,98℃,30 sec,39个循环;57℃,2 min;10℃保存。使用分析软件:QuantStudio™3D AnalysisSuite™Software对数字PCR反应结果进行分析。
1.2.3 荧光定量PCR反应体系和条件
荧光定量PCR检测使用新型冠状病毒2019-nCOV核酸检测试剂盒(荧光PCR法),反应体系及条件按照说明书要求设置。
1.2.4 准确性和灵敏度试验
新型冠状假病毒质粒合成于上海生工生物,该假病毒质粒含有完整的Orf1ab基因序列。将人基因组RNA、假病毒质粒按照一定比例进行混合分别形成假病毒含量为1×105、1×104、1×103、100、50、25 copies/mL的参考品。将上述的假病毒参考品作为模板进行实验,评价该方法的准确性和灵敏度。根据检测拷贝数和理论拷贝数做标准曲线和线性回归系数R2值。
1.2.5 特异性试验
参照核酸提取试剂盒说明书方法提取猪流行性腹泻病毒PEDV、猪传染性胃肠炎病毒TGEV、风疹病毒RV、甲型流感病毒H1N1的核酸,利用建立的数字PCR检测方法进行扩增,同时提取的健康人样本的核酸做为阴性对照,评价该方法的特异性。
1.2.6 精密度试验
选取50、500 copies/mL浓度水平的参考品分批次重复检测10次,得到重复检测结果,统计浓度对数值的变异系数(CV,%)。
1.2.7 数字PCR检测方法与荧光定量PCR检测方法对比试验
采集确诊的3例临床新型冠状病毒肺炎患者RNA样本,同时利用建立的数字PCR检测方法与新型冠状病毒2019-nCOV核酸检测试剂盒(荧光PCR法)进行检测,分别得到荧光定量PCR结果和数字PCR病原体拷贝数结果。
将人基因组RNA、假病毒质粒按照一定比例进行混合分别形成假病毒含量为500、300、150、100、75和50 copies/mL假病毒参考品。将参考品利用新型冠状病毒2019-nCOV核酸检测试剂盒(荧光PCR法)进行荧光定量PCR检测,其中100、75和50 copies/mL参考品重复检测25次。确定新型冠状病毒2019-nCOV核酸检测试剂盒(荧光PCR法)检测灵敏度,将其结果与数字PCR检测方法比较。
2 结果
2.1 准确性和灵敏度
不同含量假病毒参考品进行数字PCR检测,根据数字PCR检测病毒含量与理论病毒含量进行拟合,其线性回归系数R2为0.998 8,表明在该条件下,新型冠状假病毒的理论值病毒含量和实际检测病毒含量呈现出很好的线性关系,显示建立的数字PCR检测方法具有很好的准确性。见表1。

表1 假病毒参考品准确性的数字PCR检测结果Table 1 Results of accuracy for pseudoviral reference by digital PCR
25次重复实验的结果为50 copies/mL的假病毒参考品23次均能准确检出,而25 copies/mL的假病毒参考品只有3次能准确检出。结果表明新型冠状假病毒数字PCR检测方法的灵敏度为50 copies/mL,见图1。

图1 50 copies/mL假病毒参考品数字PCR检测结果Figure 1 Result of 50 copies/mL pseudoviral reference by digital PCR
2.2 特异性
经序列同源性比对,所选用的引物和探针与其他的人冠状病毒、流感病毒等呼吸道病毒无同源性。对病原体PEDV、TGEV、RV、H1N1的核酸与健康人群核酸样本进行特异性评价,结果均为阴性,显示较好的特异性,见图2。
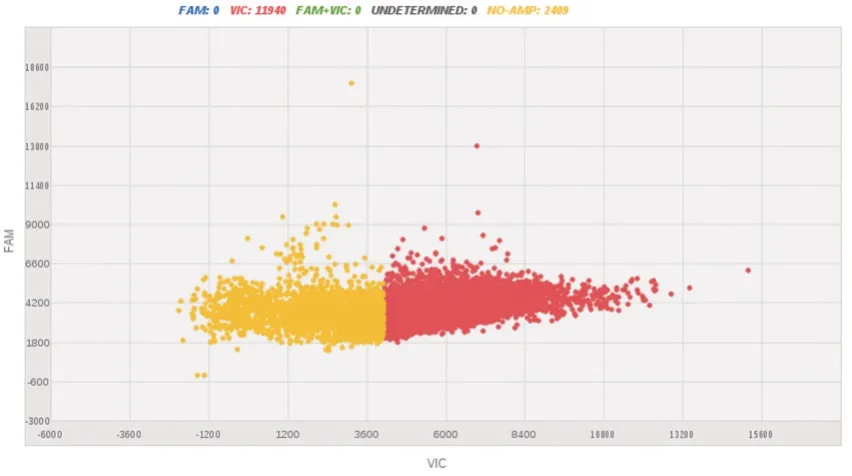
图2 健康人群核酸样本数字PCR检测结果Figure 2 Result of nucleic acid samples from healthy people by digital PCR
2.3 精密度
选取浓度为50、500 copies/mL水平的参考品分批次重复检测10次,根据检测结果统计出浓度对数值的变异系数(CV,%)为5.97%和1.99%,建立的数字PCR方法有良好的精密度。
2.4 两种检测方法对比
采集3例临床新型冠状病毒肺炎患者RNA样本,利用数字PCR检测方法进行检测,结果均为阳性。与国家药品监督管理局已经批准上市的新型冠状病毒2019-nCOV核酸检测试剂盒(荧光PCR法)的检测结果进行平行比较,见表2。
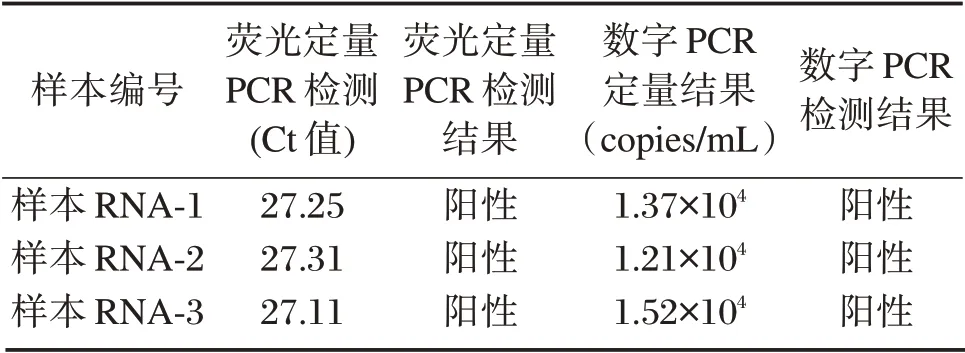
表2 两种方法检测结果比较Table 2 Comparison results of 2 detection methods
检测结果显示2019-nCOV核酸检测试剂盒(荧光PCR法)只能检测到100 copies/mL以上病毒含量的样本,与试剂盒说明说中标注的检测灵敏度一致,见图3。而数字PCR灵敏度和准确性实验结果显示数字PCR检测方法的灵敏度可达到50 copies/mL,高于荧光定量PCR方法的灵敏度(100 copies/mL)。
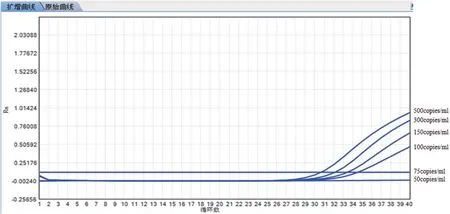
图3 样本RNA-1稀释样本荧光定量PCR检测结果Figure 3 Fluorescence quantitative PCR test results of RNA-1 diluted samples
3 讨论
新型冠状病毒SARS-CoV-2传染性强,临床症状不典型,给临床诊断和疫情防控带来很大困难,快速又精确的诊断对新冠肺炎的防控至关重要。病原学是诊断新型冠状病毒感染的金标准,但由于其存在窗口期、灵敏度低、程序复杂等缺陷,难以在此次疫情中得到广泛应用,而病毒的核酸检测也是确诊COVID-9的金标准,其灵敏度更高。定量检测可以动态检测病毒感染的程度从而观察疗效,因此核酸检测在COVID-9的诊断及疫情的防控中担任不可或缺的角色。而数字PCR技术具有更高的检测灵敏度和准确度,能够更好的满足临床诊断需求。
本研究建立了一种数字PCR检测方法,使逆转录和PCR扩增过程一步完成,减少了开盖污染的风险。选取新型冠状病毒SARS-CoV2的高保守区域Orf1ab基因进行引物与探针设计保证了特异性和准确性,通过实验结果可以看出本研究建立的数字PCR检测方法具有很好的灵敏度、准确性、特异性及临床适用性,可以用于临床新型冠状病毒的快速检测,为新型冠状病毒感染的诊断及流行病学调查提供了有效的工具。
利用3例临床新型冠状病毒肺炎患者RNA样本进行检测,均能准确检出,表明建立的数字PCR检测方法具有较好的临床适用性。与国家药品监督管理局已经批准上市的新型冠状病毒2019-nCOV核酸检测试剂盒(荧光PCR法)检测结果进行平行比较,结果显示建立的数字PCR检测方法具有更高的灵敏度,可以改善现阶段荧光定量PCR法检测试剂盒的假阴性问题。

