改性纤维素纳米微晶增强角蛋白载药膜材料的制备及性能研究*
宋凯利,朱笑吉,朱卫明
(1. 浙江理工大学 生态染整技术教育部工程研究中心,杭州 310018;2. 浙江省清洁染整技术研究重点实验室,浙江 绍兴 312000)
0 引 言
角蛋白优异的生物学特性使得角蛋白膜作为药物载体在伤口敷料、创口愈合材料等领域有突出的应用优势[1-3],作为药物载体膜除了要求具有良好的药物承载和释放能力外,还需具有一定的力学强度,避免使用时材料受到破坏而出现爆发性释放,以期具有稳定的使用性能和良好的药物释放能力[4-6]。角蛋白膜材料强度低,本课题组前期研究发现纤维素纳米微晶可实现对角蛋白材料的力学增强,但会使膜的断裂延伸性能有所下降,这就使得角蛋白膜材料的应用受到限制。这和纤维素纳米微晶与角蛋白基体之间界面结合较弱有关,纳米填料与基体材料之间的界面层作为复合材料一个重要的微结构[7-9],不仅起着连接增强材料与基体的桥梁作用,也是外加负荷从基体向增强材料传递的纽带,因此对复合材料的宏观性能有重要的影响[10-13]。
有研究者为改善纤维素纳米微晶与基体材料之间的界面结合,而对纳米微晶进行改性。如Kim等人采用表面活性剂改变纤维素纳米微晶的极性,从而提高其与疏水基体材料的界面结合[14]。Yu等人采用化学接枝改性来提高纤维素纳米微晶与基质之间的结合力,从而提高复合材料的界面强度[15]。纤维素纳米微晶表面的羟基具有一定的化学反应活性,可通过氧化反应将其氧化生成醛基,而醛基的引入则可赋予纤维素纳米微晶一些特定的反应功能性[16-18]。引入的醛基可与角蛋白分子中氨基发生反应,生成化学交联键,化学交联键的建立有利于提高纤维素纳米微晶与角蛋白基体相之间的界面结合,进而较好地改善复合材料的性能[19-20]。
在研究中,我们采用高碘酸钠氧化法在纤维素纳米微晶表面引入反应性官能团-醛基,得到醛基化纤维素纳米微晶 (DCNC)。系统研究了纤维素纳米微晶的氧化改性,将醛基化纤维素纳米微晶作为增强体制备了角蛋白复合膜,详细研究了复合膜的各项性能,探讨了改性纤维素纳米微晶对复合膜的增强增韧机制。将得到的性能最好的角蛋白复合膜材料为药物载体,研究了其对包覆药物的释放行为。
1 实验部分
1.1 实验材料、药品
纤维素粉:分析纯,上海麦克林生化科技有限公司;硫酸:分析纯,杭州高晶精细化工有限公司;冰醋酸:分析纯,杭州高晶精细化工有限公司;尿素:分析纯,上海麦克林生化科技有限公司;L-半胱氨酸:分析纯,上海阿拉丁生化科技股份有限公司。
1.2 醛基化纤维素纳米微晶的制备
硫酸水解法提取CNC:称取1 g纤维素粉,缓慢加入50 mL 64%(质量分数)的硫酸溶液中,在温度为45 ℃的水浴中水解55 min。反应结束后,将得到的混合液离心,收集离心所得固体产物,水洗4~5次。最后将CNC悬浮液装入截留分子量为5000的透析袋中透析2天。采用高碘酸钠作为氧化剂,在一定的物料比、温度和时间下对纤维素纳米微晶进行氧化改性。之后透析除去未反应的氧化剂。
1.3 角蛋白的制备
称取10 g动物羽毛,溶解在8 mol/L的尿素溶液中,再加入对羽毛质量5%(质量分数)的L-半胱氨酸还原剂,浴比为1∶100,在85 ℃水浴中反应7 h,得到角蛋白悬浮液。将该悬浮液离心,收集上清液,装入透析袋中,用大量去离子水透析2天。用等电点沉降法使角蛋白沉淀,并离心收集固体,冷冻干燥,得到角蛋白固体粉末。
1.4 醛基化纤维纳米微晶增强角蛋白载药膜的制备
称取6 g角蛋白,溶解在94 g体积比为4∶1的醋酸/水溶液,超声脱泡。在角蛋白制膜液中加入角蛋白质量5.0%的丙三醇增塑剂,采用溶液浇铸法制备纯角蛋白膜。改性纤维素纳米微晶/角蛋白复合膜制备如下:将角蛋白溶液与改性纤维素纳米微晶溶液按m(CNC)∶m(Keratin)为1%、2.5%、5%、10%的比例混合,搅拌均匀,倒入聚四氟乙烯制膜板上制膜。
庆大霉素是一种氨基糖苷类的广谱抗生素,对多种阴性菌及阳性菌都具有较强的抑制和杀菌作用,用于小面积伤口处理具有防止伤口感染的效果,本实验采用庆大霉素作为药物模型测试角蛋白复合膜药物缓释性能。选用5.0%∶ DCNC/角蛋白复合膜为载药膜基体材料,药物包覆过程如下:在20 mL 5.0%(质量分数) DCNC/角蛋白制膜液中加入60 mg庆大霉素固体,搅拌溶解后倒入制膜板内待溶剂挥发得到包覆药物的角蛋白复合膜。
1.5 醛基化纤维素纳米微晶的表征
1.5.1 DCNC醛基含量的测定
醛基含量的测定原理为:采用盐酸羟胺溶液与DCNC中醛基反应生成肟,同时生成盐酸产物,使用标准氢氧化钠溶液滴定生成的盐酸,再通过消耗的氢氧化钠体积反推出纤维素纳米微晶上醛基的含量[18]。反应方程式如(1)所示:

(1)
在滴定之前先用标准氢氧化钠溶液 (0.1 mol/L) 将配置好浓度为0.05 mol/L的盐酸羟胺溶液pH值调至5,以除去盐酸羟胺溶液中游离的盐酸。准确称取1 g冻干所得的醛基化纤维素纳米微晶,置于100 mL烧杯中,加入50 mL去离子水,用氢氧化钠溶液将上述悬浮液pH值调至5,之后加入精确体积的40 mL上述pH值为5的盐酸羟胺溶液,在40 ℃下反应4 h,然后用标准氢氧化钠溶液滴定上述反应液至pH值为5,平行做3次,记录每次使用的标准氢氧化钠体积,同时平行做3组空白对照 (使用相同质量的纤维素纳米微晶作为空白组)。
1.5.2 DCNC形貌表征
采用SEM及TEM测试改性纤维素纳米微晶的形貌。
1.6 醛基化纤维素纳米微晶/角蛋白膜的测试与表征
1.6.1 DCNC/角蛋白纳米复合膜的力学性能测试
将复合膜放在温度为25 ℃,湿度为65%的环境下平衡24 h。然后用Instron3367万能材料试验机测试复合膜的拉伸性能,设定仪器参数为:夹距20 mm,拉伸速度20 mm/min。
1.6.2 DCNC/角蛋白纳米复合膜耐水性能测试
将CNC/角蛋白复合膜放入烘箱干燥,称重记为m1。在室温下浸入超纯水中3天,取出后烘箱烘干,称量记为m2,按式(2)计算其质量溶失率:
(2)
1.6.3 DCNC/角蛋白纳米复合膜药物释放性能测试
将制备的角蛋白载药膜材料置于含50 mL不同pH值缓冲液的锥形瓶中,放在37 ℃的恒温振荡箱中在30 r/min下振荡,间隔一定时间用移液枪取出3 mL溶液,同时补加3 mL缓冲液 (采用pH值为3和5的0.1 mol/L柠檬酸-柠檬酸钠缓冲液以及pH值为7.4的0.1 mol/L PBS磷酸盐缓冲液)。采用紫外可见分光光度计测定溶液中庆大霉素的含量,庆大霉素可与邻苯二甲醛试剂发生衍生反应,反应物在332 nm处具有特性吸收,因此可通过紫外可见分光光度计检测衍生物吸光度,绘制标准曲线计算庆大霉素含量。
2 结果与讨论
2.1 DCNC的制备及表征
高碘酸钠氧化纤维素是一种具有选择性且副反应较少的氧化反应。纤维素分子中C6位羟基上的氢原子很容易与相邻葡糖糖单元中氧原子形成氢键结合,而高碘酸钠则主要进攻葡萄糖单元上的C2-C3位仲羟基,将其氧化为醛基。反应过程示意图如图1所示。

图1 醛基化纤维素纳米微晶制备过程图Fig 1 Schematic illustrate the preparation of dialdehyde cellulose nanocrystal
氧化条件主要影响DCNC上醛基含量及其制备产率。图2为不同反应条件对醛基化纤维素纳米微晶上醛基含量和产率的影响。图2(a)为高碘酸钠与纤维素纳米微晶的质量比对所得DCNC上醛基含量和产率的影响,随着氧化剂用量的增加,所得醛基化纤维素纳米微晶上醛基含量逐渐增加,直至氧化剂用量为微晶质量的1.5 倍时微晶上醛基含量达到最大值。醛基化微晶的产率则随着氧化剂用量的增加呈现逐渐下降的趋势,这是由于高碘酸钠在氧化也会造成纤维素的氧化降解,造成醛基化纤维素纳米微晶产率的下降。图2(b)为反应温度对醛基含量和产率的影响,随着反应温度由30 ℃升高至50 ℃时,醛基含量由1.6 mmol/g增加至2.7 mmol/g。从图2(c)可知,氧化剂与微晶质量比为1∶1,反应温度在40 ℃,反应时间为2 h的条件下,所得产物醛基含量为2.1 mmol/g,产率为78%。
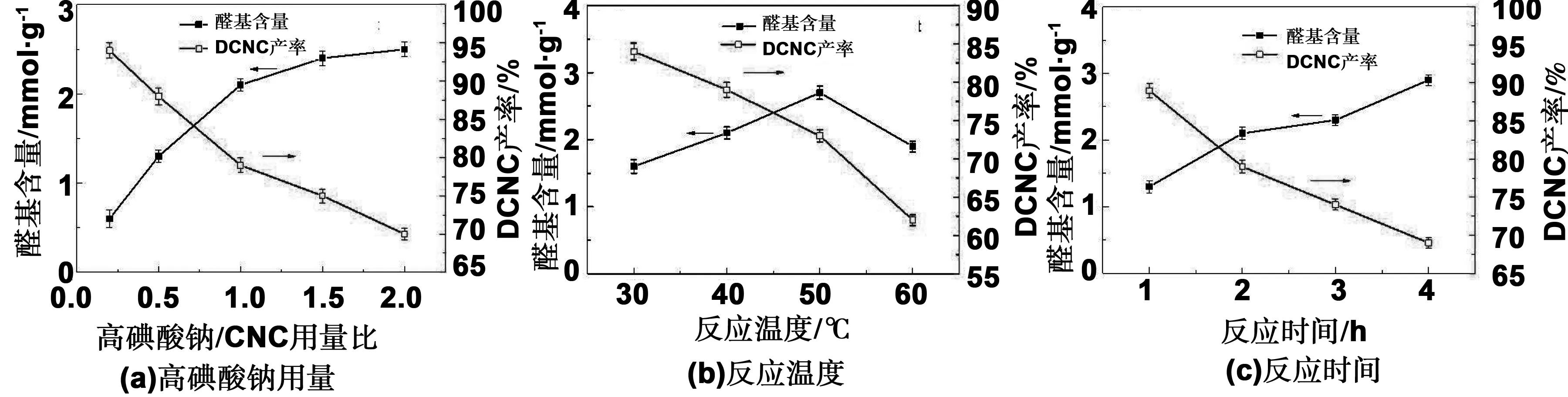
图2 高碘酸钠用量,反应温度及反应时间对醛基化纤维素纳米微晶上醛基含量及产率的影响Fig 2 Effect of NaIO4 dosage, temperature and reaction time on aldehyde content and yield of dialdehyde cellulose nanocrystal
采用FT-IR对醛基化纤维素纳米微晶进行结构表征,结果如图3所示。未改性的纤维素纳米微晶呈现典型的纤维素红外特征谱图,对比醛基化纤维素纳米微晶的红外谱图,其吸收峰的位置和强度基本上没有发生变化,只是在1 732 cm-1处出现了新峰,该峰为醛基的特征吸收峰,说明高碘酸钠氧化后成功在纤维素纳米微晶上引入了醛基。
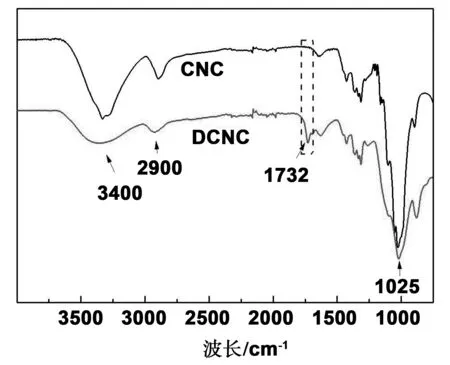
图3 醛基化纤维素纳米微晶的红外谱图Fig 3 FT-IR spectra of dialdehyde cellulose nanocrystal
图4为所得醛基化纤维素纳米微晶的形貌及粒径分布图。从图4(a)可知,DCNC形貌呈现典型的棒状形态,由于冻干所得纤维团聚现象较为严重,不能清晰观察单根纤维的形貌,因此采用透射电子显微镜对醛基化纤维素纳米微晶进行形貌表征,如图4(b)所示。醛基化纤维素纳米微晶为棒状或针状形貌。如图4(c)所示,所得醛基化纤维素纳米微晶的平均粒径在187 nm左右,其悬浮液如插图所示呈现乳白色。

图4 醛基化纤维素纳米微晶的FE-SEM,TEM 图以及粒径大小分布图 (插图为醛基化纤维素纳米微晶悬浮液照片)Fig 4 FE-SEM micrograph, TEM micrograph and particle size distribution of DCNC determined by dynamic light scattering (inset: digital graph of DCNCs suspension)
2.2 DCNC/角蛋白复合膜的制备及性能
醛基化纤维素纳米微晶增强角蛋白基复合材料的制备如图5所示。角蛋白制膜中加入相对于角蛋白质量的1.0%,2.5%,5.0%以及10.0%的醛基化纤维素纳米微晶,超声分散均匀后在聚四氟乙烯基板上制膜,待溶剂挥发完全之后,在80 ℃的烘箱中加热1.5 h以促进醛基与角蛋白分子上氨基之间的反应,在醛基化纤维素纳米微晶与角蛋白之间建立化学键结合。

图5 醛基化纤维素纳米微晶增强角蛋白复合膜的制备流程图Fig 5 Schematic plot of the preparation process of dialdehyde cellulose nanocrystal reinforced keratin nanocomposites
通过添加醛基化纤维素纳米微晶来改善材料力学性能,因此测试了复合材料的断裂强力及断裂延伸性能,结果如图6所示。从图中可知未添加DCNC的纯角蛋白膜的力学性能较差,断裂强力和断裂延伸均较低,其断裂强力只有2.7 MPa,断裂延伸为11.0%。与纯角蛋白膜相比,添加DCNC之后复合膜的断裂强力均有较大的增加,DCNC添加量为1.0%时复合膜的断裂强力提高至8.5 MPa,且随着DCNC添加量增加复合膜的断裂强力大大增加,直到添加量为5.0%时,复合膜的断裂强力达到最大值为23.5 MPa,再继续增加DCNC的用量后复合膜的断裂强力出现下降趋势。DCNC的添加较好的改善了角蛋白复合膜的断裂强力,与CNC相比,DCNC的添加对复合材料的力学性能改善效果较为理想。
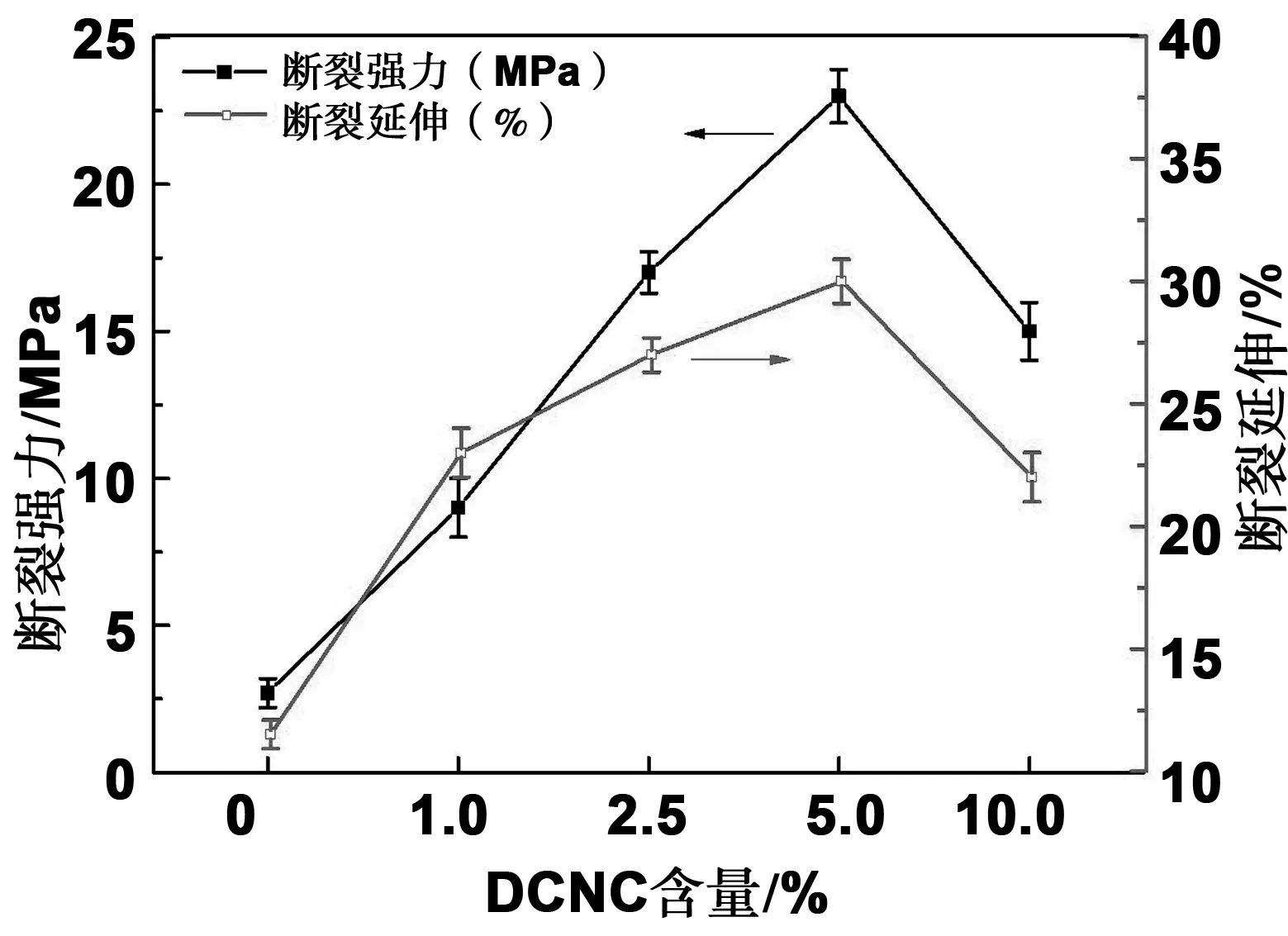
图6 醛基化纤维素纳米微晶增强角蛋白复合膜的力学性能Fig 6 Mechanical properties of dialdehyde cellulose nanocrystal reinforced keratin nanocomposites
图7为DCNC/角蛋白复合膜材料动态力学性能测试结果。图7(a)为DCNC/角蛋白复合材料的贮能模量随温度的变化趋势,随着温度的升高复合材料的贮能模量在100 ℃附近开始出现下降趋势,此温度范围为材料的玻璃化区域,材料的贮能模量在此温度范围内达到最大值,温度低于材料的玻璃化转变温度时材料处于橡胶态,材料的贮能模量较小。添加不同量的DCNC后复合材料的贮能模量呈现增加趋势,这与上述复合材料断裂强力变化趋势类似。复合材料贮能模量的增加,可能是由以下原因导致:(1)纤维素纳米微晶本身具有较高的模量,因此作为复合材料的增强相能够大大改善材料的力学性能,使得角蛋白复合材料的贮能模量也大大提高;(2)醛基化改性的纤维素纳米微晶与角蛋白发生交联反应,在纤维素纳米微晶与角蛋白之间建立了化学键的结合,化学键的建立大大提高了增强相与基质相之间的界面作用力,因此,使得两相之间界面强度大大提高。在DCNC本身的增强效果与强界面作用力的共同作用下,复合材料的力学性能得到了较为理想的改善效果,因此使得复合材料的贮能模量增加。
图7(b)为DCNC/角蛋白复合材料损耗因子随温度的变化趋势。从图中可以看出添加DCNC之后复合材料的tanδ波峰向高温方向发生移动。材料tanδ曲线的波峰表示材料的玻璃化转变温度Tg,添加DCNC之后一方面可与角蛋白分子链之间相互缠结,使得分子链的运动阻力增加,自由移动变得困难;另一方面DCNC与角蛋白分子之间交联键的建立,也使得角蛋白大分子链的自由移动阻力增加,这两方面的原因造成复合材料玻璃化转变温度Tg的提高。
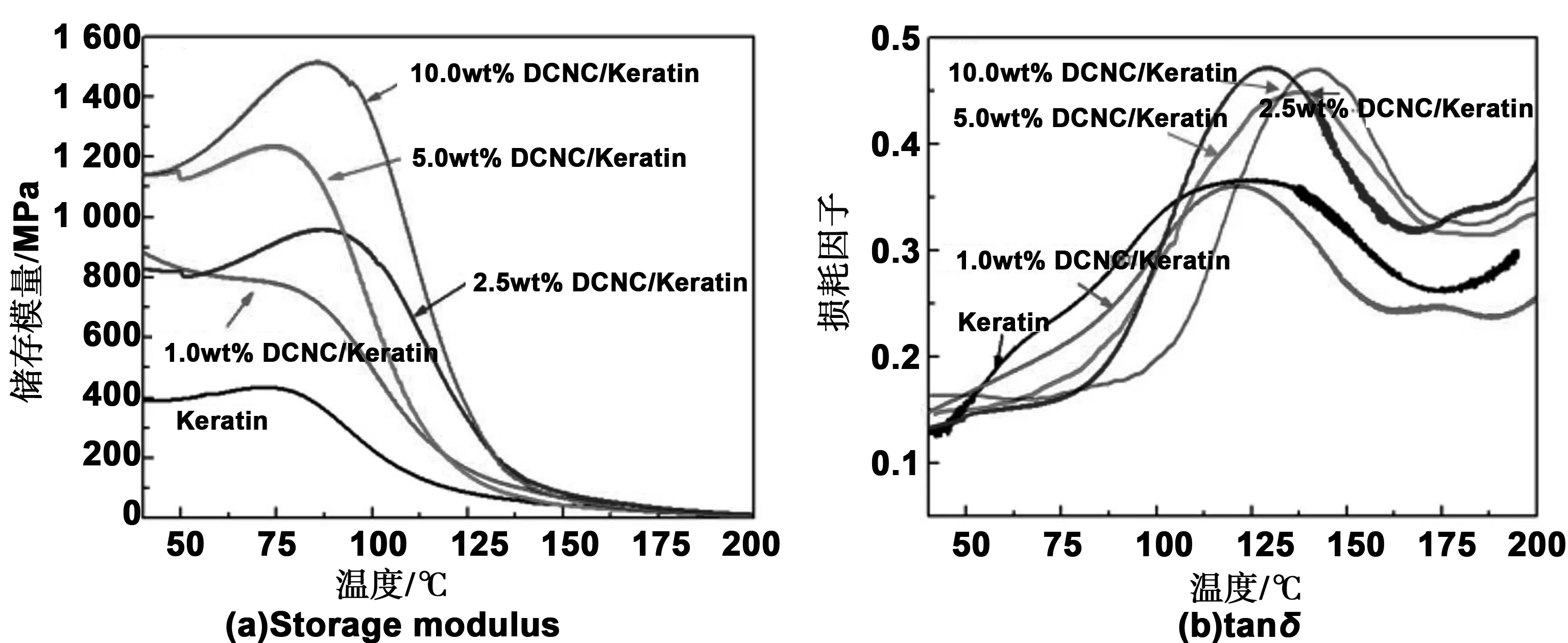
图7 醛基化纤维素纳米微晶增强角蛋白复合膜的动态力学性能Fig 7 Dynamic mechanical thermal analysis of dialdehyde cellulose nanocrystal reinforced keratin nanocomposites
2.3 DCNC/角蛋白复合膜药物缓释性能研究
通过以上研究可知,采用DCNC增强可使得角蛋白膜材料的性能得到较好的改善,采用5.0%(质量分数)DCNC增强的角蛋白复合膜为载药材料,与纯角蛋白膜材料进行对比,以硫酸庆大霉素为药物模型,研究了角蛋白基膜材料作为药物缓释载体的应用性能,结果如图8所示。图8(a)~(c)分别为角蛋白基膜材料在pH值为3、5和7.4的缓冲液中随时间变化的累积药物释放率。从3张图中可知,纯角蛋白膜对药物均呈现爆发性释放,说明纯角蛋白膜材料对包覆的药物没有持续缓释的效果,这是因为角蛋白膜材料性能较差,在使用过程中容易发生破坏而使包覆的药物突释。这种药物释放规律的膜材料不能满足作为伤口敷料材料对伤口持续给药的要求。DCNC/角蛋白复合膜对包覆的药物在60 h后仍有药物释放,说明复合膜材料能使包覆的药物缓释,在伤口敷料材料等领域具有潜在应用价值。

图8 角蛋白膜材料在不同pH值条件下对包覆药物的释放性能Fig 8 Drug release profile of keratin films at different pH solution
3 结 论
本研究通过在纤维素纳米微晶上引入反应性醛基官能团,利用醛基与角蛋白氨基之间建立化学键结合,来改善纤维素纳米微晶与角蛋白之间的界面作用力。制备了一种力学性能较好的角蛋白复合膜材料,并且研究了复合膜材料作为药物载体的使用性能。研究表明,高碘酸钠与微晶质量比为1∶1,反应温度为40 ℃,反应时间为2 h条件下所得醛基化纤维素纳米微晶的醛基含量为2.1 mmol/g,产率为78%。TEM证明改性纤维素纳米微晶的形貌为针状,FT-IR证明氧化改性没有破坏纤维素微晶的化学结构。当DCNC的添加量为5.0%时复合膜的断裂强力可由2.3 MPa提高到23.5 MPa,断裂延伸由11.0%提高至30.0%。 且DCNC增强的角蛋白复合膜对药物呈现缓慢释放的规律,DCNC/角蛋白复合膜在50 h后仍有药物释放,说明该复合膜材料具有较好的缓释性。这种药物释放规律的载药材料较适合作为伤口敷料材料应用。

