肠系膜脂肪代谢异常的CT 诊断及其分型
黄 越 徐学权 王利敏 杜 斌 胥广贺
肠系膜脂肪代谢异常(mesenteric fatty metabolic abnormality)既往认为是少见疾病,发病率低,临床症状不典型,易被忽视,但随着肥胖人群增多,其发病率增高。对于该病的相关文献报道增多,近年来该病逐渐被临床及影像医生所重视。本文旨在通过分析我院81例肠系膜脂肪代谢异常患者的CT表现,提高诊断准确率,并依据影像表现对其分型,为后期临床合理治疗提供有效帮助。
方 法
1.临床资料
收集我院2013 年至今经影像及临床诊断的肠系膜脂肪代谢异常患者81例,其中男性42例,女性39例,年龄22 ~87岁,平均59.35±14.28岁。患者临床症状表现轻重不一,轻者多为慢性持续性腹痛,无血便或排便异常,无肠梗阻等症状,常规服药症状无明显改善,部分症状严重者可扪及腹部肿块。
2.检查方法
所有患者均进行CT 检查, 检查设备为SIEMENS SOMATOM Perspective CT、GE lightspeed VCT 以 及PHILIPS Brilliance iCT,均采用螺旋扫描模式,层厚1.25mm,重建间隔1.25mm,pitch 1.375,管电压120 ~140kV,管电流250 ~350mA,FOV 30 ~35cm,采用腹窗显示,扫描范围自膈顶层面到耻骨联合上缘,包括全腹腔脏器。增强扫描均行三期模式,包括动脉期、门脉期及延迟期,Nemoto 高压注射器,注射流率3.5ml/s,注射剂量75 ~80ml,对比剂为北陆药业碘海醇350注射液,经肘正中静脉注入。采集原始轴位数据后,传至随机所带的ADW4.3、ADW4.5、ADW4.7 或EBW2.5 工作站,进行最大密度投影(MIP)及多平面重组(MPR),选择最佳成像角度,观察图像包括冠状位及斜矢状位,最大限度使病灶显示清楚,利于诊断,并由两名以上的高年资医师进行影像分析。
结 果
1.病变部位及其分型

图1 Ⅰ型肠系膜脂肪营养不良。A.轴位CT 图像,显示围绕血管分布的同心圆样磨玻璃影,相互间存在正常脂肪组织。B.冠状位图像,肠系膜血管显示清楚。为原始轴位图像,可见典型的“靶征”及增厚水肿的肠壁。
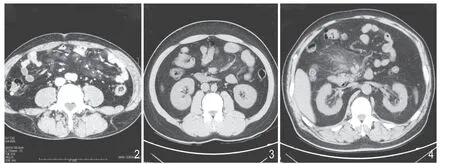
图2 Ⅰ型肠系膜脂肪营养不良。分布范围较前一患者广泛,但未连成片。图3 Ⅱ型肠系膜脂膜炎。左半区肠系膜可见呈片状分布的磨玻璃影,病变区域内无正常脂肪组织出现。图4 Ⅱ型肠系膜脂膜炎。右半区肠系膜病变内可见索条,外缘见线样分界。
肠系膜的解剖分布为扇形分布,其扇轴位置是腹主动脉及其分支,扇面远端附着于结肠及小肠系膜,因此病变分布区域分为扇轴及扇面两处。在81例患者中,其中45例分布于肠系膜根部,即扇轴,病变围绕肠系膜上动脉或肠系膜下动脉呈圆形或片状分布;36例分布于扇面的各个部位,病灶亦呈圆形或片状分布。根据病变的表现形式及严重程度,将肠系膜脂肪代谢异常分为三型,即Ⅰ型肠系膜脂肪营养不良,Ⅱ型肠系膜脂膜炎及Ⅲ型回缩性脂膜炎,其中Ⅰ型肠系膜脂肪营养不良患者58例,Ⅱ型肠系膜脂膜炎患者19例,Ⅲ型回缩性脂膜炎患者4例。
2.肠系膜脂肪代谢异常的CT 表现
把患者的CT 原始轴位扫描数据传至随机所带的ADW 系列及EBW 工作站进行系统分析,肠系膜脂肪营养不良表现为肠系膜血管根部局限的、呈靶环样或同心圆样分布的磨玻璃影,病灶围绕肠系膜血管向外放散,病灶与病灶间可见正常的肠系膜脂肪组织,增强后病灶区域无明显强化(图1、2);肠系膜脂膜炎其范围较肠系膜脂肪营养不良大,病灶分布多呈片状分布,病变区域内无正常脂肪组织出现,其内可见长索条,病变区域与远处正常脂肪组织间存在明显的分界线,病变区域的磨玻璃密度较肠系膜脂肪营养不良更高,增强后病变区域血管显示清晰,但无狭窄无变形,病灶远端分界线呈索条样强化(图3、4);回缩性脂膜炎多呈包裹态,病灶区域有明显的界限,外缘可见类似的假包膜,多为线样高密度索条,病变区域内肠管及肠系膜血管包裹明显,扭曲变形,系膜组织回缩,严重者可见假包块形成,增强后包块呈不均匀性的轻度强化(图5、6)。
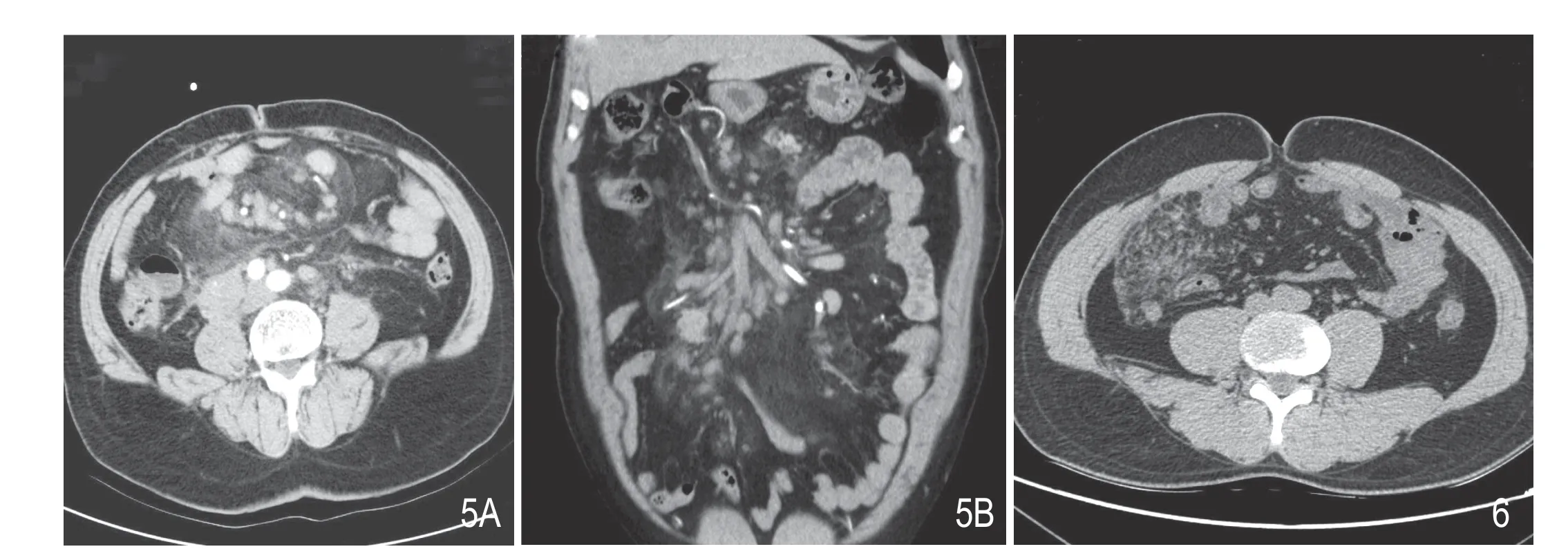
图5 Ⅲ型回缩性脂膜炎。病变区域多呈包裹态,与邻近组织有明显的界限,外缘可见线样高密度索条形成的假包膜,血管根部受包绕,内见增大的淋巴结。图6 Ⅲ型回缩性脂膜炎。病变区域内肠管及肠系膜血管分布杂乱,扭曲变形,系膜组织回缩增厚。
讨 论
1.肠系膜脂肪代谢异常的病理改变及分型
肠系膜脂肪代谢异常属于一组疾病的总称,是肠系膜脂肪组织的一种非特异性炎症,最早出现于Durst 等的文章中,起初命名为回缩性肠系膜炎[1]。1955 年Crane 等首先报道该病病理表现为肠系膜脂肪组织内大量巨噬细胞浸润,因此将其称为孤立性脂肪代谢障碍。随着对该病的逐渐认识,国内对于该病存在多种称谓,如肠系膜脂肪肥厚症、肠系膜脂性肉芽肿、原发性肠系膜脂硬化症、缩窄性肠系膜炎、特发性收缩性肠系膜炎、硬化性肠系膜炎等[2],但以上每个称谓其病理表现却不尽相同,其病理变化从最初的脂肪组织内大量巨噬细胞浸润,发展成炎性细胞大量聚集,继而细胞间出现纤维组织,大量纤维组织聚集,脂肪细胞坏死、萎缩,最后大量纤维组织收缩形成包裹硬化。而最新研究认为不同的病理时期,该病的名称也应不同,当病变位于较早阶段时,由于只是由大量的巨噬细胞吞噬脂肪细胞,尚未引起明显的炎症反应,病理以脂肪细胞坏死为主,该阶段应称为肠系膜脂肪营养不良,属于Ⅰ型;而当病变进一步发展时,肠系膜脂肪间出现大量炎性细胞聚集时,此时病理以炎性细胞聚集为主,掺杂脂肪细胞坏死,病灶边缘出现纤维组织,该阶段应称为肠系膜脂膜炎,属于Ⅱ型;随着病变进一步加剧,炎症及脂肪细胞坏死增多,瘢痕纤维组织成为该阶段主要的病理改变,纤维组织收缩加剧,最终形成包裹硬化,外观呈蚕茧样,此阶段应称为回缩性脂膜炎,属于Ⅲ型。不同的病理时期,名称应有所区别,所表现的影像学改变也各不相同,因此不应用统一称谓代替[3-6]。
2.肠系膜脂肪代谢异常不同阶段的CT 表现
肠系膜脂肪代谢异常患者进行CT 检查时,均可见腹腔内脂肪组织多于正常人群,这是其发生背景,而且腹腔内脂肪组织越多其发病率越高。肠系膜脂肪营养不良属于早期改变,病理改变以巨噬细胞增多为主,合并脂肪细胞坏死,因此表现为肠系膜血管根部原本正常的脂肪密度增高,代之以局限的呈靶环样或同心圆样分布的磨玻璃影,病灶围绕肠系膜血管向外放散,病灶与病灶间可见正常的肠系膜脂肪组织将其分隔,增强后病灶区域无明显强化,该阶段脂肪细胞坏死多于炎细胞浸润及纤维增生;肠系膜脂膜炎属于病变的中间阶段,该阶段以炎细胞浸润为主,含有少量的脂肪细胞坏死和纤维增生,因此CT 表现其范围较肠系膜脂肪营养不良增大,病灶分布多呈片状分布,病变区域内无正常脂肪组织出现,脂肪密度被磨玻璃影取代,其内可见长索条,但病变区域与远处正常脂肪组织间存在明显的分界线,病变区域的磨玻璃密度较肠系膜脂肪营养不良更高,增强后病变区域血管显示清晰,但无狭窄无变形,病灶远端分界线呈细线样强化[7-9];回缩性脂膜炎属于肠系膜脂肪代谢异常的终末期,该阶段病变以纤维增生为主,因此病变区域多呈包裹态,与邻近组织有明显的界限,外缘可见类似的假包膜,多为线样高密度索条,病变区域内可见淋巴结增大,肠管及肠系膜血管包裹明显,分布杂乱,扭曲变形,系膜组织回缩增厚,严重者可形成假包块,增强后包块呈不均匀性的轻度强化[10-13]。
3. 肠系膜脂肪代谢异常不同阶段的治疗及预后
肠系膜脂肪营养不良的患者临床表现轻微,属于自限性疾病,可以通过合理饮食及体质锻炼,提高机体抵抗力,消耗掉腹腔内过多堆积的脂肪组织后,临床症状短期内会消失,影像表现恢复正常,一般不需要进行额外的临床干预。对于肠系膜脂膜炎的患者,症状严重者可以给予肾上腺皮质激素、抗生素及三苯氧胺综合治疗,症状可得到有效控制。而对于回缩性脂膜炎患者当发生肠梗阻及血管压迫症状时,可进行外科手术治疗。
总之,肠系膜脂肪代谢异常具有自限性,预后佳,通常2 年内,大多数病人的疼痛可消失及肿块退缩。

