可光助再生二氧化钛/层状双氢氧化物去除水体中有机染料
胡京宇,姚戎,潘玉航,朱超,宋爽,沈意
(浙江工业大学环境学院,浙江杭州310032)
引 言
吸附法作为一种传统的水处理方法,已被广泛应用于各种水污染处理工艺中[1-2],但是吸附剂的再生难题一直是限制该方法进一步发展的技术瓶颈[3]。一般情况下,吸附剂的再生主要通过高温挥发和酸性脱附,往往再生效率不高,且容易造成能源浪费和二次污染[4]。因此,开发一种吸附和光催化双功能的复合材料,可同时实现污染物的去除及吸附剂的再生,是值得探索的研究方向。其可以在不添加任何有毒有害化学物质的情况下,仅利用光源甚至是太阳光的情况下氧化降解(矿化)水中有机污染物[5]。
在之前的研究报道中,多将碳基吸附剂(活性炭[6-7]、多壁碳纳米管[8-9]等)和常见光催化剂(TiO2[10-11]、ZnO[12-13]等)组合,来实现水中污染物的吸附及光催化去除。然而,碳基材料作为光催化剂的基底,在光催化降解过程中由于活性氧的攻击会发生自身的逐渐氧化,间接造成了吸附能力的降低和光催化剂的脱落[14]。因此,选择一种抗氧化,同时兼具高吸附容量和快速吸附动力学的吸附剂作为基底,是实现吸附和光催化双功能复合材料开发的关键。
层状双氢氧化物(LDHs)是一种由水镁石层和层间的阴离子及水分子相互交叠而成的层状黏土[15],因其具有大比表面积、高离子交换能力和可控的夹层空间,可以通过吸附方式有效地捕捉离子型有 机 分 子(NO3-LDH,甲 基 橙,qe=148 mg/g[16];MgZnAl-LDH,2,4-二氯苯氧乙酸,qe=395 mg/g[17];NO3-LDH,2-甲基-4-氯苯氧基乙酸,qe=243 mg/g[18])。同时,利用LDHs 材料的化学稳定性、抗氧化性和高透光性,TiO2负载的LDH 复合材料也被开发用于增强光催化还原CO2能力的研究[19]。然而,利用TiO2负载的LDH 复合材料吸附去除水中有机污染物及材料自身通过光助再生的研究还没有被报道。
因此,本研究开发了一种将TiO2颗粒负载在镁铝-层状双氢氧化物(MgAl-LDH)的TiO2/LDH 复合材料,保留了LDH 原始的层状结构,用于吸附及光助再生循环去除水中两种代表性的有机污染物:甲基橙(有机阴离子染料)和亚甲基蓝(有机阳离子染料)。通过等温吸附模型和动力学模型比较LDH 和TiO2/LDH 的吸附性能,通过再生率评价材料的光助再生性能。本文可为水中有机污染物去除提供可行的节能高效方法,为吸附-光催化双功能复合材料设计和优化提供针对性的策略。
1 材料与方法
1.1 实验材料
六 水 硝 酸 镁(Mg(NO3)2·6H2O)、九 水 硝 酸 铝(Al(NO3)3·9H2O)、碳酰胺购自上海阿拉丁试剂公司。二氧化钛(TiO2;锐钛矿∶金红石=8∶2;带隙为3.1~3.3 eV)购自北京百灵威科技有限公司。实验所用试剂均为分析纯,未经纯化直接使用。
1.2 吸附剂制备
1.2.1 LDH 的制备 采用典型的尿素水解法水热合成LDH(CO32-作为LDH 的夹层阴离子)。具体的操作步骤如下:在室温下,将1.20 g Mg(NO3)2·6H2O、0.88 g Al(NO3)3·9H2O 和1.31 g 碳酰胺在70 ml 去离子水中溶解,搅拌30 min 形成透明溶液。将已制得的混合溶液置于100 ml 聚四氟乙烯高压反应釜中,于140℃烘箱中反应24 h 后,依次用乙醇和水洗数次烘干得到LDH粉末。
1.2.2 TiO2/LDH 的制备 TiO2/LDH 的合成在上述70 ml 的透明溶液的基础上加入0.09 g TiO2超声分散1 h。将制得的混合溶液置于100 ml 聚四氟乙烯高压反应釜中,于140℃烘箱中反应24 h 后,依次用乙醇和水洗数次烘干得到TiO2/LDH粉末。
1.3 吸附剂表征
吸附剂中TiO2负载量采用美国Perkin Elmer 公司的Optima 5300DV 电感耦合等离子体发射光谱仪(ICP-OES)进行分析。X 射线衍射(XRD)测试采用美国Thermo 公司的ARL SCINTAG X’TRA 型XRD仪,Cu 靶Kα辐射,工作电流和电压分别为40 mA 和45 kV。吸附剂的微观结构采用美国FEI 公司的Tecnai G2 F-30 型透射电子显微镜(TEM),其加速电压为300 kV,分辨率为0.2 nm。 采用美国Micromeritics 公司的ASAP 2010 比表面和孔径分布测定仪(BET)测定材料比表面积及孔径分布。
1.4 吸附实验
1.4.1 等温吸附实验 分别量取100 ml 浓度梯度为0~20 mg/L 的亚甲基蓝和浓度梯度为0~60 mg/L的甲基橙于250 ml 具塞锥形瓶中,再准确称量1.0 mg的吸附剂分别加入锥形瓶中,置于25℃避光恒温摇床中以120 r/min 振荡吸附。4 h 后取样,通过微孔滤膜后,用双光束紫外可见分光光度计(Persee T6-1650E)测量吸附后溶液中染料的残留浓度Ct。吸附量计算公式为

式中,qt为t时间的吸附量,mg/g;m为吸附剂的质量,mg;C0为染料溶液的初始浓度,mg/L;Ct为吸附t时间时溶液中染料的浓度,mg/L;V为溶液体积,ml。
采用等温吸附模型对吸附数据进行模型拟合分析,考察吸附剂与吸附质之间的相互作用关系。Langmuir 模型假设吸附剂表面均一,各处的吸附能相同,其表达式为

式中,Ce为平衡质量浓度,mg/L;qe为平衡吸附量,mg/g;qm为理论饱和吸附量,mg/g;KL为吸附常数,L/g。
Freundlich 模型假设吸附剂表面活性位点的分布是不均匀的,亲和力强的位点先被占据,可以进行多层吸附,其表达式为

式中,Ce为平衡质量浓度,mg/L;qe为平衡吸附量,mg/g;Kf和N为吸附常数。
1.4.2 动力学吸附实验 分别量取100 ml 5 mg/L的亚甲基蓝和20 mg/L 的甲基橙于250 ml 具塞锥形瓶中,再准确称量1.0 mg 的吸附剂分别加入锥形瓶中,置于25℃避光恒温摇床中以120 r/min 振荡吸附。在一定时间取样,通过微孔滤膜后,测量溶液中染料的残留浓度Ct。采用拟一级动力学模型和拟二级动力学模型对吸附过程进行分析。拟一级动力学方程表达式为
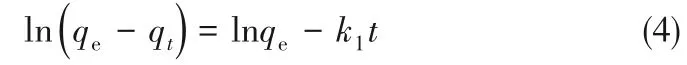
式中,k1为拟一级速率常数,1/s;qe为平衡吸附量,mg/g;qt为t时间点的吸附量,mg/g。
拟二级动力学方程表达式为

式中,k2为拟二级速率常数,g/(mg·s);qe为平衡吸附量,mg/g;qt为t时间点的吸附量,mg/g。
1.5 吸附-再生实验
1.5.1 预吸附实验 在200 ml 反应液中,目标污染物为甲基橙(初始浓度为100 mg/L)和亚甲基蓝(初始浓度为50 mg/L),加入吸附剂粉末0.02 g。在暗态下振荡4 h,达到吸附解析平衡后抽滤并用去离子水洗涤去除表面残留的染料,制备达到吸附饱和的吸附剂(即达到其最大吸附容量的材料)。为确保吸附剂达到饱和吸附量,在预吸附后,再进行一轮低浓度(甲基橙,20 mg/L;亚甲基蓝,10 mg/L)的吸附验证实验。吸附前后,溶液浓度保持不变,证明吸附剂的吸附位点基本都被染料占据。
1.5.2 光助再生实验 将15 mg 预吸附材料分散在15 ml 去离子水中,用磁力搅拌器搅拌,通过低压汞灯(16 mW/cm2)辐射样品溶液。在一定时间取出定量悬浊液,用15 ml 1 mol/L 的盐酸酸化解析悬浊液样品中残留的染料(酸化后对LDH 的溶解度可以忽略不计)。通过微孔滤膜后,检测上清液中染料的浓度,通过获得不同辐照时间后复合材料吸附中染料的残留量来估算通过光催化降解后可用吸附位点百分比,评估复合材料的光助再生动力学。材料再生动力学恢复率计算方程表达式为

式中,Rt为t时间的恢复率;qm为材料的饱和吸附量,mg/g;q't为光催化t小时后染料残留量,mg/g。
同时通过循环再生实验,评估材料的稳定性。材料再生率计算方程表达式为

式中,Rn为再生率;q'n为材料循环n次后的饱和吸附量,mg/g。
2 结果与讨论
2.1 材料表征
2.1.1 电感耦合等离子体发射光谱仪 将TiO2/LDH 消解后,采用ICP-OES 检测钛元素的含量,结果如表1 所示:测得TiO2在LDH 吸附剂上的负载量在2.25%~2.35%(质量)之间,平均负载量为2.29%(质量),与理论负载量(2.59%(质量))相差不大。这证明TiO2成功负载到LDH 吸附剂上,且在吸附剂上的分布较均一。
2.1.2 透射电镜 采用TEM 表征材料的形貌和元素分布,结果如图1所示:合成的LDH晶体具有清晰均匀的大尺寸六边形结构,粒径为2.9 μm×0.7 μm。使用EDX 获得TiO2/LDH 材料Ti 元素的映射显示,在基底LDH 材料上出现Ti元素,证明了TiO2在LDH基底上成功负载。同时,完整六边形的形貌在TiO2添加后没有变化,这表明TiO2颗粒的负载不会改变LDH的层状结构。
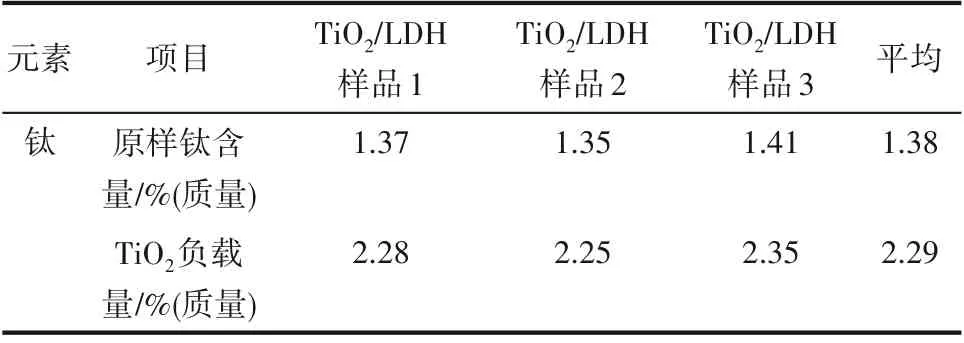
表1 TiO2/LDH中TiO2负载量实验数据Table 1 Test on TiO2 loaded in TiO2/LDH
2.1.3 X 射线衍射 采用XRD 表征材料的结晶度,结果如图2 所示:LDH 材料在11.7°、23.5°、61.2°和62.5°出现的衍射峰分别对应于(003)、(006)、(110)和(113)晶面,与文献[20]报道的一致。较强的(003)和(006)晶面衍射分别表示0.754 nm 和0.378 nm 的层间距,这证明了LDH有序的分层结构和层间CO32-的存在。同时,(110)和(113)晶面衍射峰是由于MgAl-OH 层内原子排布所产生[21]。TiO2/LDH 材料的XRD 谱图中,在25.3°、27.4°和48.0°还出现了来自TiO2的锐钛矿(101)、金红石(110)和锐钛矿(200)晶面衍射的峰[22],这同样证明了TiO2在LDH 基底上成功负载。同时,添加TiO2后LDH的XRD特征峰没有改变,表明TiO2不会干扰LDH 的层形成过程,CO32-可以通过大量的氢键作用将MgAl-OH 层的各层紧密结合在一起[23]。
2.1.4 比表面和孔径分布 通过BET 测试材料的比表面积及孔径分布情况。结果如表2 所示:LDH和TiO2/LDH的比表面积分别为59.4 m2/g和67.1 m2/g。TiO2/LDH 的平均孔径和孔体积都比LDH 略大,这可能是由于TiO2的负载使LDH 的分层开口略微增大,有利于LDH 表层的吸附位点暴露出来,增加了比表面积。
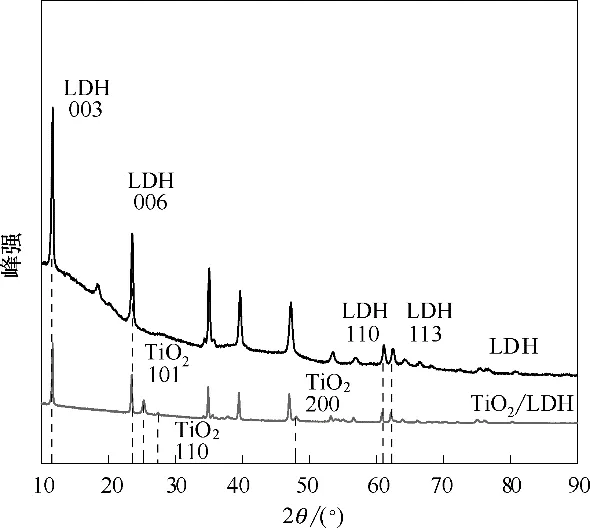
图2 LDH和TiO2/LDH的X射线衍射谱图Fig.2 X-Ray diffraction(XRD)patterns of LDH and TiO2/LDH

表2 LDH和TiO2/LDH材料的比表面积及孔隙性质Table 2 Specific surface area and pore textural properties of LDH and TiO2/LDH
2.2 材料吸附性能评价

图1 LDH和TiO2/LDH的扫描透射电镜及TiO2/LDH元素映射图Fig.1 Scanning electron microscopy(SEM)and mapping image of LDH and TiO2/LDH
2.2.1 等温吸附性能评价 采用Langmuir 和Freundlich等温吸附模型对LDH 和TiO2/LDH 材料吸附甲基橙和亚甲基蓝的过程进行拟合,结果如图3和表3 所示:Langmuir 吸附模型拟合的相关系数均高于Freundlich 吸附模型,表明有机染料对两种LDH 基材料的吸附倾向于单层而非多层吸附[24]。两种LDH 基材料对带负电的甲基橙的吸附量(527.5 mg/g)比带正电的亚甲基蓝的吸附量(208.3 mg/g)高得多。相比于其他碳基吸附剂的吸附量(活性碳纤维,甲基橙,qm=294.12 mg/g[25];兰炭材料,亚甲基蓝,qm=40.8 mg/g[26]),LDH 展现出优异的吸附性能。同时,TiO2/LDH 材料对两种有机染料的吸附总体上显示出比LDH 材料略高的吸附容量,可能是由于TiO2的负载会导致LDH 层间吸附位点的暴露,使材料的吸附性能有所提高。
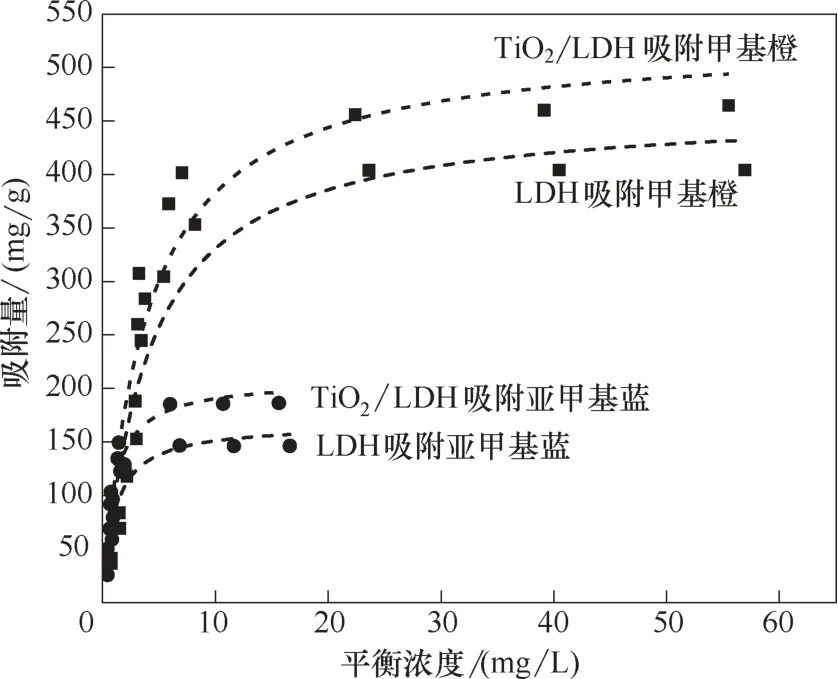
图3 LDH和TiO2/LDH对有机染料的Langmuir等温吸附拟合图Fig.3 Adsorption isotherms of organic dyes onto LDH and TiO2/LDH fitted by Langmuir model
2.2.2 动力学吸附性能评价 通过拟一级和拟二级动力学模型对LDH 和TiO2/LDH 材料吸附甲基橙和亚甲基蓝的过程进行拟合,拟合曲线见图4,动力学参数见表4。拟二级动力学方程对LDH 和TiO2/LDH 材料吸附两种有机染料的相关性系数均大于拟一级动力学方程,这意味着两种污染物的吸附机制可能相同[27]。LDH 和TiO2/LDH 材料对两种有机染料的吸附在前2 min 内非常迅速,在5 min 后达到吸附平衡。
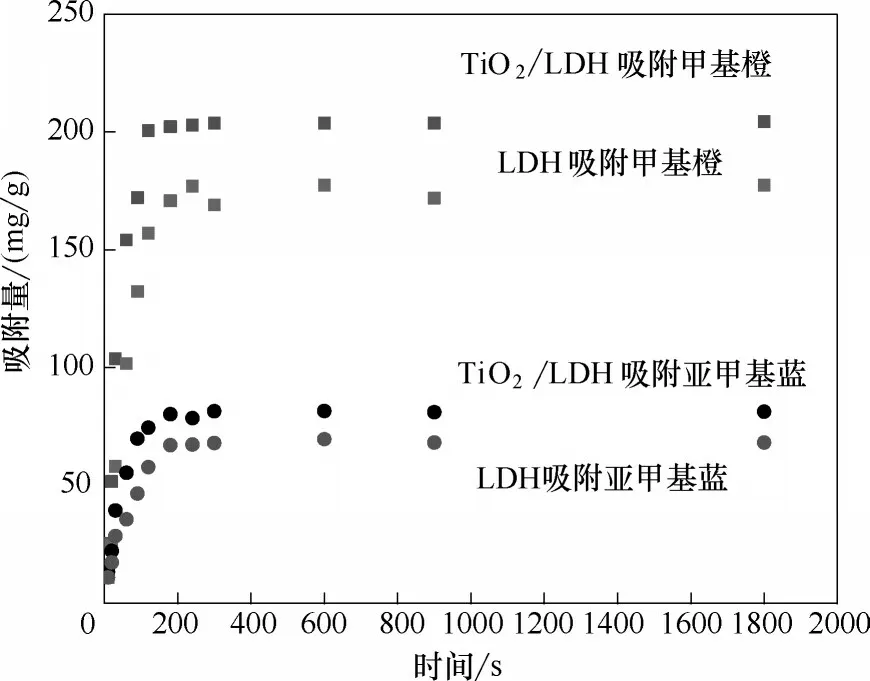
图4 LDH和TiO2/LDH对有机染料的吸附动力学Fig.4 Adsorption kinetics of organic dyes onto LDH and TiO2/LDH
2.3 材料再生性能评价
图5显示了甲基橙和亚甲基蓝吸附饱和的LDH和TiO2/LDH 材料再生动力学曲线,表5 为再生动力学参数。其中亚甲基蓝吸附饱和的材料在2 h 内完成了80%以上的再生,在4 h 后达到了再生饱和,亚甲基蓝吸附饱和的TiO2/LDH 材料第一轮再生率为93.9%。甲基橙吸附饱和的TiO2/LDH 材料在3 h 内完成80%以上的再生,在5 h 后同样达到再生饱和,甲基橙吸附饱和的TiO2/LDH 材料第一轮再生率为96.8%。未负载TiO2的LDH 材料在10 h 的光助再生后,只有2%~3%的吸附位点被再生,其可能是由于有机染料在LDH材料上的脱附而产生。图6显示的是多轮吸附再生循环实验中,甲基橙吸附饱和的TiO2/LDH 材料在4 轮循环再生吸附后还保持88.6%的再生率。亚甲基蓝吸附饱和的TiO2/LDH 材料在4轮循环再生后再生率仍保持在94.7%以上。与同类型碳基催化材料相比具有更高的循环再生能力(NTiO2/季铵化壳聚糖杂化膜,甲基橙,4 次循环再生率83.8%[28];石墨烯负载TiO2复合材料,亚甲基蓝,5 次循环再生率82.3%[29])。
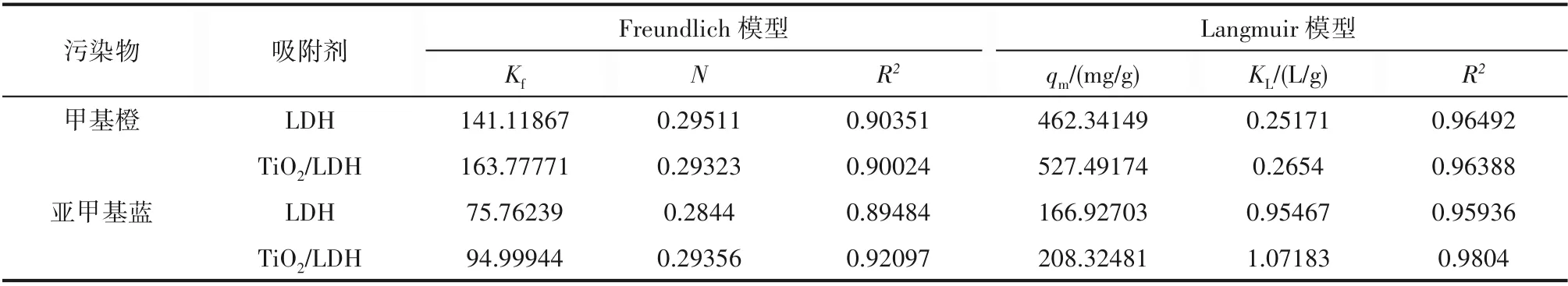
表3 LDH和TiO2/LDH对有机染料的Freundlich和Langmuir等温吸附参数Table 3 Regression parameters of adsorption isotherms of organic dyes onto LDH and TiO2/LDH fitted by Freundlich and Langmuir models
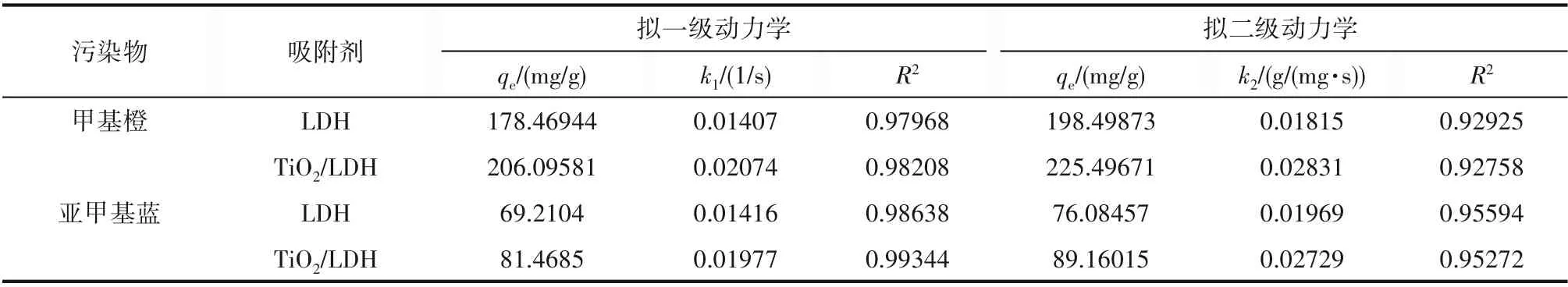
表4 LDH和TiO2/LDH对有机染料的吸附动力学参数Table 4 Adsorption kinetic parameters of organic dyes onto LDH and TiO2/LDH
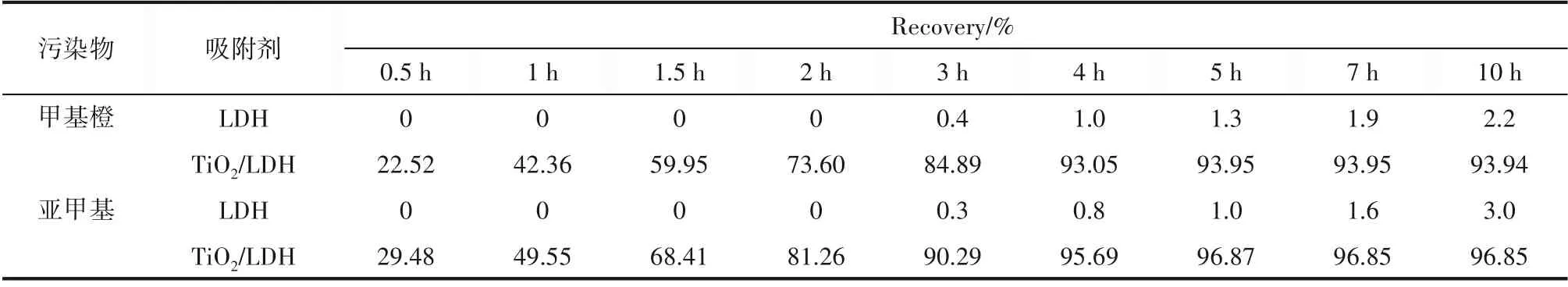
表5 LDH和TiO2/LDH对有机染料的再生动力学参数Table 5 Regenerated kinetic parameters of LDH and TiO2/LDH for organic dyes in timeline of photocatalytic regeneration

图5 LDH和TiO2/LDH对有机染料的再生动力学Fig.5 Regenerated kinetics of LDH and TiO2/LDH for organic dyes in timeline of photocatalytic regeneration
2.4 材料光助再生机理
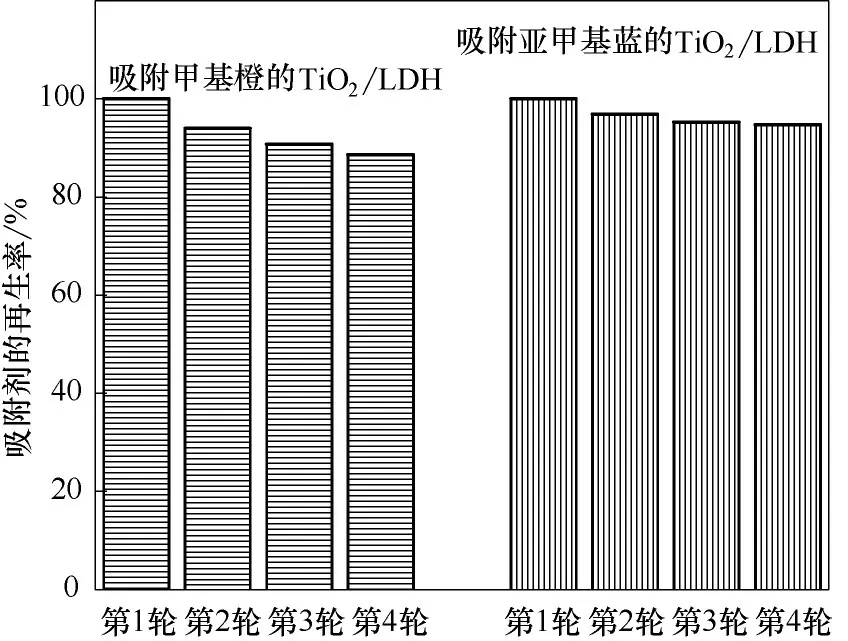
图6 TiO2/LDH吸附有机染料的多轮循环吸附再生Fig.6 Percentage of regenerated adsorption capacity of LDH and TiO2/LDH for organic dyes in cycles of photocatalytic regeneration
TiO2/LDH 具有光助再生性能,主要是由于LDH吸附剂上负载的TiO2在受到紫外光辐射时,当辐射光的能量大于或等于TiO2带隙能(3.1~3.3 eV)时,TiO2价带上的电子吸收光能后,被激发跃迁至导带,使得导带上生成激发态电子(e-),而在价带上生成空穴(h+)[30-31]。激发态电子(e-)与吸附在材料表面上的O2分子发生还原反应,产生超氧分子自由基(·O2-),·O2-可进一步与H+反应生成H2O2。同时h+与H2O、OH-发生氧化反应,产生活性很强的羟基自由基(·OH)。这些自由基具有很强的氧化性,由于LDH 的强抗氧化能力,这些活性氧物种可以特异性地矿化吸附在LDH 上的染料分子产生CO2和H2O 等物质[32],而不破坏LDH 吸附剂的结构,实现LDH 上吸附位点的再生。而且LDH 透光性强的特点,很好地保证了光辐射的能量尽可能多地被TiO2所利用,提高了整个光再生过程的光量子利用率。
3 结 论
采用典型的尿素水解水热法成功地将TiO2负载到LDH 基底材料上,制备出二氧化钛/层状双氢氧化物吸附剂(TiO2/LDH),对有机染料具有较高的吸附容量,而且由于材料的抗氧化能力和透光性可以避免光催化过程中材料受活性氧攻击和基底的光吸收导致光量子效率的下降,具有高效的光助再生能力。对甲基橙的吸附量为527.5 mg/g,在4轮循环再生后仍具有88.6%的再生率;对亚甲基蓝的吸附量为208.3 mg/g,在4 轮循环再生后仍具有94.7%的再生率。

