多元层板金属LDH-PDS复合材料的氧化性能比较
张国芳
(上海城投<集团>有限公司,上海 200020)
近年来,水体中各种微污染物急剧增加,其中包含一些新型的、难降解的污染物,如药物和个人护理品[1-2]、内分泌干扰物[3-4]、藻毒素[5-6]等,水源水质不容乐观。同时,随着生活水平的日益提高,人们对水质的要求也更为严格,这对水处理环节提出了严苛的技术要求。
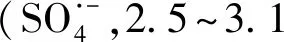

本研究从层板金属组成角度出发,考察不同层板二价金属(Cu/Ni/Co/Mg)与三价金属(Al)组成的二元或三元LDH-PDS复合材料的氧化性能,为优化LDH-PDS复合材料的制备提供数据支撑。
1 材料和方法
1.1 试剂与仪器
仪器: Dmax-2500 X 射线衍射仪(日本理学公司),高效液相色谱仪(日本岛津公司),电感耦合等离子体仪(美国LEEMAN公司)。
试剂:硝酸镁[Mg(NO3)2·6H2O,AR]、硝酸铝[Al(NO3)3·9H2O,AR]、硝酸铜[Cu(NO3)2·3H2O,AR]、硝酸钴[Co(NO3)2·6H2O,AR]和硝酸镍[Ni(NO3)2·6H2O,AR]、氢氧化钠(NaOH,AR)和苯酚(PhOH,AR)。
1.2 试验方法
试验所用LDH材料均采用共沉淀法进行合成。初始金属盐比例根据不同的试验要求进行投加。本研究中如无特殊说明,均使用配比为3∶1的Mg/Al金属层板、硝酸根离子插层的LDH,记为MgAl-LDH-NO3或LDH-NO3。
1.2.1 多元层板金属LDH前体物的制备(LDH-NO3)
称取75 mmol/L Mg(NO3)2·6H2O 和25 mmol/L Al(NO3)3·9H2O配制成100 mL的盐溶液,另称取200 mmol/L NaOH 固体配制成100 mL碱溶液。在室温条件下,将碱液和盐溶液逐滴加入三口烧瓶中,同时用磁力搅拌器剧烈搅拌,整个过程在 N2氛围中进行,滴加时间保持在10 min之内,待溶液均滴加完后,pH值约为10。塞住瓶口,使之密封,继续剧烈搅拌2 h后,将该乳浊液于65 ℃水浴锅中恒温陈化12 h,并以去离子水洗涤3次。最后,将样品置于65 ℃真空干燥箱中干燥,研磨得到固体粉末,待用。试验所用水均为脱CO2的去离子水。
制备不同金属层板LDH时方法同上,需相应地改变投加盐的质量。
1.2.2 PDS插层的多元层板金属LDH的制备(LDH-PDS)
PDS插层LDH的制备:称量上述制备好的LDH前体物投加到一定浓度的PDS溶液中,隔绝空气的条件下剧烈搅拌1 h,然后离心并将得到的固体粉末进行冷冻干燥。制备后的PDS插层LDH均记为LDH-PDS或LDH-PDS-x,x表示插层时加入的PDS初始浓度,单位为 mmol/L。与之混合的LDH如无特殊说明,均默认为1 g/L。
1.2.3 材料表征
X射线衍射光谱分析(X-ray diffraction)采用日本理学公司 Dmax-2500 X射线衍射仪,使用铜Kα辐射,波长为 0.15 418 nm,电压为40 kV,电流为 250 mA,步幅为0.02°,测角转速器的转速为8°/min,起始角度为5°,终止角度为80°。依据相关文献中出峰位置及Jade软件卡片数据库对所得XRD图谱的主要衍射峰进行定性分析。本研究中XRD主要用来确定LDH的层间距和层状结构。
LDH层板金属含量利用美国LEEMAN公司的电感耦合等离子体仪(inductively coupled plasma emission spectrometer,ICP)进行测定。准确称取10 mg LDH溶于100 mL 50%的硝酸溶液中,4 h后过0.45 μm膜,并用ICP测定溶液中的金属浓度。
2 结果与讨论
2.1 多元层板金属LDH-PDS复合材料的表征
试验中使用的几种多元层板金属LDH-PDS复合材料的实际金属含量如表1所示。其中,所有LDH层板2/3价金属比例为2∶1~3∶1,Co1和Co2指Co含量不同的样品。

表1 各类LDH-PDS中的金属含量 [单位:mmol/(100 mg LDH)]Tab.1 Metal Content in Various LDH-PDS[Unit:mmol/(100 mg LDH)]
图1为不同层板金属LDH前体物的XRD图谱。由图1可知,MgAlCo1-LDH、MgAlCo2-LDH、MgAl-LDH、NiAl-LDH均具有良好的层状结构,基线平稳,峰形完整,而CoAl-LDH波谱上的峰强度相对较小,但在(003)、(006)等处的LDH特征峰均明显可见。

图1 不同LDH的XRD图Fig.1 XRD Spectra of Different LDH
其中,MgAlCo1-LDH-PDS相对于MgAlCo2-LDH-PDS的d003峰有明显左移,说明后者层间距相对于前者减小了0.23 nm。进一步利用Jade软件进行物相匹配分析,2种三元LDH材料中均有纯相的Co(OH)2存在,说明含Co三元LDH层板晶型不够完美。
CuAl-LDH的波谱基线起伏大,峰形不明显,说明其结构混乱,杂质较多。事实上,Cu2+(0.069 nm)单独作为二价金属离子组成层板的LDH确实较难合成且不稳定。因为Cu2+在和层板羟基配位形成铜氧八面体时姜-泰勒效应严重,首先生成八面体复合盐而并非层状结构的水滑石[12-13]。这种八面体复合盐有可能是一种拉长的铜八面体,姜-泰勒效应导致的畸变与客体间的氢键和静电作用力非常弱,导致层状结构无法形成[14]。
总的来说,含Co三元LDH和含Cu二元LDH的峰形结构不明显,层板晶型不完美,可能会对其活化PDS氧化有机物的性能产生一定的影响。
2.2 多元层板金属LDH-PDS复合材料的氧化性能比较
以苯酚为目标有机物,对比Co/Cu/Mg/Ni 4种二价金属与Al组成的不同二元或三元层板金属组合的LDH-PDS对有机物的氧化性能。
如图2所示,当苯酚初始浓度为3 mg/L时,除二元类水滑石CoAl-LDH-PDS对PhOH只有14.3%的降解率外,其余LDH-PDS材料对PhOH都有着较好的降解效果。其中,CuAl-LDH对PhOH的降解率最高,达到95%以上。NiAl-LDH-PDS的苯酚去除率次之,在10 min之内达到78.1%,4 h后达到88.2%,高于同时刻的MgAl-LDH-PDS(83.8%)。
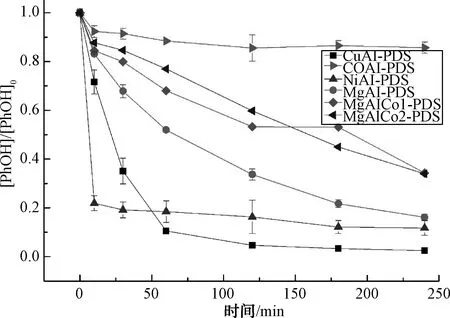
图2 不同金属层板组成的LDH-PDS对PhOH的降解Fig.2 Effect of Metal Type as Laminent on the Degradation of PhOH by LDH-PDS
不同的有机物氧化效果可能和层板结构有密切的关系。对于CuAl-LDH,其对苯酚的高效氧化可能与生成的八面体Cu复合盐对PDS的催化性能有关。Co2+(0.075 nm)的半径大于Mg2+(0.072 nm)和Ni2+(0.069 nm),因此,CoAl-LDH-NO3的层间距比MgAl-LDH-NO3、NiAl-LDH-NO3大[15],这一点可以从XRD图中得到验证(图1)。另外,CoAl-LDH-NO3、MgAl-LDH-NO3和NiAl-LDH-NO33种水滑石的晶面电荷密度(d110)逐渐减小,分别为0.154、0.153、0.151 nm,说明3种水滑石的晶胞参数a(a=d110)同样是逐渐减小的。这种差别可能导致层板金属对层间阴离子的作用力不同,进而影响PDS的活化与苯酚的降解,使得CoAl-LDH-PDS对苯酚的去除率较低。此外,NiAl-LDH-PDS对PhOH极好的降解效果和其层板中含有的Ni2+对PDS的活化作用有关。由Co参与组成的2种三元类水滑石(MgAlCo1-LDH-PDS和MgAlCo2-LDH-PDS)的效果略不及MgAl-LDH,这可能与其峰形结构不明显和层板晶型不完美有关(图1)。

图3 二元LDH-NO3对PhOH的吸附Fig.3 Adsorption of PhOH by Binary LDH-NO3
为考察复合材料自身对有机物的吸附作用,研究上述几种二元或三元LDH-NO3对苯酚的的吸附性能(图3和图4)。由图3和图4可知,各二元或三元LDH-NO3对PhOH的吸附性能均较接近,4 h内吸附率基本都在20%以内,表明LDH-PDS复合材料对有机物去除并不主要来自吸附。其中,两种不同Co含量的三元水滑石的吸附作用相差较明显,高含量Co的LDH(Co2)对PhOH的吸附性能不及低含量Co的LDH(Co1)。可能原因是金属层板上适当地引入Co可以增加LDH的比表面积[16],增大吸附性能。但随着Co引入量的增加,LDH的层板结构遭到破坏,Co3O4或其他Co氧化物破坏LDH的层板晶型,导致LDH结构塌陷,比表面积下降,反而破坏了LDH的催化性能,这与文献报道一致[17-18]。

图4 三元LDH-NO3对PhOH的吸附Fig.4 Adsorption of PhOH by Ternary LDH-NO3
3 结论
以Cu/Ni/Co/Mg 4种二价金属与三价Al组成的LDH-NO3作为LDH-PDS复合前体物,Cu/Ni/Mg 3种二价金属的LDH-PDS具有较好的降解苯酚性能,4 h时PhOH的去除率分别为95%、88.2%、83.8%,而含Co的LDH-PDS效果并不显著(14.3%)。各材料对PhOH的氧化性能由高到低的顺序依次为Cu≈Ni>Mg>Co。其中,含Co三元LDH和含Cu二元LDH结构晶型较差,层状结构不明显。含Cu和Ni的LDH的较强氧化能力分别来源于八面体Cu复合盐和过渡金属Ni对PDS的活化。含Co的LDH氧化能力较弱是由于层板金属对层间阴离子的作用力较弱,同时,Co的过度引入会影响材料的催化性能。

