电位滴定法连续测定磷矿浮选尾矿中的钙镁含量
史 鑫,付学会,梅连平,余慧茹,彭 桦
(国家磷资源开发利用工程技术研究中心,云南 昆明 650600)
在磷矿浮选过程中,尾矿中钙、镁含量是一项重要指标。测定磷矿石中钙、镁含量的方法包括传统的乙二胺四乙酸(EDTA)容量法、火焰原子吸收法及电感耦合等离子发射光谱法等。其中传统EDTA 容量法干扰元素较多,滴定终点主要依据肉眼判断,而浮选尾矿中钙、镁含量偏高,加入指示剂后滴定终点不易观察,容易造成数据误差较大从而导致测定结果不准确。笔者采用电位滴定法连续测定磷矿石浮选尾矿中的钙、镁含量。该法操作简单,并且测得结果重现性好、准确度高,是一种可靠、便捷的分析方法。
1 实验部分
1.1 仪器及工作参数
Metrohm-905 全自动电位滴定仪;瑞士万通Ca2+选择性电极;250 mL 容量瓶;梅特勒电子天平,AB204-S;刻度移液管,5、10、20 mL;烧杯,150、300 mL。
1.2 试剂及标准溶液
盐酸、硝酸、糊精、三乙醇胺、三羟甲基氨基甲烷(Tris)、乙酰丙酮(HAA)、EDTA-2Na 均为分析纯;去离子水,电阻率18 MΩ·cm(20 ℃)。
20 g/L 糊精溶液:称取糊精2 g,用水调成糊状,加入煮沸的纯水100 mL(使用前配制)。
辅助溶液(c(乙酰丙酮)= 0.1 mol/L,c(Tris)=0.2 mol/L):取三羟甲基氨基甲烷20.4 g 溶于500 mL去离子水中,加入乙酰丙酮12 mL,定容到1 L。
三乙醇胺(1+4);EDTA-2Na 标准溶液,0.02 mol/L,配制与标定按GB/T 601—2016执行。
1.3 反应机制
在滴定过程中,当EDTA-2Na 标准溶液加入时,其先与Ca2+发生反应,得到第一个反应终点EP1,继续滴加EDTA-2Na标准溶液,由于EDTA-Mg的络合平衡常数比Mg(AA)2大,使得Mg2+与EDTA发生反应,从而得到第二个反应终点EP2,而第二个反应终点EP2与第一个反应终点EP1的差值对应的就是Mg2+的含量,从而实现电位滴定法连续滴定混合溶液中Ca2+、Mg2+[1]。
1.4 实验方法
称取磷矿试样约0.5 g(精确至0.000 1 g),置于300 mL 烧杯中,加少量水润湿试样,小心加入盐酸15 mL和硝酸5 mL,盖上表面皿,混匀,在低温电热板上加热至沸,保持微沸15 min。取下烧杯,待烧杯稍冷,用蒸馏水冲洗表面皿及杯壁,冷却后将烧杯中液体转移至250 mL 容量瓶中,用水稀释至刻度,摇匀,同时做空白实验。将容量瓶中的液体用慢速滤纸干过滤后用移液管吸取滤液20 mL置于150 mL 烧杯中,加入蒸馏水50 mL、20 g/L 的糊精10 mL、三乙醇胺(1+4)10 mL、辅助溶液8 mL(每加一种试剂都需摇匀),然后将烧杯放置于自动电位滴定仪上,将钙电极及搅拌装置置于溶液中,连接自动电位滴定仪,用已标定好的EDTA-2Na标准溶液滴定试液中的钙、镁离子,通过电位突跃变化测量等当点的电极电位EP1和EP2,自动记录滴定钙、镁离子的EDTA-2Na标准溶液用量,消耗体积记为V1、V2。并根据在计算机软件中编制的计算公式计算出钙、镁的含量[2]。
1.5 计算公式
磷矿浮选尾矿中钙、镁含量按式(1)、式(2)进行计算。

式中 V1——第一个等当点消耗EDTA-2Na标准滴定溶液体积,mL;
V2——第二个等当点消耗EDTA-2Na标准滴定溶液体积,mL;
V0——空白实验消耗EDTA-2Na标准滴定溶液体积,mL;
m1——吸取试样溶液相当于氧化钙试样的质量,g;
m2——吸取试样溶液相当于氧化镁试样的质量,g;
ρ1——与1.00 mL EDTA-2Na标准滴定溶液相当的氧化钙质量,0.056 08 g/mL;
ρ2——与1.00 mL EDTA-2Na标准滴定溶液相当的氧化镁质量,0.040 03 g/mL。
2 结果与讨论
2.1 糊精溶液的用量
在样品中加入糊精,主要是为了抑制样品溶液中磷酸根的干扰及防止胶体吸附Ca2+对滴定结果产生影响,结果见表1。通过实验,发现加入糊精溶液5 mL 即可充分抑制样品溶液中磷酸根的干扰,为完全掩蔽PO43-,防止浪费试剂,选择加入糊精溶液10 mL。
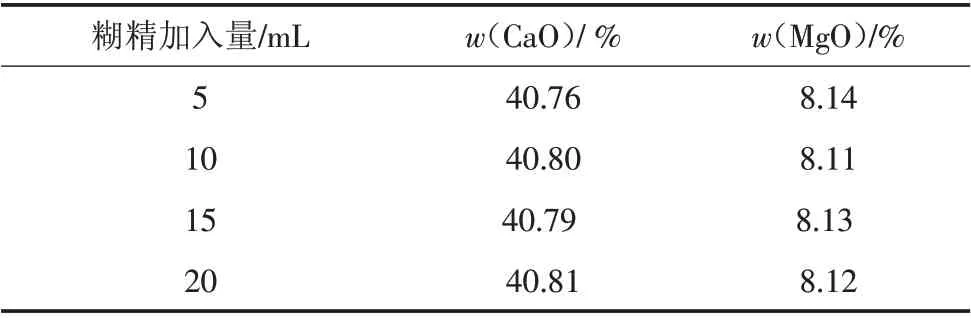
表1 糊精用量对测定结果的影响
2.2 三乙醇胺的用量
样品溶液中加入三乙醇胺,主要的目的是掩蔽溶液中的Fe3+、Al3+,防止其对滴定造成干扰。在待测液中分别加入三乙醇胺(1+ 4)5、10、15、20 mL,测定结果如表2所示。
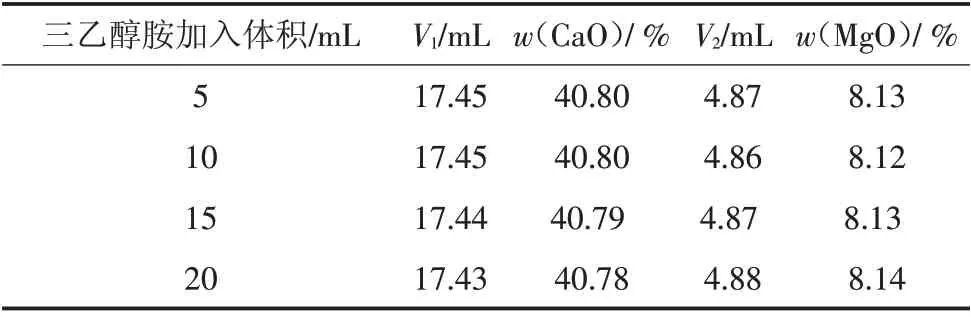
表2 三乙醇胺用量对测定结果的影响
通过在实验中加入不同体积的三乙醇胺,发现当加入三乙醇胺10 mL时既可以充分掩蔽样品溶液中Fe3+、Al3+,也不会过多的浪费试剂,因此选择加入三乙醇胺溶液10 mL。
2.3 辅助溶液的用量
为了分别滴定出样品中的Ca2+、Mg2+,加入乙酰丙酮,因为HAA为一元弱酸,可以使Mg2+首先与其络合生成Mg(AA)2而不影响钙的滴定。通过实验,选择样品中辅助溶液(乙酰丙酮-三羟甲基氨基甲烷缓冲溶液)的最佳加入量,结果如表3所示。
通过实验可以看出,当乙酰丙酮-Tris 缓冲溶液的加入量增大时,会影响Ca2+、Mg2+的滴定终点,从而改变滴定结果。分析原因:乙酰丙酮为一元弱酸,当它的加入量增大时,会影响到溶液的pH 值,从而影响钙离子与EDTA 的络合反应,当加入量大于8 mL 时钙离子滴定结果偏低而镁离子滴定结果偏高,加入量小于8 mL 时镁离子滴定结果偏低而钙离子滴定结果偏高。因此结合上述实验,选择加入8 mL 的乙酰丙酮-Tris 缓冲溶液,这样既不会影响到钙离子与EDTA的络合反应,同时也保证了结果的准确性。
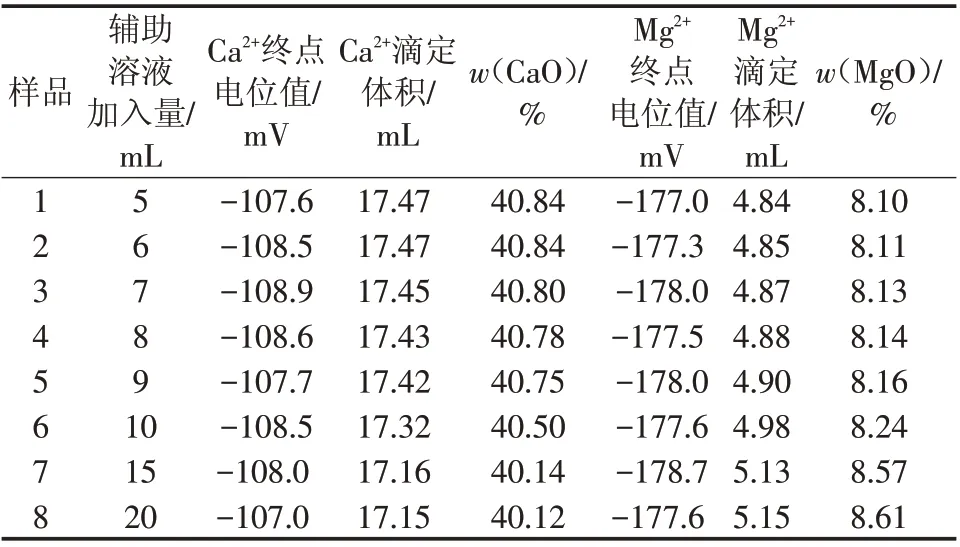
表3 辅助溶液用量对测定结果的影响
2.4 滴定速度的影响
实验中可以看出滴定速度会影响到此分析方法的精密度与准确度。当滴定速度过快时,会减小滴定过程中电位变化情况,即使达到滴定终点,电位变化也不明显。因此,为了保证此分析方法的精密度与准确度,将自动电位滴定仪设置为按最小体积添加,滴定速度为最优[1]。
2.5 精密度和准确度
按照分析方法,选择浮选尾矿样品(HX-1)和磷矿国标样品(GBW 07212)2 个样品进行测定,计算其精密度,分析结果见表4。
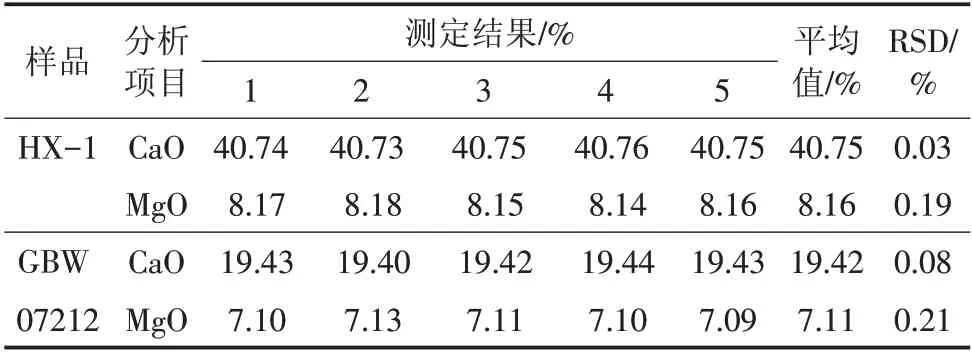
表4 电位滴定法精密度实验结果
由表4可知,CaO、MgO 的RSD 分别为0.03%~0.08%、0.19%~0.21%,表明此方法对磷矿石中钙、镁含量的测定精密度好,达到分析要求。
对试样做了回收率实验,计算其回收率如表5所示。
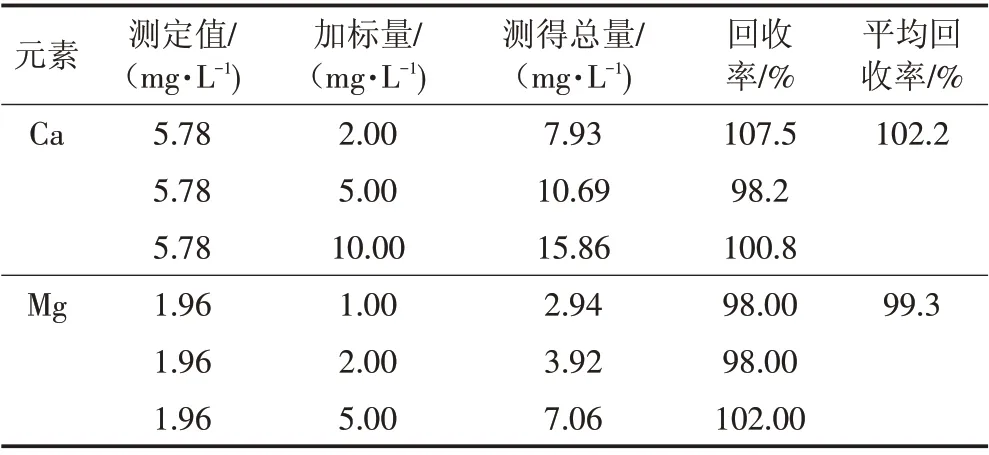
表5 样品准确度
表5 结果可以看出:钙离子的加标回收率为98.2%~107.5%,平均回收率为102.2%,镁离子的加标回收率为98%~102%,平均回收率为99.3%,说明该方法准确度较高。
2.6 干扰元素实验
浮选尾矿中含大量的PO43-、Fe3+、Al3+、Si4+等离子,为了考察上述离子的干扰,按实验方法,取浮选尾矿样品HX-1制成待测液,并向待测液中加入10倍的PO43-、Fe3+、Al3+、Si4+,对该溶液进行测定,结果见表6。
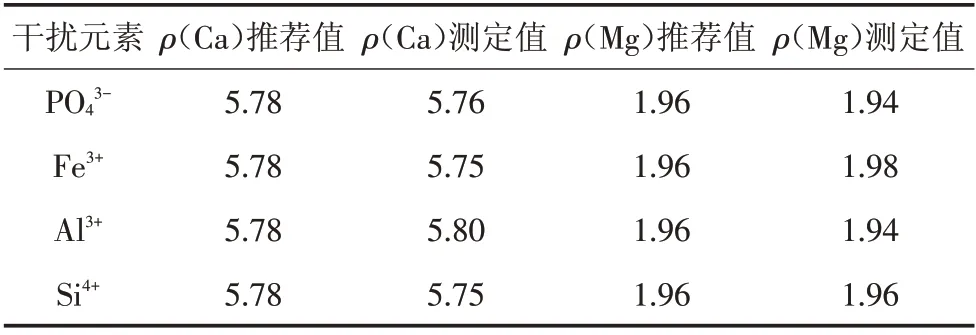
表6 不同干扰元素共存下待测液的测定结果 mg/L
由表6可知,待测液中加入较高含量水平的干扰元素后,钙、镁的测定值与其认定值偏离较小,说明用此法测量时,上述常见元素对钙、镁的测定基本无干扰。
2.7 方法对比
分别用电位滴定法和GB/T 1868—1995规定方法(化学法)测定磷矿国标样品(GBW 07212)与浮选尾矿样品(HX-1)中Ca、Mg含量,结果见表7。
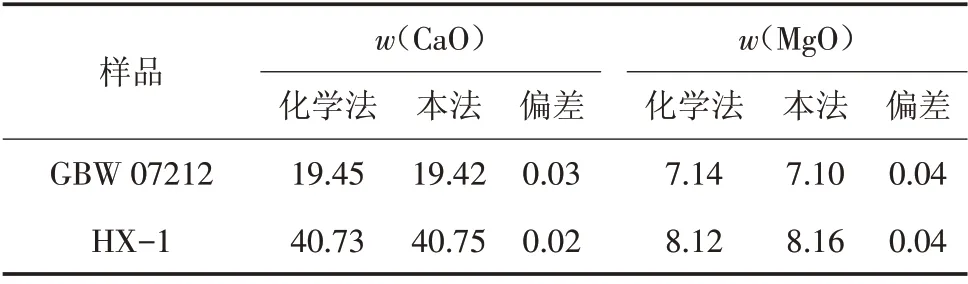
表7 分析结果 %
由表7 可知,本方法测定值与化学法结果相符,表明本方法测定结果准确性高,适用于磷矿浮选尾矿中钙、镁的分析检测。
3 结论
利用自动电位滴定仪可准确滴定出磷矿浮选尾矿中钙、镁含量。该方法与传统的滴定方法相比,具有较高的选择性,测量快捷,结果准确,具有广泛的适用性。

