石灰石和钾长石焙烧法制备硅钙钾肥试验研究
李兴平,刘阳,2,胡兆平,2,3
(1.金正大生态工程集团股份有限公司,山东 临沂 276000;2.养分资源高效开发与综合利用国家重点实验室,山东 临沂 276000;3.国家缓控释肥工程技术研究中心,山东 临沂 276000)
钾矿资源中的钾一般分为水溶性钾和水不溶性钾,但中国的水溶性钾矿资源稀缺,而以钾长石为代表的水不溶性钾矿资源极为丰富[1],但农作物不能直接吸收利用钾长石中的钾元素,因此研究从水不溶性钾长石中提取钾元素,生产水溶性或枸溶性钾肥,可有效缓解目前中国钾肥短缺问题。国内外学者利用水不溶性钾矿提钾进行了多种方法研究[2-3],主要包括:高温焙烧法[4]、水热法、低温酸分解法[5]和微生物分解法[6-7]。这些研究为以钾长石为原料制备钾肥提供了可靠的理论依据[8-9]。本文选用高温焙烧法,利用石灰石在助剂硫酸钠的作用下,将钾长石中的钾和硅元素转化为能被植物吸收的有效成分,制备硅钙钾肥,找出该生产过程中的较佳参数条件,探索石灰石与钾长石在助剂硫酸钠作用下的热反应原理。
1 试 验
1.1 试验原料
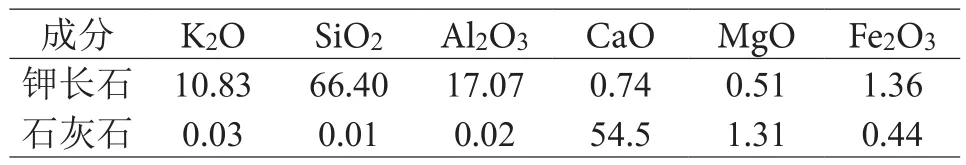
表1 钾长石和石灰石的主要化学组成/%Table 1 Main chemical composition of potassium feldspar and limestone
原料采用石灰石、钾长石和硫酸钠三种。钾长石和石灰石均采自贵州某地,硫酸钠为无水硫酸钠分析纯试剂。钾长石和石灰石的化学成分分析结果见表1。
1.2 试验方法与分析
1.2.1 硅钙钾肥制备方法
试验所用原料经破碎机破碎后再经球磨机粉磨,过0.074 mm标准筛后得到试验原料,以试验配比混合研磨的钾长石、石灰石和硫酸钠。将混合均匀的物料放入瓷坩埚中,然后放到马弗炉中在设定的温度下焙烧一定时间,等焙烧结束后将焙烧产物取出放到常温冷却,将冷却好的样品研磨至一定粒度即为硅钙钾肥,密封保存留用。
1.2.2 分析方法
称取1 g研磨后的焙烧产物于250 mL容量瓶中,加入100 mL浓度为2%的柠檬酸溶液,放到振荡器上振荡1 h后进行定容,过滤溶液,弃去刚开始的10 mL溶液,用火焰光度计分析样品中枸溶性K2O含量[10]。
通过XRD分析焙烧产物,根据物相分析结果讨论石灰石和钾长石在助剂硫酸钠作用下的热反应机理。
1.2.3 K2O的活化率计算
K2O的活化率计算公式为:
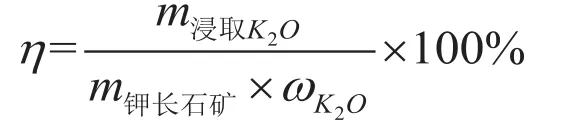
式中:m浸取K2O-浸取液中氧化钾的质量,g;
m钾长石矿-原料中钾长石的质量,g;
ωK2O-钾长石矿中氧化钾含量,%。
2 结果与讨论
2.1 石灰石与钾长石质量比对钾长石中K2O活化率的影响
固定焙烧温度1100℃,焙烧时间60 min,无水硫酸钠用量为石灰石和钾长石总质量的4%,改变石灰石与钾长石质量配比进行试验,K2O活化率试验结果见图1。
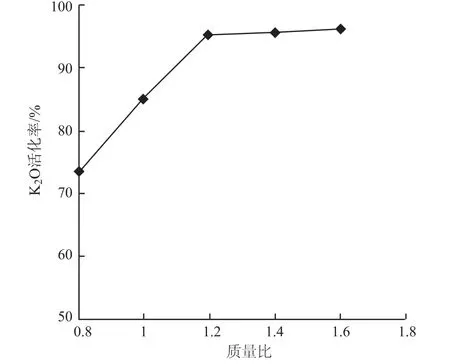
图1 石灰石与钾长石质量比对K2O活化率的影响Fig .1 Effect of mass ratio on K2O activation rate
由图1可知,随着石灰石与钾长石的质量比由0.8增加到1.2时,钾长石中K2O活化率一直在增大,当质量比增加到1.2:1后,K2O活化率随质量配比的增加变化不大,此时配料中石灰石比例的增加对提高K2O活化率没有显著作用,由于石灰石比例的增加,反而会降低焙烧产物中对植物有益的元素含量,如钾和硅等元素,综合考虑,石灰石和钾长石的质量比为1.2:1时较佳,此时钾长石中K2O活化率为95.3%。
2.2 硫酸钠用量对钾长石中K2O活化率的影响
固定石灰石与钾长石质量比为1.2:1,焙烧温度1100℃,焙烧时间60 min,改变硫酸钠占石灰石和钾长石总质量的百分数进行试验,试验结果见图2。
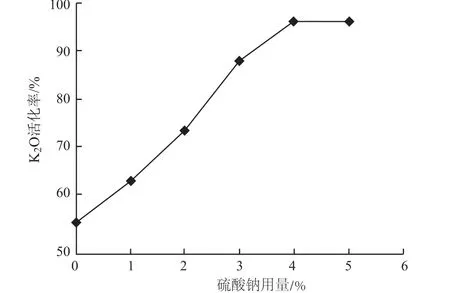
图2 硫酸钠用量对K2O活化率的影响Fig .2 Effect of sodium sulfate dosage on K2O activation rate
从图2可以看出,随着硫酸钠用量的增加,钾长石中K2O活化率一直在增大,在硫酸钠用量为4%之前,K2O活化率增大很快,当用量超过4%以后,K2O活化率基本维持不变,此时K2O活化率为95.3%。结果表明,硫酸钠的加入能够使石灰石和钾长石在不烧熔的条件下进行完全反应,起到降低反应温度并提高钾的溶出率的作用,硫酸钠的合适添加量为石灰石和钾长石总质量的4%。
2.3 焙烧温度对K2O活化率的影响
钾长石自身的分解温度很高,但通过添加助剂可有效降低钾长石的分解温度[12]。在探索体系的合适焙烧温度时,固定石灰石与钾长石质量比为1.2:1,无水硫酸钠用量为石灰石和钾长石总质量的4%,焙烧时间60 min,在1000 ~ 1180℃进行试验,试验结果见图3。
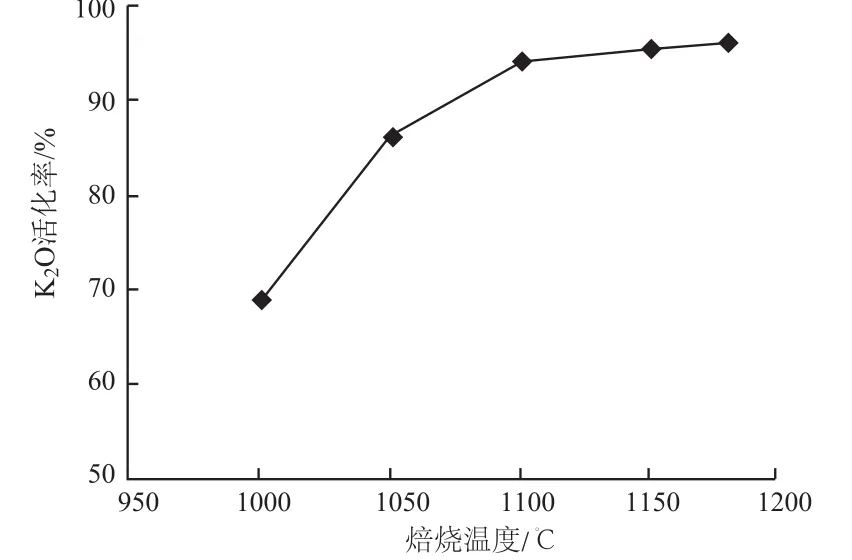
图3 焙烧温度对K2O活化率的影响Fig .3 Effect of roasting temperature on K2O activation rate
由图3可以知,随着焙烧温度的升高,钾长石中K2O活化率也逐渐增加,当焙烧温度达到1100℃以后,K2O活化率随温度变化不大。工业生产时要控制好温度,防止温度过高时(1200℃)物料熔化出现液相,导致回转窑不能正常运转。考虑到节约能源,降低能耗,焙烧温度定为1100℃。
2.4 焙烧时间对K2O活化率的影响
固定石灰石与钾长石质量比为1.2:1,无水硫酸钠用量为石灰石和钾长石总质量的4%,焙烧温度1100℃,在20 ~ 100 min的时间段内进行试验,K2O活化率试验结果见图4。

图4 焙烧时间对K2O活化率的影响Fig .4 Effect of roasting time on K2O activation rate
从图4可以看出,随着焙烧时间的升高,K2O活化率先增大后趋于平缓。钾长石与石灰石在助剂硫酸钠的作用下于1100℃时,物料之间是固-固反应,物质之间移动慢,所以体系刚开始反应时,随着反应时间的延长,K2O活化率逐渐增大,当反应达到一定时间后(60 min),K2O活化率逐渐维持不变,焙烧时间越长,能耗越高,所以焙烧时间定为60 min,此时K2O活化率为95.3%。
2.5 硅钙钾肥枸溶性营养成分分析
按照石灰石与钾长石质量比为1.2:1,无水硫酸钠用量为石灰石和钾长石总质量的4%,在1100℃的马弗炉中焙烧60 min进行优化试验,冷却后的样品通过研磨即为硅钙钾肥,采用ICP对制得的硅钙钾肥进行枸溶性营养成分分析,其结果见表2。

表2 硅钙钾肥枸溶性营养成分/%Table 2 The solubility nutrients of silicate- calcium- potassium fertilizer
可以发现焙烧产物硅钙钾肥中含有的枸溶性的K2O和SiO2营养成分能被农作物直接吸收,CaO和MgO营养成分对提升农作物的产量及质量均是有益的。
2.6 钾长石与石灰石反应机理探讨
2.6.1 钾长石与石灰石焙烧产物XRD分析
将研磨后的石灰石与钾长石按质量比1.2:1混合均匀,在1200℃的马弗炉中焙烧60 min,焙烧产物冷却后进行研磨并进行XRD分析测试,图5即为上述焙烧产物的XRD图谱。
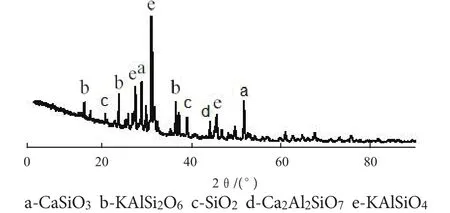
图5 石灰石与钾长石焙烧产物的XRDFig .5 XRD pattern of calcined products of limestone and potassium feldspar
从图5可以看出,在1200℃时,石灰石与钾长石体系中出现了白榴石KAlSi2O6的特征峰,而钾长石KAlSi3O8的衍射峰已经消失,随着CaCO3分解的CaO增多,新生的KAlSi2O6将进一步分解为 KAlSiO4和SiO2。而生成的CaO与SiO2反应形成CaSiO3,从焙烧产物相图可以看出还有一些铝黄长石Ca2Al2SiO7的衍射峰。Ca2+半径比K+小,所以高温条件下Ca2+能把钾长石结构中部分K+置换出来,由于钾长石结构被破坏,分子处于活跃和不稳定状态,体系反应更容易进行。焙烧产物中总钾含量低于反应前的总钾量,表明石灰石与钾长石体系在高温煅烧过程有部分钾损失,说明石灰石与钾长石系统中无合适的阴离子固定置换出来的K+。
2.6.2 石灰石、钾长石和硫酸钠焙烧产物XRD分析
按照石灰石与钾长石质量比为1.2:1,无水硫酸钠用量为石灰石和钾长石总质量的4%,焙烧温度1100℃,焙烧时间60 min的条件进行反应,焙烧产物冷却后进行研磨并做XRD分析测试,图6为焙烧产物的XRD图谱。
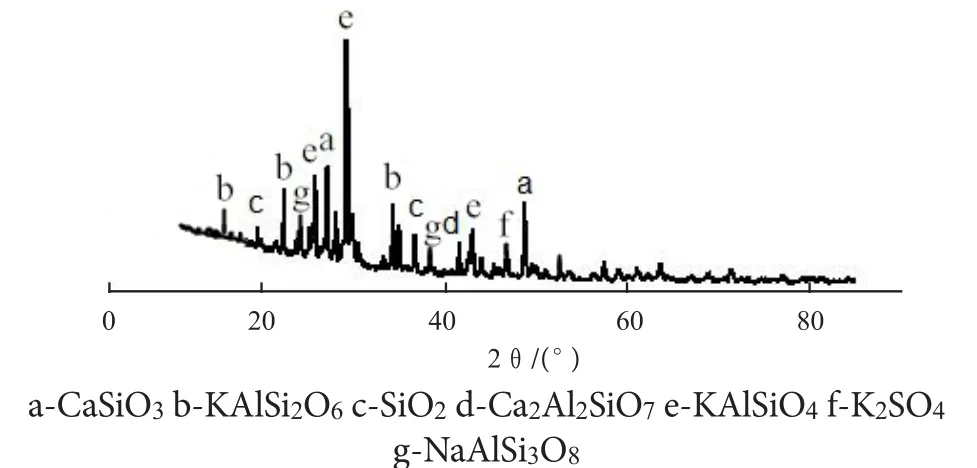
图6 石灰石、钾长石和硫酸钠体系焙烧产物的XRD图谱Fig .6 XRD pattern of calcined products of limestone,potassium feldspar and sodium sulfate
由图6可知,添加硫化钠后,焙烧产物中出现了K2SO4和钠长石NaAlSi3O8,钾长石与硫酸钠之间的分解反应基本上是离子交换反应,由于Na+半径比K+小,所以当温度达到Na2SO4的熔点时,Na2SO4中游离出来的Na+能进入钾长石结构中把有高温活性的K+挤出,很容易生成钠长石[11],而SO42-能固定K+,形成K2SO4。相对于钾长石KAlSi3O8来说,钠长石NaAlSi3O8的熔点低,因此由于钠长石NaAlSi3O8的形成,石灰石与钾长石体系熔点降低,反应时间缩短。
3 结 论
(1)石灰石、钾长石和硫酸钠体系的较优质量比为:石灰石与钾长石质量比为1.2:1,无水硫酸钠用量为石灰石和钾长石总质量的4%,焙烧温度1100℃,焙烧时间60 min,此时焙烧产物硅钙钾肥中K2O活化率为95.3%,K2O含量为5.31%,CaO含量为36.85%,SiO2含量为31.26%。
(2)X射线衍射仪分别对石灰石与钾长石、石灰石与钾长石和硫酸钠体系焙烧产物物相分析得出:高温条件下石灰石与钾长石体系能反应,但该体系反应温度高且反应达到平衡时间长,无阴离子来固定钾长石分解的钾元素导致部分K2O损失;添加硫酸钠后,由于形成的钠长石能降低石灰石与钾长石体系的熔点和缩短反应时间,降低了能耗,体系中的SO42-能固定钾长石分解的钾元素。体系中的CaCO3会分解为CaO和CO2,CaO与钾长石高温分解下产生的SiO2反应生成CaSiO3,随着CaO增多,新生KAlSi2O6将进一步分解为KAlSiO4和SiO2。同时CaO也会与Al2O3和SiO2发生反应,生成Ca2Al2SiO7等矿物。

