卵巢癌发生的高危因素分析
许培荣
卵巢癌能够导致病人短期内组织器官功能衰竭的发生,病人的远期临床预后较差[1]。而通过对于相关预防干预措施的分析,能够为卵巢癌的整体诊疗方面发挥重要的作用[2]。月经周期的改变,可能通过反应基础性的性激素水平的波动,反应性激素受体的敏感性,进而影响到卵巢生发上皮细胞的异常病变风险[3];吸烟、饮酒等生活习惯,可能通过影响到自身T淋巴细胞的免疫监察作用,导致T淋巴细胞吞噬癌细胞能力的下降,进而影响到卵巢癌的发生[4];卵巢癌相关家族史,能够增加后代携带卵巢癌相关癌基因的风险,导致肿瘤早期异常增殖和异常分化风险的上升,增加了癌细胞内肿瘤信号通路的激活水平,进而促进了卵巢癌的发生[5]。基础性性激素水平的紊乱或者卵巢癌家族史,是卵巢癌发生的危险性因素[6]。为了探讨本地区卵巢癌发生的高危因素,本研究选取2016年1月至2018年6月在我院治疗的卵巢癌病人90例,分析不同临床因素对卵巢癌发生的影响。现作报道。
1 资料与方法
1.1 一般资料 选取2016年1月至2018年6月在我院治疗的卵巢癌病人90例作为观察组,年龄26~70岁;同时按照年龄匹配方法选取270例健康志愿者作为对照组,年龄29~67岁。纳入标准:(1)2组受试者均在本辖区居住10年以上;(2)卵巢癌均经病理学确诊;(3)汉族;(4)能配合调查者。排除标准:(1)合并有其他恶性肿瘤者;(2)有认知功能障碍等精神疾病。
1.2 调查方法 收集2组一般资料,包括年龄、婚姻状况、文化程度,其中婚姻状况包括未婚、已婚、丧偶及离异等,文化程度主要包括高中及以上或者高中以下;收集2组孕次、产次、宫内节育器放置情况、月经周期及初潮年龄、哺乳与否,收集其吸烟、饮酒、卵巢癌家族史、自然流产及人工流产病史,其中吸烟与否以每日吸烟根数超过3支为界,饮酒与否以每日饮酒总量超过150 mL为界。采用单因素分析的方法评估不同因素对于卵巢癌发生的影响,并采用logistic回归分析评估卵巢癌发生的危险性因素。
1.3 统计学方法 采用χ2检验和多因素logistic回归分析。
2 结果
2.1 2组一般资料比较 2组年龄、婚姻状况及文化程度差异均无统计学意义(P>0.05)(见表1)。观察组产次为0次、月经周期>30 d、初潮年龄<13岁、有人工流产史、卵巢癌家族史的比例明显高于对照组(P<0.05~P<0.01)(见表2)。
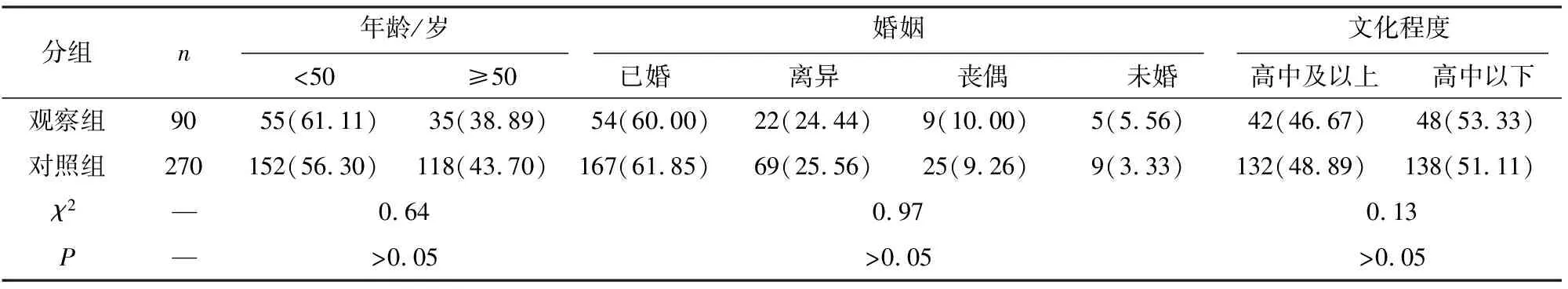
表1 2组年龄、婚姻及文化程度比较[n;构成比(%)]
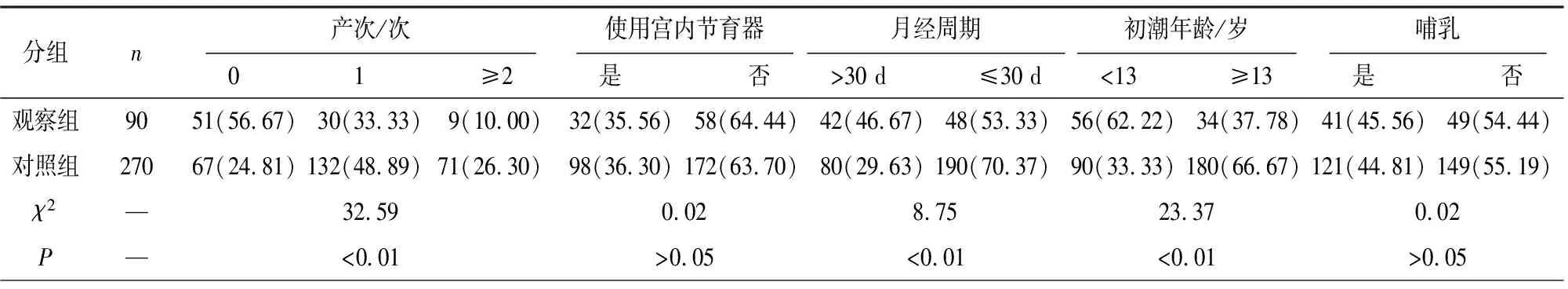
表2 观察组和对照组临床资料比较[n;构成比(%)]
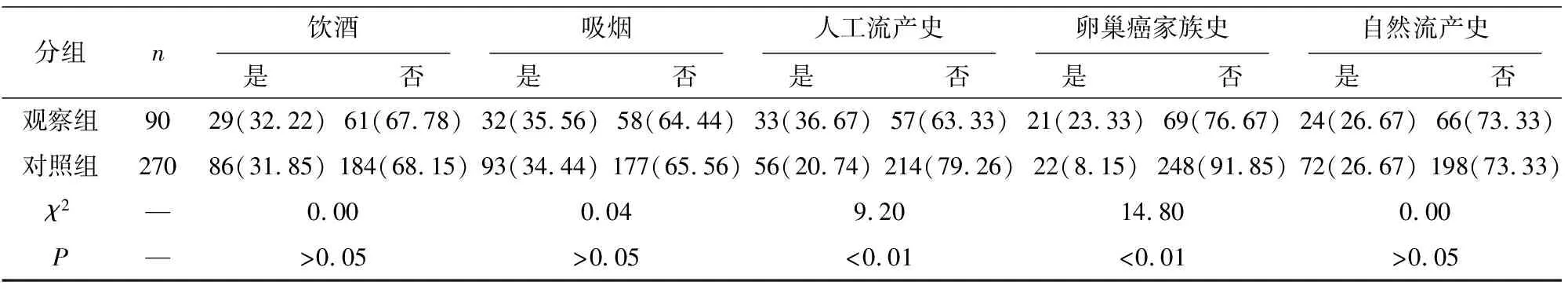
分组n饮酒 是 否 吸烟 是 否 人工流产史 是 否 卵巢癌家族史 是 否 自然流产史 是 否 观察组9029(32.22)61(67.78)32(35.56)58(64.44)33(36.67)57(63.33)21(23.33)69(76.67)24(26.67)66(73.33)对照组27086(31.85)184(68.15)93(34.44)177(65.56)56(20.74)214(79.26)22(8.15)248(91.85)72(26.67)198(73.33)χ2—0.000.049.2014.800.00P—>0.05 >0.05 <0.01 <0.01 >0.05
2.2 多因素分析 将单因素分析有统计学意义的指标作为自变量,是否为卵巢癌作为因变量(1=是,0=否)进行logistic回归分析,结果显示,产次≥2次、初潮年龄≥13岁是卵巢癌发生的保护因素(OR=0.664和OR=0.739,P<0.01),月经周期>30 d、人工流产史和卵巢癌家族史是卵巢癌发生的危险因素(OR=1.595、1.525、1.495,P<0.01)(见表3)。
3 讨论
临床上卵巢癌的整体发病率较高,同时卵巢癌的患病率及每年新发病例数量均明显的上升[7]。卵巢癌病人的3年内病死率明显上升,而其总体生存时间逐渐缩短[8]。手术治疗及术后联合化疗治疗,虽然能够在卵巢癌的治疗中发挥重要作用,但综合性治疗措施治疗后,卵巢癌病人的整体预后仍然无明显的改善。而对于相关预防措施的分析,不仅能够揭示卵巢癌的病情进展内在原因,同时还能够为临床上卵巢癌病人的早期预防提供现实性的措施。
不同的临床特征或者临床因素,能够通过影响到卵巢生发上皮的异常增殖、凋亡抑制或者免疫逃逸等过程,进而增加卵巢癌的发生风险。孕产史或者月经周期的紊乱,能够通过干预病人雌激素受体敏感性,影响到游离雌激素水平的波动,进而提高卵泡生发上皮细胞的持续性自我增殖速度,增加卵巢癌的发生率[9-10];自然流产或者人工流产,可能影响到了子宫内膜内环境,诱导细胞间质成分磷酸酶的释放速度,导致卵巢生发上皮细胞磷酸化的异常[11];卵巢癌的相关家族史,其近亲属或者直系亲属多携带有相关卵巢癌隐性癌基因,在病理性应激下降相关癌基因的激活,能够提高卵巢癌的发生风险[12]。而过早的月经初潮或者未孕的人群,其卵巢癌的保护性因素可显著减少,卵巢癌的发生率显著上升,但缺乏对于其他因素的全面性分析。
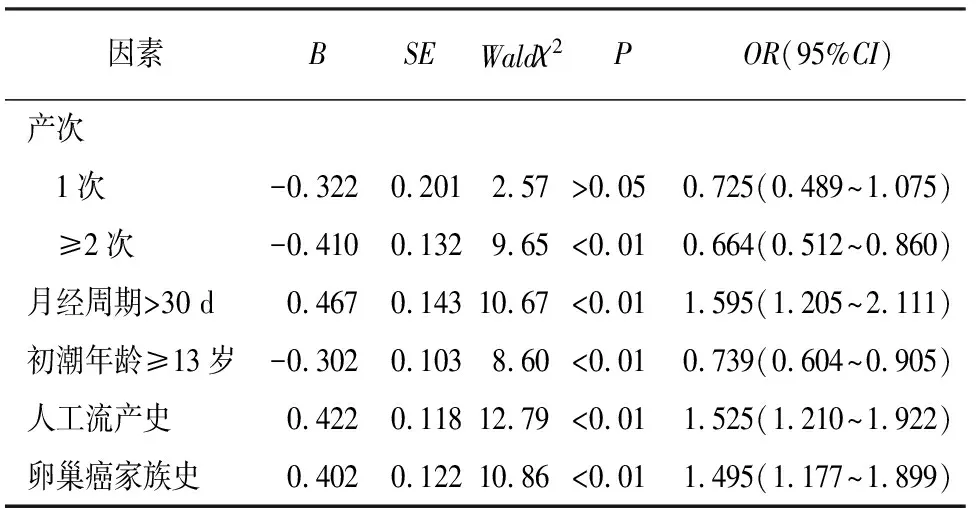
表3 卵巢癌的多因素logistic分析
本研究中观察组病人与对照组在年龄、婚姻状态等方面并无明显差异,排除了后天性的临床一般因素对于卵巢癌发生的影响。可以发现的是,产次为0次、月经周期>30 d、初潮年龄<13岁的人群,其发生卵巢癌的比例明显上升,高于产次较多、月经周期≤30 d或者初潮年龄较晚的人群,提示了孕产史或者月经史等因素对于卵巢癌发生的影响。我们继而探讨其原因,分析相关因素对于卵巢癌的发生影响,可能与下列几个方面的途径有关[13-14]:(1)未孕的人群,其体内孕激素的波动幅度较低,失去了对于雌激素的拮抗作用,导致雌激素的相对生理性活性较高,从而刺激了卵巢生发上皮细胞的持续性增殖;(2)月经周期紊乱或者较早月经来潮的人群,其基础雌激素水平存在明显的异常,游离雌激素水平的浓度较高,从而增加了卵巢生发上皮细胞核DNA的扩增速度。丁贤彬等[13]研究发现,在未分娩的人群中,卵巢癌的整体发病率可平均上升0.16%以上,另外在月经周期超过40 d的人群中,其卵巢恶性或者交界性肿瘤的发生率也明显上升。在具有人工流产病史或者卵巢癌家族史的病人中,其发生卵巢癌的风险明显上升,提示了二者对于卵巢癌的发生影响,这主要由于反复的人工流产,增加了盆腔内炎症性疾病的发生率,并能够促进炎症性因子对于卵巢的持续性刺激,从而增加了卵巢癌的发生率。临床上应指导已婚女性合理避孕,降低反复人工流产的次数。在具有卵巢癌家族史的人群中,可以通过早期血清学筛查,并每半年进行一次肿瘤标志物及妇科超声检查,进而提高具有卵巢癌家族史人群的卵巢癌早期诊断水平。最后危险因素分析可见,产次<2次、初潮年龄<13岁、月经周期>30 d、人工流产史和卵巢癌家族史均是卵巢癌发生的危险因素。
临床上可以针对相关高危因素的女性,早期进行筛查,并可以指导已婚女性早期受孕妊娠、及时调整月经周期、合理指导避孕,进而降低卵巢癌的发生率。

