2种高通量核酸检测方法多种呼吸道病原体检测效能比较
荆红波, 李 湛, 何 牧, 王彦波, 李 文, 马红梅
(北京市顺义区疾病预防控制中心微生物检验科,北京 101300)
急性呼吸道感染是一种常见的疾病,感染力强、传播速度快、发病率高。不同病原体呼吸道感染的临床症状极为相似,尤其是在不明原因呼吸道疾病爆发时,及时、准确地鉴定致病病原体是临床诊疗的关键。近年来,核酸检测技术已经成为快速诊断呼吸道病原体的首选方法,且多重病原体检测系统也越来越普及,TaqMan微流体芯片(TaqMan array card,TAC)技术作为国内外近几年研究较多的高通量病原体筛查技术[1-5],是一种基于384孔微流体卡片中单重定量PCR的微流控技术。本研究采用多重荧光定量聚合酶链反应(polymerase chain reaction,PCR)和TAC技术检测急性呼吸道感染病原体,比较2种方法的检测效能。
1 材料和方法
1.1 研究对象
按照北京市“传染病监测技术平台”发热呼吸道症候群监测方案病例定义的标准,收集2017年3月—2018年10月北京市顺义区医院发热门诊、呼吸内科门诊、急诊、儿科门诊就诊的流感样和肺炎患者临床样本419例。样本类型主要为上呼吸道咽拭子样本、下呼吸道灌洗液和痰液样本。采集后的临床样本立即保存于4 ℃冰箱,24 h内送检,未及时检测样本于-70℃保存。样本每月采集,每周均匀分布。
1.2 核酸提取
痰液样本采用痰消化液(英国Oxoid公司)消化待用;咽拭子样本震荡后直接采用QIAamp viral RNAmini kit(德国QIAGEN公司)提取病原体核酸,核酸提取后-80℃保存。
1.3 多重荧光定量PCR核酸检测
采用ViiA 7实时荧光定量PCR仪(美国Applied Biosystems公司)及呼吸道病毒核酸多重联检试剂盒、肺炎支原体和肺炎衣原体核酸多重检测试剂盒、肠道病毒核酸检测试剂盒(江苏和创生物科技有限公司)检测甲型流感病毒、新甲型H1N1流感病毒、H3N2流感病毒、乙型流感病毒、呼吸道合胞病毒、副流感病毒1型、副流感病毒2型、副流感病毒3型、副流感病毒4型、腺病毒、人偏肺病毒、鼻病毒、冠状病毒229E型+HKU1型、冠状病毒NL63型+OC43型、博卡病毒、肠道病毒、肺炎支原体和肺炎衣原体共18种病原体。
1.4 TAC 检测
采用军事医学科学院自主研发的定制TAC板对同一例临床样本进行呼吸道多种病原核酸检测,可检测的病原体包括甲型流感病毒、新甲型H1N1流感病毒、H3N2流感病毒、甲型流感病毒H5亚型、甲型流感病毒H7亚型、甲型流感病毒N9亚型、乙型流感病毒、呼吸道合胞病毒、呼吸道合胞病毒A型、呼吸道合胞病毒B型、副流感病毒1型、副流感病毒2型、副流感病毒3型、副流感病毒4型、腺病毒、人偏肺病毒、人偏肺病毒A型、人偏肺病毒B型、鼻病毒、冠状病毒229E型、冠状病毒HKU1型、冠状病毒NL63型、冠状病毒OC43型、博卡病毒、肠道病毒、肺炎支原体、肺炎衣原体、Q热立克次氏体、嗜肺军团菌通用型、肺炎链球菌、肺炎克雷伯菌、金黄色葡萄球菌、A族链球菌、流感嗜血杆菌、结核分枝杆菌、百日咳鲍特菌(包括Ⅰ相和Ⅱ相)等30余种。
按照AgPath-ID one-step RT-PCR kit(美国Applied Biosystems公司)说明书要求配置反应液体系。每个样本取20 μL的核酸提取液加入到80 μL的预混液中,混合并添加到TAC板上,离心后备用。采用ViiA 7实时荧光定量PCR仪进行扩增,扩增条件:45 ℃ 10 min;95 ℃10 min;95 ℃ 15 s,60 ℃ 45 s,40个循环。
1.5 结果判定
以出现“S”型扩增曲线且循环阈值(cycle threshold,Ct)≤38为阳性。如果2种方法检测结果一致,则认为该样本的检测结果是正确的。如果2种方法检测结果不一致,采用单一病原荧光定量PCR试剂盒进行复核,如果复核结果为阳性,确认复核结果并视为最终结果;如果复核结果是阴性,再次使用普通荧光定量PCR复核,确认复核结果并视为最终结果。
1.6 PCR复核
肺炎支原体、甲型流感病毒、乙型流感病毒、人偏肺病毒、腺病毒、呼吸道合胞病毒、鼻病毒、肠道病毒、副流感病毒3型采用单一病原荧光定量PCR试剂盒(江苏硕世生物科技有限公司)进行复核。对初次复核结果不一致的样本采用普通定量PCR扩增测序复核,参照相关文献设计鼻病毒[6]、肠道病毒[7]、副流感病毒3型[6]、甲型流感病毒[8]、乙型流感病毒[9]引物,采用iCycler PCR扩增仪(美国BIO-RAD公司)进行PCR扩增,扩增产物采用QIAxcel毛细管电泳仪(德国Qiagen公司)进行电泳,根据条带大小判定结果。
1.7 统计学分析
采用SPSS 20.0软件进行统计分析,以P<0.05为差异有统计学意义。
2 结果
2.1 多重荧光RT-PCR检测结果
419例样本中有126例阳性,阳性率为30.1%,其中96%(121/126)的阳性样本为单一病原感染,仅有4%(5例)为混合感染,均为2种病原共感染,分别为:肺炎支原体+鼻病毒(1例)、肺炎支原体+乙型流感病毒(1例)、肺炎支原体+肠道病毒(1例)、乙型流感病毒+鼻病毒(1例)、副流感病毒2型+人偏肺病毒(1例)。
2.2 TAC检测结果
419例样本中有117例阳性,阳性率为27.9%。96.6%(113/117)的阳性样本为单一病毒感染,3.4%(4例)为混合感染。混合感染中有3例为2种病毒混合感染,分别为2例鼻病毒+肠道病毒混合感染和1例副流感病毒2型+人偏肺病毒混合感染,1例鼻病毒+肠道病毒+肺炎支原体三重混合感染。除了病毒病原体外,TAC还能检测部分细菌。419例样本中有55例检出细菌,阳性率为13.1%,其中74.5%(41/55)为单一细菌感染,病原体包括19株金黄色葡萄球菌、7株肺炎链球菌、9株肺炎克雷伯菌、2株A族链球菌、3株百日咳鲍特菌和1株流感嗜血杆菌,有14株(25.5%)为2种以上细菌混合感染。419例样本中检出15例病毒和细菌的混合感染。
2.3 多重荧光定量PCR和TAC 检测结果比较
419例样本中有389例(92.8%)2种方法检测结果一致,其中阳性结果108例,阴性结果281例。仅有30例(7.2%)病毒检测结果不一致。
在2种方法检测结果不一致的30例样本中,复核之后的结果与多重荧光定量PCR一致18例,其中阳性结果16例、阴性结果2例;复核之后的结果与TAC检测结果一致11例,其中阳性结果9例、阴性结果2例。见表1。
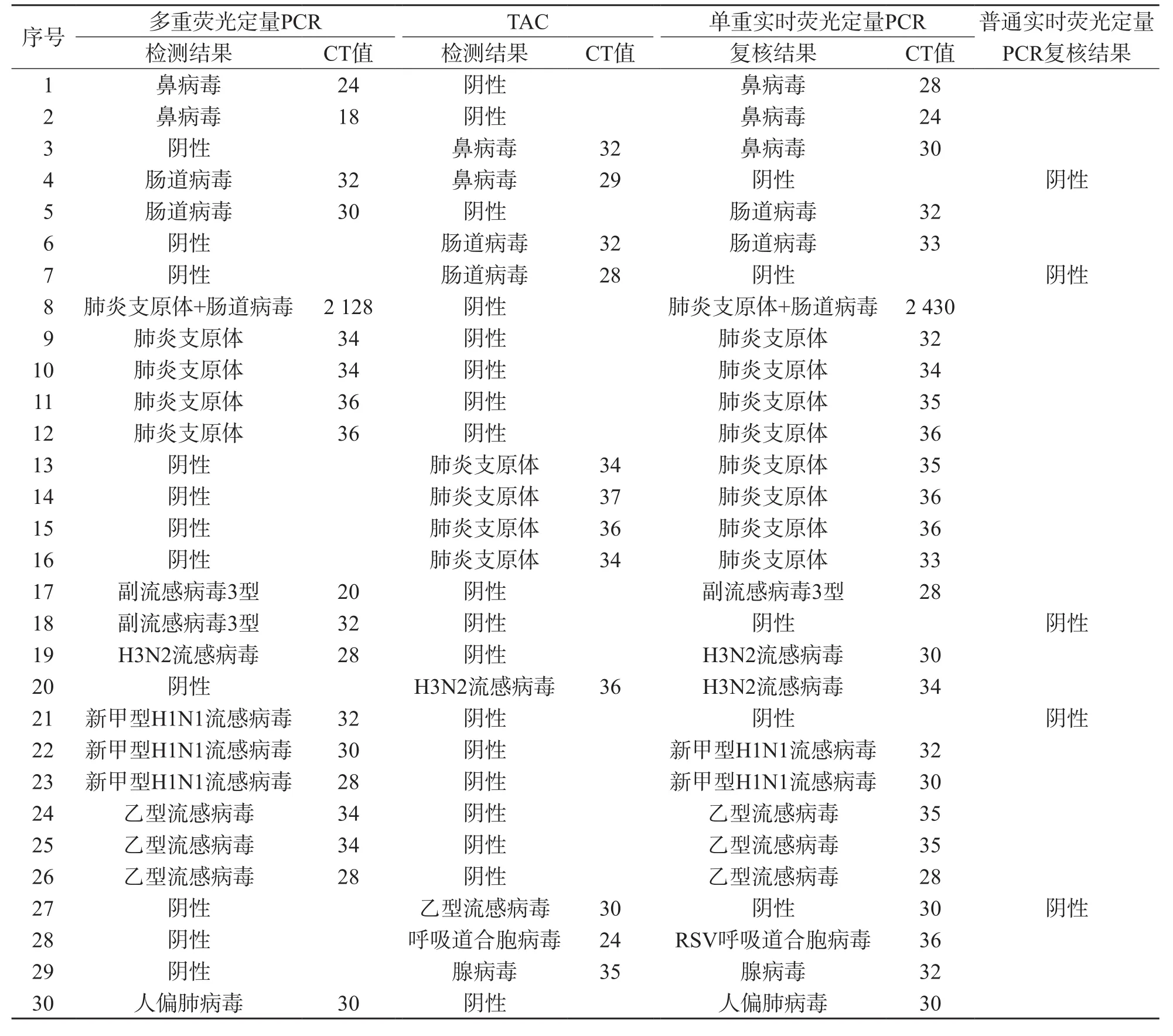
表1 2种方法不一致结果的复核情况
2种方法检测肺炎衣原体、1型和2型副流感病毒的敏感性和特异性均为100%。多重荧光定量PCR检测人偏肺病毒的敏感性和特异性均为100%,检测其他病毒的特异性均超过99%、敏感性均超过80%。TAC检测腺病毒的敏感性和特异性均为100%,检测其他病毒的特异性均超过99%,敏感性均为60%~90%。多重荧光定量PCR和TAC检测呼吸道病毒的敏感性分别为93.4%和87.4%,特异性分别为98.9%和98.9%,阳性预测值分别为97.7%和97.5%,阴性预测值分别为96.9%和94.3%。2种方法比较差异无统计学意义(P>0.05)。见表2、表3。
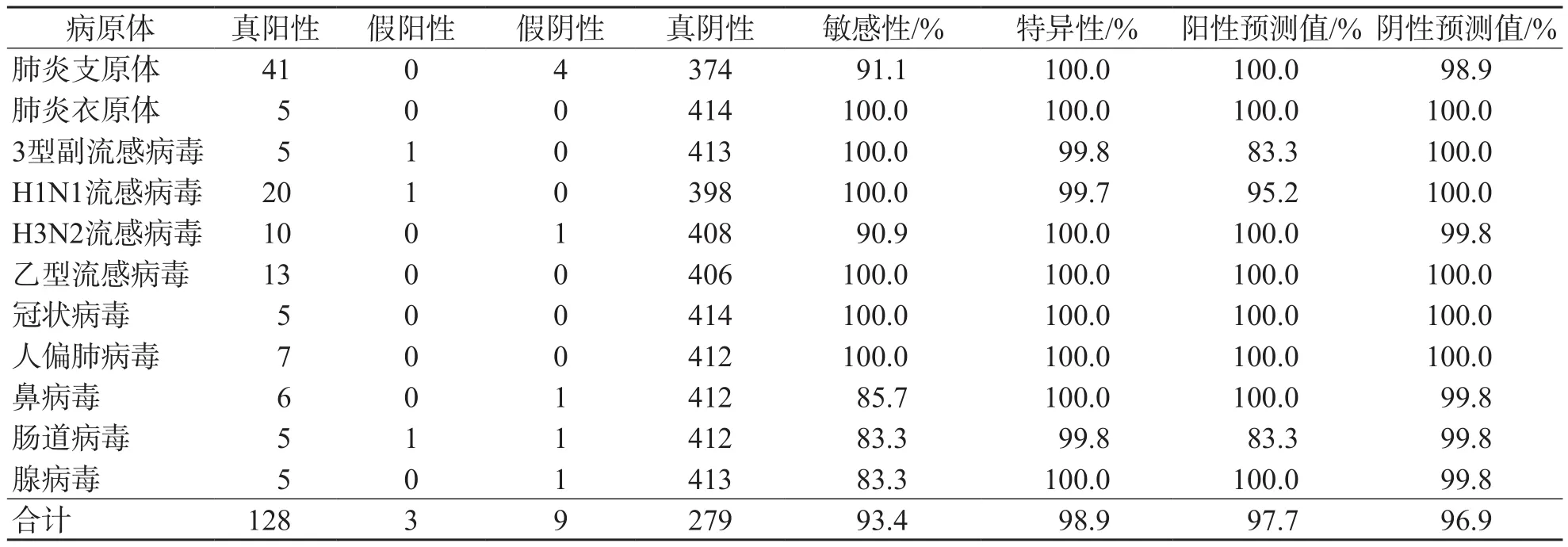
表2 多重荧光定量PCR对单一呼吸道病毒的检测性能
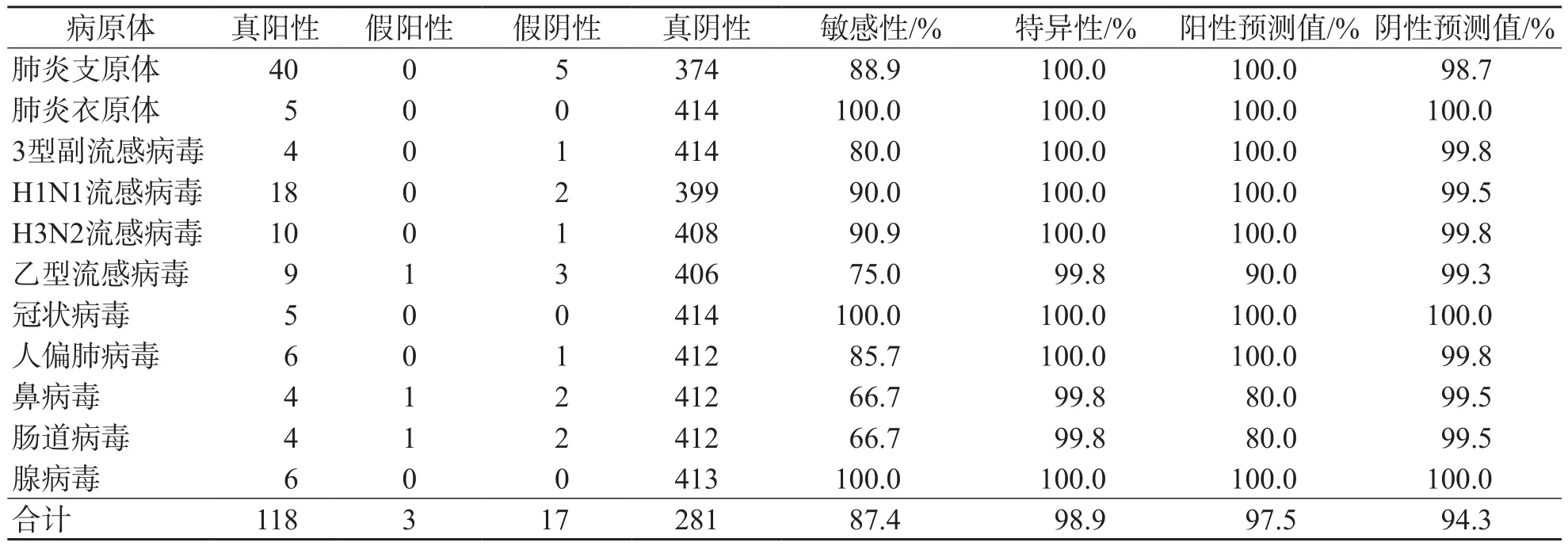
表3 TAC对单一呼吸道病毒的检测性能
3 讨论
多重荧光定量PCR是目前比较常用的检测呼吸道病毒的方法,而TAC是国内外近几年研究较多的一种高通量病原体筛查技术,1次可通过空间分布实现对384个目标的检测,被广泛用于呼吸道病毒、肠道细菌、疟疾和基因表达等研究中[2-5]。KODANI等[10]发现,TAC检测在呼吸道病原体的敏感性和特异性接近于实时PCR检测单一病原体的敏感性和特异性。STEENSELS等[11]发现,TAC技术呼吸道病毒的检出率明显高于常规的直接荧光抗体呼吸道病毒检测法。
本研究结果表明,2种方法检测单一病毒的特异性均接近100%,但TAC技术的检测敏感性,尤其是检测副流感病毒3型、乙型流感病毒、鼻病毒和肠道病毒的敏感性低于荧光定量PCR。可能由于TAC技术对所有的反应均采用同一个提取方法、PCR体系和反应条件导致的。而多重PCR可以根据不同病原体优化不同的实验条件,可能会更敏感地检测到某些病原体。
在不明原因的呼吸道感染中,细菌和病毒共感染会使病情更为复杂,迫切需要快速、准确地检测出致病病原体,TAC技术病原谱检测范围更为广泛,能同时对38种病原体进行检测,包括27种病毒、8种细菌和3种其他非经典微生物。TAC主要基于384孔板上的单重荧光定量PCR,相同的反应体系、相同的反应条件,每个孔的反应体积仅需要3 μL左右。多重荧光定量PCR可对16种病毒和2种其他病原体进行检测。此方法主要是基于单管多重扩增,将几种不同病原体的引物集中在同一个管中进行检测。本研究使用3种试剂盒,如检测TAC涵盖的其他病原体,则需要更多的试剂盒。因此相对来说,TAC检测的病原体种类更多一些,这在疾病监测,特别是暴发疫情的调查中,可以在短时间内完成对多个患者样本中38种病原体的检测,尤其可以快速检测到多种呼吸道病原体共感染的情况。而使用多重荧光定量PCR进行如此多的病原体检测,需要花费更多的时间,也增加了检测成本。因此,当呼吸道疾病的病因未知或怀疑多种病原体共同感染时,TAC技术是实现快速筛查的有效方法。
本研究对2种方法的操作简便性和时效性进行了比较,2种方法样本处理及核酸提取的过程相同,结果判读都是依据Ct值。TAC技术1次能同时检测38种病原体,但每次只能检测8个样本;多重荧光定量PCR 1次能同时检测18种病原体,但每次最多检测18个样本。操作步骤方面,TAC技术操作简便,仅需一步操作即可完成;而多重荧光定量PCR需要配置多个试剂盒,需要手工操作的步骤比较多。仪器要求方面,TAC技术完成所有病原体的检测仅需要1台荧光定量PCR仪,1.5~2 h即可完成,但如果同时检测多个病原体需要的时间也会相应增加;多重荧光定量PCR需要2台荧光定量PCR仪,2.5~3 h完成,如果需要进行更多的病原体检测,也需要更多的时间或更多的仪器。因此,在实际应用中,可根据实际情况来选择合适的方法。
本研究因未找到相应的呼吸道细菌检测试剂盒,仅比较了2种方法在多种呼吸道病毒和2种其他病原体检测方面的性能,没有比较呼吸道细菌检测的性能,具有一定的局限性。本研究结果显示,TAC技术对金黄色葡萄球菌和肺炎链球菌的检出率较高,与国外报道[6]相似。虽然尚不清楚是否与疾病相关,但国外有报道肺炎链球菌在病例组和正常对照组中都能被检测到,且检出率相近,是否是引起疾病的原因尚待进一步分析[12]。本研究检出3例百日咳鲍特菌感染病例,且得到了临床的证实,并根据检测结果及时控制了病情。
综上所述,TAC技术与多重荧光定量PCR常见呼吸道病毒检测的敏感性和特异性相近,但TAC技术病原谱的检测范围更广,在紧急情况下可作为快速筛查多种呼吸道病原体的有效方法。

