精准肝切除术对老年原发性肝癌患者血清Ⅲ型胶原前肽、细胞间黏附分子-1水平的影响
陈俊辉 吴军 钱叶本
(1安徽医科大学第一附属医院肝胆胰外科,安徽 合肥 230022;2芜湖市第二人民医院急诊外科)
肝癌是指发生于肝脏组织的消化系统恶性肿瘤,主要发病群体为中老年,且男性多于女性〔1,2〕。而原发性肝癌的主要发生部位为肝脏上皮或间叶组织,是发病率及病死率极高的恶性肿瘤。据统计,原发性肝癌的死亡率处于第三,仅次于胃癌及食道癌,现已成为危害人类身心健康及生命安全的重要恶性肿瘤疾病之一〔3,4〕。血清Ⅲ型胶原前肽(PⅢP)、细胞间黏附分子(ICAM)-1水平是临床诊断肝癌的两种重要参考指标。临床通常采用手术对原发性肝癌进行治疗,如肝切除术等,但传统肝切除术对患者的身体创伤较大,且术后患者出现并发症的概率较高,临床治疗效果不理想〔5〕。精准肝切除术是通过综合应用整套的现代科学理论和技术研究所得到的产物,在临床应用越来越广泛,但临床对该手术方法的研究还鲜为少见。本研究探讨精准肝切除术对原发性肝癌患者PⅢP、ICAM-1水平的影响。
1 资料与方法
1.1一般资料 选取2016年2月至2018年7月于安徽医科大学第一附属医院就诊的老年原发性肝癌患者80例,参照随机数字表法分为对照组40例和观察组40例。对照组男29例,女11例;年龄60~78〔平均(68.83±2.21)〕岁;肿瘤直径1~9〔平均(4.51±1.26)〕cm;体重指数17~26〔平均(21.43±1.06)〕kg/m2;TNM分期:Ⅰ期16例、Ⅱ期24例;发病部位:19例肝右叶前段、21例肝左外叶。观察组男28例,女12例;年龄61~78〔平均(68.87±2.25)〕岁;肿瘤直径1~10〔平均(4.56±1.29)〕cm;体重指数17~27〔平均(21.45±1.08)〕kg/m2;TNM分期:Ⅰ期21例、Ⅱ期19例;发病部位:18例肝右叶前段、22例肝左外叶。两组一般资料比较差异无统计学意义(P>0.05),具有可对比性。
1.2纳入和排除标准 纳入标准:①符合《原发性肝癌诊疗规范(2011版)摘要》〔6〕中相关诊断标准;②经病理学检查确诊为原发性肝癌;③凝血功能正常者。排除标准:①肝内或向其他远处转移者;②合并心、肝、肾等重要脏器功能严重损害者;③精神疾病史;④原发性肝癌肝门淋巴结转移者;⑤随访期间脱落者。
1.3方法 两组术前均给予抗病毒及保肝等治疗措施。对照组采用传统肝切除术进行治疗,具体内容如下:所有患者采用气管插管全身麻醉,手术体位取仰卧位,常规消毒,铺手术巾。根据患者术前确认的肿瘤组织位置,选用腹部正中切口、右上腹反L形切口逐层入腹,将肿瘤组织完全显露在视野范围内,并对第一、二肝门进行阻断,同时对大血管及肝门给予夹闭操作,分离肝圆韧带、镰状韧带等周围韧带,之后在距肿瘤组织边缘约2 cm位置进行切除手术,由浅至深、由里向外,切除完成后结扎或缝扎创面的残留血管及胆管。之后对创面反复清洗,并观察是否出现出血及胆瘘现象,最后进行止血、放置腹腔引流管及关腹等操作。术后给予镇痛、保肝及减轻腹腔积液等治疗。观察组采用精准肝切除手术进行治疗,具体内容如下:所有患者采用气管插管全身麻醉,手术体位取仰卧位。根据患者术前经超声造影剂、模拟肝切除残肝体积测定及CT血管三维成像等检查对手术切除范围进行精准确认。首先将肝周韧带充分游离后,再进行B超检查对肿瘤深度及范围、对周围组织的侵犯程度及是否存在转移的状况进行确认,进一步对切除范围进行确认。对第一肝门进行仔细解剖并分离,并结扎或阻断预切除侧半肝或相应肝叶的肝动脉和门静脉分支,对半肝缺血界限采用电刀进行标记。在手术过程中采用超声对肿瘤附近的主要肝静脉支进行定位,并选用电刀标记其于肝表面走向。若半肝缺血界限较为模糊,且再次采用超声对肝中静脉进行定位后再对切除平面进行确认。若肿瘤组织与第二肝门较近,将第二肝门和肝右静脉根部进行充分游离,同时为了避免发生出血过多现象,采用无损伤血管钳对肝静脉血流进行掌控。之后选用电刀对断肝平面进行标记,控制中心静脉压的范围不超过5 cmH2O,同时采用超声刀及水刀等器械,由浅至深、由前至后对肝组织逐步进行切断。并且在手术过程中,注意对肝静脉属支及主干进行保护,避免出现撕裂损伤出血等现象,同时采用双极电直接凝固切断直径≤3 mm的脉管,对>3 mm的脉管给予Keiil钳钳夹进行切断,切断后并进行结扎或缝扎。切除完成后将入、出肝血流放开,提高中心静脉压。缝扎断肝创面出血及胆瘘部位,之后将腹腔引流管置入,手术结束。术后叮嘱患者早期下床活动及尽早进食,有助于术后恢复。两组术后均随访1年。
1.4评价指标 ①血清因子:分别采集两组术前及术后1 w的空腹静脉血3 ml,并进行离心措施,离心后取上清液,采用全自动酶标仪(北京普朗新技术有限公司,型号:DNM-9602G)对ICAM-1、PⅢP进行检测评估。②免疫功能:分别采集两组术前及术后3 d的空腹静脉血4 ml,进行离心操作,设置离心速度为3 000 r/min,离心时间为10 min,离心完毕后取上清液。采用流式细胞仪(北京东迅天地医疗仪器有限公司,型号:BD FACSCalibur)对CD3+、CD4+,上海康朗生物科技有限公司提供的试剂盒对免疫球蛋白(Ig)A、IgG、IgM水平进行检测评估。③并发症:观察并记录两组患者术后1 w内出现的并发症,主要包括切口感染、胸腔积液、消化道出血、胆汁漏。④观察并记录两组随访1年的肿瘤复发状况。
1.5统计学方法 采用SPSS24.0软件进行t及χ2检验。
2 结 果
2.1两组血清因子比较 术后两组ICAM-1及PⅢP明显低于术前,且观察组ICAM-1及PⅢP明显低于对照组,差异有统计学意义(均P<0.05)。见表1。
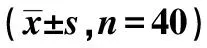
表1 两组手术前后血清因子比较
与同组术前比较:1)P<0.05,下表同
2.2两组免疫功能比较 术后两组CD3+、CD4+、IgA、IgG及IgM值明显低于术前,且观察组CD3+、CD4+、IgA、IgG及IgM值明显高于对照组,差异均有统计学意义(均P<0.05)。见表2。
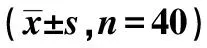
表2 两组手术前后免疫功能比较
2.3两组并发症比较 观察组并发症总发生率明显低于对照组,差异有统计学意义(P<0.05)。见表3。
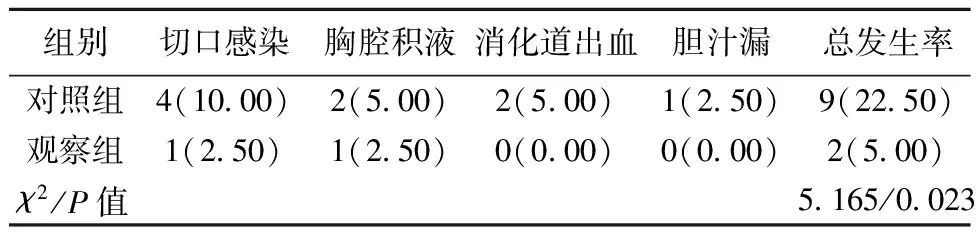
表3 两组并发症状况比较〔n(%),n=40〕
2.4两组复发率比较 随访1年后观察组复发率〔1例(2.50%)〕明显低于对照组〔8例(20.00%)〕,差异有统计学意义(χ2=4.507,P=0.013)。
3 讨 论
肝细胞型肝癌、胆管细胞型肝癌及混合型肝癌是原发性肝癌的3种类型,其中肝细胞肝癌在我国占全部原发性肝癌的90%以上〔7〕。临床对原发性肝癌的发病原因尚不明确,但有研究表明,乙型肝炎病毒(HBV)、丙型肝炎病毒(HCV)感染、酒精、肝硬化及微量元素等均会诱发肝癌〔8,9〕。早期原发性肝癌患者无明显特异性临床表现,当患者出现明显身体不适感时,病情往往已发展至中晚期,患者会出现肝区疼痛、腹胀、乏力、消瘦及上腹部包块等临床表现,部分患者还存在低热、上消化道出血等症状,随着病情发展,患者极易发生上消化道出血、肝癌破裂出血及肝肾衰竭等并发症,严重威胁了患者身心健康及生命安全〔10,11〕。因此,对原发性肝癌患者给予合理有效的治疗措施对提高患者预后状况具有重要意义。手术方法是临床治疗原发性肝癌最常用且最有效的治疗手段,传统肝切除术即为治疗原发性肝癌的手术方法之一,其可有效清除肿瘤组织,改善患者病情,但该手术方法对患者的身体创伤较大,且患者术后会发生肠源性内毒素血症等并发症,降低了患者预后,临床治疗效果不理想〔12,13〕。而精准肝切除术是医疗科学技术发展所得到产物,主要以高度发达生物医学和信息科学技术为基础所产生的一种新型肝脏外科手术,相比于传统肝切除手术具有手术时间短、术后引流量少及术后恢复快等优点。精准肝切除术不仅能够彻底清除肿瘤组织,同时还能保证剩余肝脏解剖结构的最大完整性和功能性,并且手术过程中的出血量较少,可有效保护周围组织,避免造成不必要的损伤,最终使患者获得最佳的治疗效果,利于提高患者的预后状况〔14,15〕。本研究结果表明采用精准肝切除术对原发性肝癌患者进行治疗,患者的ICAM-1、PⅢP水平得到了明显降低,且能够有效改善患者病情,有利于促进患者恢复,安全性较高。ICAM-1是最早发现的免疫球蛋白超级家族黏附分子之一,临床认为其是免疫细胞裂解靶细胞的辅助分子,有研究表明,ICAM-1与原发性肝癌的转移具有密切关系〔16〕。PⅢP能够加快术后残留组织的纤维化,从而提高其他组织器官出现并发症的概率。由于老年原发性肝癌患者的自身免疫功能下降,而患者接受手术治疗后会进一步促进免疫功能降低,从而大幅度提升了患者发生感染等并发症的概率,患者出现不良结局的概率也随之提升〔17〕。T淋巴细胞亚群可准确反馈机体内的免疫功能状况,是判断机体内免疫功能是否处于平衡状态的指标,其中CD3+是主要的活性细胞,CD4+是辅助性T淋巴细胞,其水平下降越多则表明机体免疫功能损伤越严重〔18〕。免疫系统主要由免疫组织、器官、免疫细胞及免疫活性分子等成分组成,其中免疫球蛋白是免疫活性分子中的一类,主要存在于黏膜组织中,包括消化、呼吸及泌尿生殖系统。临床将免疫球蛋白分为5种类型,主要包括IgG、IgA、IgM、IgD及IgE,而免疫调节主要通过IgA、IgG与IgM等阻止病原体与细胞结合从而发挥作用,尤其是IgG。

