L-精氨酸衍生物的合成及其性质研究
刘晓菊,王金玺,任国瑜,弓 莹
(榆林学院化学与化工学院, 陕西 榆林 719000)
氨基酸在许多领域的意义都非常重大[1-2],如在医学治疗方面,精氨酸可以治疗肝机能障碍;组氨酸可以缓解心绞痛、心功能不全等疾病;半胱氨酸可以促进头发的生长。L-氨基酸希夫碱含有多个强电负性配位原子,并具有较强的配位能力和多样的配位模式等优点。希夫碱类化合物因含有多种活性基团而具有独特的生理学活性,其过渡金属配合物具有良好的抗菌、抗癌活性,并在药物研究方面受到广泛关注[3-5]。同时在催化领域、光学领域、分析化学领域等都有很好的发展前景,已经成为当代配位化学研究热点之一。
本文以L-精氨酸和香兰素为原料,设计合成新型的具有手性的希夫碱配体L,其次配体分别与金属盐BaCl2、(CH3COO)2Ni·2H2O、(CH3COO)2Zn·2H2O进行络合反应,得到3种新型的金属配合物,通过红外分析、荧光分析和元素分析对形成的希夫碱及其金属衍生物进行表征,从而推断出其可能的化学结构,并用紫外漫吸收进而研究光催化性质。
1 实验部分
1.1 仪器与试剂
TU-1201紫外可见分光光度计,北京普析通用仪器有限责任公司;RF-5301PC荧光分光光度计,日本岛津公司;AXIMA-CFR plus MALDI-TOP Mass Spectrometer飞行质谱仪,岛津集团英国克雷斯托分析仪器公司;德国艾乐曼VarioEL Ⅲ元素分析仪;EQUINOX-55傅立叶红外光谱仪,干燥KBr压片,德国布鲁克公司;VARIANINOVA-400核磁共振仪,溶剂DMSO,美国Varian公司。试剂为市售分析纯试剂,溶剂为市售工业级试剂,并对所有溶剂进行无水处理;用自制的薄层色板。
1.2 实验过程
1.2.1 希夫碱配体L的合成
首先称取0.174 g(1 mmol)L-精氨酸放入三颈瓶(150 mL)反应器中。再用量筒称取15 mL甲醇加入反应器中。在控温磁力搅拌器上连接冷凝管和三颈反应器,加热回流,控制反应器温度为60 ℃。待反应0.5 h后加入0.062 g(1 mmol)氢氧化钾继续反应。0.5 h后氢氧化钾完全溶于溶液,称取0.152 g(1 mmol)香兰素加入反应器中,溶液变为白色,反应3 h后溶液由淡黄色变为深橘色。等冷却后对其过滤,滤纸上无沉淀析出,烧杯中的液体静置三天后,所得固体为橙黄色0.28 g。产率:85%,IR (KBr,cm-1) ν:1625.3,2998,2964,2899,2711,1581,1503。LC-MS(M+1) C14H14KN3O4理论值327.06;实验值327.00。元素实验值(%):C,51.40;H,4.31;K,11.90;N,12.84;O,19.55。
1.2.2 希夫碱配体L与锌金属配合物
在三颈烧瓶中加入希夫碱配体L 0.327 g(1 mmol)和10 mL甲醇,加热搅拌使其全部溶解,加入乙酸锌0.183 g(1 mmol),溶液呈乳白色,回流3 h后反应器底部有白色沉淀析出,液体呈红色。过滤后对滤纸上的沉淀和烧杯中的液体静置三天后得到白色固体0.35 g,产率75%;IR (KBr,cm-1), ν: 1620,577。C16H19ZnKN3O7理论值(%):C,40.90;H,4.08;K,8.32;N,8.94;O,23.84;Zn,13.92。 实验值(%):C,40.86;H,4.12;K,8.31;N,8.95;O,23.86;Zn,13.90。
1.2.3 希夫碱配体L与钡金属配合物
在三颈烧瓶中加入希夫碱配体L 0.327 g(1 mmol)和10 mL甲醇,加热搅拌使其全部溶解,加入0.244 g(1 mmol)氯化钡,溶液由黄色变为草咖啡色,反应3 h后反应器底部无沉淀析出,液体呈咖啡色。过滤滤纸上有咖啡色固体,对烧杯中的液体及滤纸上的固体放在干燥箱内进行静置干燥得到烧杯中的固体为咖啡色,滤纸上的固体得淡咖啡色固体0.40 g。产率80%;IR(KBr,cm-1),ν:1677,586。C14H14BaClKN3O4理论值 (%):C,33.62;H,2.82;Ba,27.46;Cl,7.09;K,7.82;N,8.40;O,12.80。实验值(%):C,33.60;H, 2.84;Ba,27.50;Cl,7.05;K,7.80;N,8.41;O,12.81。
1.2.4 希夫碱配体L与镍金属配合物
在三颈烧瓶中加入希夫碱配体L 0.327 g(1 mmol)和10 mL甲醇,加热搅拌使其全部溶解,加入0.248 g(1 mmol)C2H11NiO6,溶液由黄色变为草绿色,反应2.5 h后反应器底部无沉淀析出。溶液呈草绿色。过滤后滤纸上无残留固体,对烧杯中的液体静置干燥三天后得到草绿色固体0.33 g。产率65%;IR(KBr,cm-1),ν:1669,582。C18H20KN3NiO8理论值(%):C,42.88;H,4.00;K,7.76;N,8.33;Ni,11.64;O,25.39。实验值(%):C,42.80;H,4.08;K,7.70;N,8.39;Ni,11.60;O,25.43。
2 结果与讨论
2.1 红外光谱数据分析

2.2 荧光光谱数据分析
目标化合物荧光光谱图如图1所示。从图1可知,希夫碱配体L有两个荧光发射峰,分别在404 nm和433 nm,希夫碱配体L与氯化钡的配合物有两个发射峰,分别为401 nm和430 nm,希夫碱配体L与乙酸锌的配合物和希夫碱配体L与乙酸镍的配合物都有一个发射峰,分别为400 nm、402 nm,三种配合物与希夫碱配体L相比均发生了红移,其中希夫碱配体L与氯化钡的配合物红移最明显,在430 nm处。由此推测希夫碱配体L与金属盐发生了络合反应,而且与不同的金属络合生成的配合物的荧光性质也有区别,这与红外,紫外漫反射结果一致。
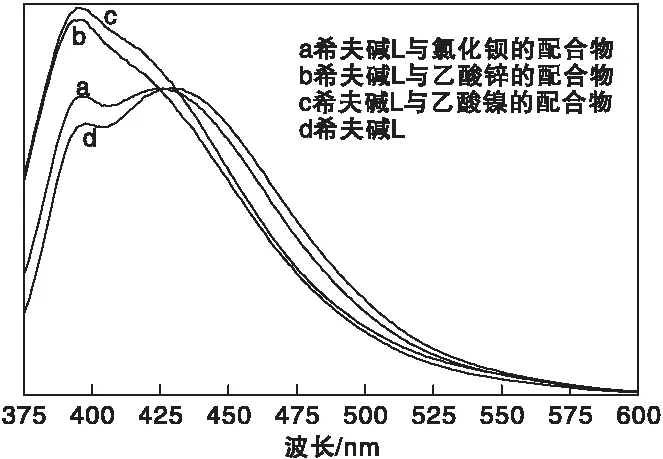
图1 目标化合物在甲醇/水 (体积比1∶1) 溶液中荧光光谱图Figure 1 Fluorescence emission spectra of the title complexes in CH3OH/H2O (1∶1) solution 浓度5×10-6mol·L-1,激发波长397 nm
2.3 紫外漫反射吸收光谱数据分析
目标化合物紫外漫反射吸收光谱图如图2所示。
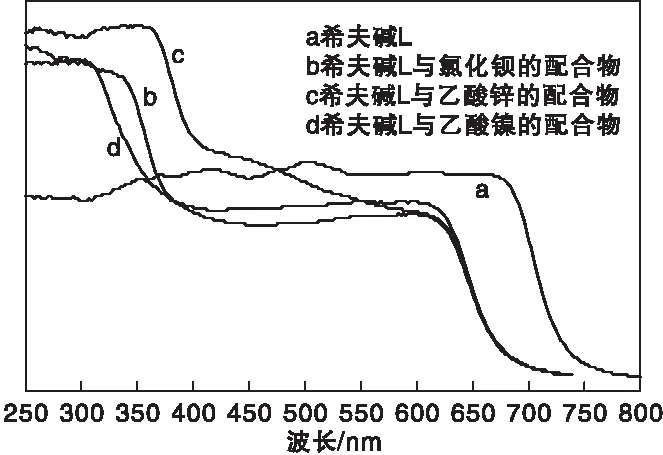
图2 目标化合物紫外漫反射吸收光谱图Figure 2 UV diffuse reflection spectra of title complexes
由图2可知,希夫碱配体L在(260~740) nm均有紫外吸收。希夫碱配体L金属配合物在(260~650) nm均有紫外光吸收,其中希夫碱配体L与乙酸锌的金属配合物具有最强的紫外光吸收强度,希夫碱配体L与乙酸镍的金属配合物具有最弱的紫外光吸收强度,推测希夫碱配体L及其金属配合物均可以作为光催化剂材料。
3 结 论
以L-精氨酸和香兰素为原料,合成新型的具有手性希夫碱配体L,然后配体L分别与乙酸锌、氯化钡和C2H11NiO6进行配位反应。得到3种新型的具有手性的希夫碱金属配合物 C16H19ZnKN3O7、C14H14BaClKN3O4和C18H20KN3NiO8。用红外光谱和元素分析表征和确认化合物的结构,用紫外漫反射吸收研究了其性质,数据表明希夫碱配体L在(260~740) nm均有紫外吸收,但与希夫碱L金属配合物差别不大。由紫外吸收强度分析可知,希夫碱金属配合物均比配体L具有更强的紫外光吸收强度,其中希夫碱L与乙酸锌的金属配合物具有最强的紫外光吸收强度,希夫碱配体L与乙酸镍的金属配合物具有最弱的紫外光吸收强度,推测金属络合物和希夫碱均适合做光催化材料,但是金属配合物应用潜力更大。这将是课题组下一步的深入研究内容。

