广西2株H9N2亚型猪源流感病毒的HA基因序列分析
孔子荣,李 凡,李三木,何奇松,曾咏芳,杨可妍,冯淑萍 ,孙翔翔,熊 毅,颜健华*
(1.广西大学动物科学技术学院,广西 南宁 530004;2.广西大学医学院,广西 南宁 530004;3.广西动物疫病预防控制中心,广西 南宁 530001)
【研究意义】猪流感病毒(Swine influenza virus,SIV)可引起猪群暴发急性、高度接触性传染病,属于正粘病毒科A型属单股负链分节段RNA病毒,由8个独立RNA片段组成,分别编码流感病毒结构蛋白(PB2、PB1、PA、HA、NP、NA、M1和M2)和非结构蛋白(NS1和NS2)[1]。20世纪70年代之前,猪流感主要在欧美大陆以地方性方式流行,之后传到我国,迄今已遍布世界各地。SIV在以不为人知的速度和方式悄然进化,而猪作为“混合器”和“孵育器”[2],扮演着流感病毒进化的中间宿主角色。在猪群中流行的流感病毒亚型包括H1N1、H3N2、H1N7、H4N6、H5N1和H9N2等,而H9N2亚型流感病毒相对于H5N1亚型流感病毒更容易跨越物种屏障,可在人群中传播[3]。因此,对SIV进行序列分析不仅对其流行防控意义重大,还具有重要的公共卫生学意义。【前人研究进展】流感病毒8个基因节段中的HA基因编码血凝素蛋白,该蛋白是流感病毒重要的表面蛋白,可与靶细胞表面的唾液酸受体位点结合,帮助病毒颗粒黏附于细胞表面而侵入细胞,种间传播的机制取决于HA序列上受体结合位点与宿主细胞表面病毒受体的结合特性[4]。HA蛋白的裂解性、受体特异性和糖基化是决定流感病毒感染性和致病性的重要因素[5],因此HA基因研究是流感病毒研究工作的重要热点。较多学者对各亚型流感病毒也进行了流行病学调查及基因组测定等研究[6],如魏东等[7]建立H9N2亚型猪流感病毒感染BALB/c小鼠动物模型,为研究病毒致病机制提供模型动物;殷斌等[8]对山东H9N2亚型猪流感病毒进行了分离鉴定及遗传进化分析;刘晓敏等[9]建立了禽源H9N2亚型猪流感病毒反向遗传操作技术平台;孙王杨吉等[10]对江苏分离的1株H9N2亚型猪流感病毒进行了遗传进化和致病性分析。张玉霞等[11]对分离的1株产蛋高峰鸡H9N2进行HA基因序列分析,发现目前H9N2病毒亚型呈现变异趋势,毒力虽未增强,但能逃避某些疫苗所诱导抗体的保护作用。张瑞华等[12]利用表达的H9N2亚型猪流感病毒HA重组蛋白,建立了H9亚型猪流感病毒抗体的LAT检测方法。【本研究切入点】近年来,低致病性H9N2亚型流感病毒的宿主范围越来越宽,对HA基因的研究在疫情监测和跨种间传播机制等方面均具有重要意义,但目前国内缺乏猪源H9N2流感病毒的HA基因分析数据。【拟解决的关键问题】对2011年从广西百色某猪场分离获得的2株H9N2猪流感病毒分离株的HA基因进行同源性比对、进化分析和编码蛋白氨基酸重要功能位点阐述,了解广西H9N2亚型SIV的分子生物学特征及病毒的遗传变异特点,为广西猪流感疫情监控和人流感的防控提供参考依据。
1 材料与方法
1.1 试验材料
H9N2病毒株A/swine/Guangxi/P2/2011和A/swine/Guangxi/P3/2011(以下称P2和P3)均由广西动物疫病预防控制中心从广西百色市乐业县送检的猪肺脏组织病料分离鉴定并保存。SPF鸡胚购自北京梅里亚维通实验动物技术有限公司。
主要试剂及引物:RNA提取试剂盒及质粒提取试剂盒购自天根生化科技(北京)有限公司;AMV反转录酶及相关试剂、TaqDNA聚合酶和pMDl8-T载体等购自宝生物工程(大连)有限公司。用于扩增H9亚型猪流感病毒HA全基因的引物由宝生物工程(大连)有限公司合成,引物序列见表1。
1.2 HA全基因测序及分析
将已分离鉴定病毒株的种毒使用PBS液稀释1000倍后,按每枚0.2 mL接种9日龄SPF鸡胚,收取24~96 h鸡胚的尿囊液,对经血凝试验鉴定为流感病毒阳性鸡胚尿囊液进行病毒总RNA提取。使用随机引物Uni12反转录合成的cDNA为模板,进行PCR扩增全长HA基因片段。再经1 %琼脂凝胶电泳后回收PCR产物进行pMDl8-T克隆,鉴定为阳性的克隆质粒送至生工生物工程(上海)股份有限公司进行测序,最后利用DNAstar对测序结果进行序列拼接和分析,并以MEGA 5.0绘制遗传进化树。
2 结果与分析
2.1 广西分离株HA基因序列的测定结果
经序列测定,P2和P3分离株的HA基因全长1701 bp,开放阅读框(ORF)全长1683 bp,共含有560个氨基酸。分离株和24株参考序列核苷酸和氨基酸的同源性比对结果见表2。其中,在与禽源H9N2亚型流感病毒比较中,P2和P3分离株与A/ChickeiVFiyian/G9/09的核苷酸同源性最高,为98.3 %,氨基酸同源性最高,为98.2 %,二者与北美分离株A/Turkey/Wisconsin/1/66的同源性最低;在与人源H9N2亚型流感病毒的同源性比较中,核苷酸同源性在87.5 %~92.7 %,氨基酸同源性在88.1 %~90.1 %;在与猪源H9N2亚型流感病毒的比较中,与A/Swine/Shanghai/Yl/2009的同源性最高,与A/Swine/Korea/Y452/2004的同源性最低,核苷酸同源性在83.7 %~94.8 %,氨基酸同源性在86.6 %~97.0 %。
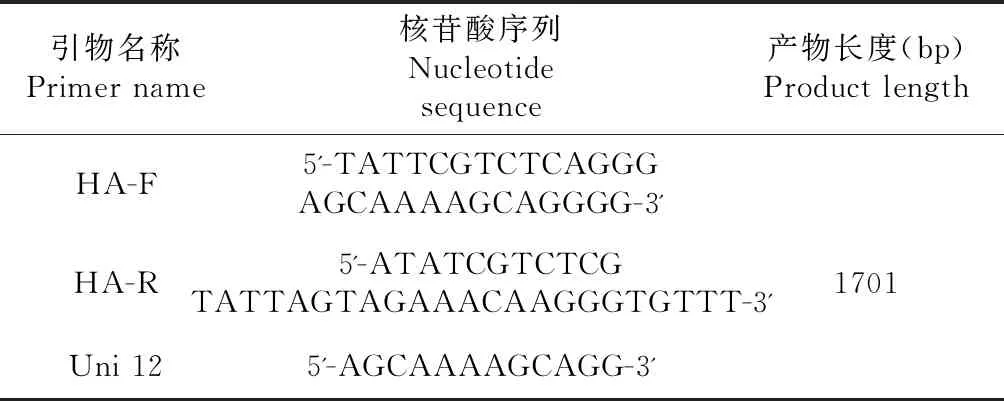
表1 引物序列
2.2 HA基因的遗传进化分析结果
从图1可看出,P2和P3分离株的HA基因与A/Duck/HongKong/Y280/97病毒同属欧亚谱系的Y280亚系;与BJ型代表毒株A/Chicken/Beijing/1/94、A/Chicken/HongKong/G9/97和A/Chicken/Shanghai/F/98等亲缘关系较远,与代表毒株A/Duck/HongKong/Y439/97和A/Quail/HongKong/Gl/97的亲缘关系最远。
2.3 HA基因的受体结合位点和裂解位点分析
由表3可知,H9N2亚型猪源流感的HA蛋白裂解位点位于335~341 aa间,2株分离株的裂解位点附近氨基酸均为-RSSRGLF-;HA蛋白球状受体结合位点由第109、161、163、191、198、202、203、146~150和232~237位氨基酸构成;与参考毒株比较,109、161、163、202和203位较保守;第198位与CK/HK/G9/97和CK/SH/F/98均为精氨酸(R),表明198位点对受体结合的亲和力具有影响,亲和力排序为缬氨酸(V)>苏氨酸(T)>精氨酸R[13];第234位发生了谷氨酰胺(Q)→亮氨酸(L)变化,前者存在于禽流感病毒中,后者存在于人流感病毒中。因此,广西的P2和P3分离株具有与人和猪流感受体结合的特性。
表3 HA连接肽序列及病毒结合受体结合的相关氨基酸
注:-代表潜在糖基化位点缺失,+代表潜在糖基化位点不缺失。
Note:- stands for potential glycolation site absent,+ stands for not missing.
2.4 HA基因糖基化位点分析
分离株HA蛋白具有8个保守的潜在糖基化位点,分别位于HA1链29、141、218、298、305、313位点和HA2链492、551位点(表4)。其中313位点上发生了脯氨酸(P)→丝氨酸(S)变化,导致新增一个潜在的糖基化位点,该位点在HA1和HA2裂解位点附近,位点的糖基化可影响HA链裂解,可能导致病毒的毒力和抗原性发生变化。
3 讨 论
H9N2亚型流感病毒的HA基因演化主要在其北美和欧亚两大分支中存在,其中北美分支以A/Turkey/Wisconsin/1/66为代表毒株,欧亚分支中存在3个亚分支,分别是以A/Duck/HongKong/Y280/97为代表的Y280-like、以A/Quail/HongKong/G1/97为代表的Gl-like和以A/Duck/HongKong/Y439/97为代表的Y439-like,我国大陆大部分分离株主要属于Y280-like分支,在Y280-like亚分支中还有2个亚分支[14]。从HA基因的遗传进化树图可看出,本研究的毒株SW/GX/P2/2011和SW/GX/P3/2011均属于欧亚分支中的Y280-like,相较于其他物种来源的流感病毒HA基因,其与禽源HA基因的亲缘关系更近,说明本研究的HA基因应来源于禽源H9N2亚型流感病毒,与伍和明等[15]分析认为H9N2亚型SIV的HA基因在遗传演化分支中属于Y280-like亚分支、且来源于禽的观点基本一致,表明在几年间广西地区猪H9N2流感病毒HA基因均处于相对稳定状态,未出现明显的抗原漂移或突变,可能与H9N2亚型流感病毒具有适应性感染猪只的某些HA基因特征有关,具体的感染和致病机理需进一步探究。但值得注意的是,在基因的遗传进化树中出现了与试验毒株HA基因核苷酸同源性极高的犬H9N2亚型流感病毒,说明该型流感病毒具备感染其他哺乳动物的基因特征,提示应警惕H9N2亚型流感的跨种属传播问题,与伍和明等[15]的研究结果一致。本研究中2株分离株的氨基酸裂解位点在335~341 aa间,为RSSR↓GLF,表明HA1和HA2是由两个碱性氨基酸互相连接,没有多个碱性氨基酸插入,具有低致病性禽流感病毒特点,但从核苷酸水平分析,丝氨酸(S)与精氨酸(R)仅有一个碱基的差异,即AGC/AGU-AGG/AGA,因此,此位点附近的氨基酸有突变成碱性氨基酸类(R)的可能,从而使病毒的毒力增强。
H9N2亚型流感病毒的HA蛋白受体结合位点形成一个球状结构,由第109、161、163、191、198、202和203位的氨基酸组成。本研究的2株分离株在HA蛋白上的第109、161、163、202和203位均高度保守,在198位上为丙氨酸(A),在其他位为缬氨酸(V)、苏氨酸(T)和谷氨酸(E),符合Y280-like亚分支毒株的分子标志。Weis等[16]对H3亚型流感病毒位点进行分析发现,当H9亚型流感病毒HA蛋白的234位为亮氨酸(L)时,具有结合SAα-2和6Gal受体特异性,优先与人的流感病毒受体蛋白结合,而HA蛋白的234位为甘氨酸(G)时具有结合SAα-2和3Gal受体特异性,优先结合禽的流感病毒受体,当HA蛋白的234位为蛋氨酸(M)时则对2种受体具有相同的结合能力。本研究中2株分离株的234位氨基酸均为亮氨酸(L),说明2株分离株具有与人流感受体结合的倾向。
HA蛋白上的糖基化位点对维持HA分子结构及功能至关重要,例如裂解位点附近的寡糖链可形成空间屏障进而阻碍HA蛋白裂解[17]。本研究的2株流感病毒株均存在于8个糖基化位点,其中29、141、218、298、305、492和551位点与参考毒株均无明显差异,第313位点由于发生了脯氨酸(P)→丝氨酸(S)变化,导致增加了一个糖基化位点,这是病毒毒力的进化还是病毒对宿主的适应尚需进一步探究。Baigent和Mccauley[15,18]应用H3模型研究Hl、H5和H7等亚型毒株的HA糖基化位点时发现,HA蛋白的158位有糖基化位点而NA颈部有氨基酸缺失,或158位没有糖基化位点而NA颈部无氨基酸缺失,可保证病毒有效生长。本研究2株分离株HA蛋白的158位无糖基化位点而NA颈部无氨基酸缺失,说明该2株病毒可在宿主体内有效生长。
4 结 论
广西2株H9N2亚型猪源流感病毒分离株A/swine/Guangxi/P2/2011和A/swine/Guangxi/P3/2011的HA基因属于欧亚普系的Y280亚系,从HA基因的基因层次分析2株分离毒株均有毒力增强趋势并能在宿主体内良好复制,具备典型的低致病性和与人流感受体结合的特征。因此,今后应加强对H9N2亚型猪源流感病毒的监测及防控,防止该型流感病毒和其他亚型流感病毒在猪体内发生基因重排,引发更严重的传播后果。

