布地奈德联合肺表面活性物质治疗胎粪吸入综合征对血气指标的影响及安全性分析
赵振彤,臧小英
(1.天津医科大学第二医院新生儿科,天津300211;2.天津医科大学护理学院,天津300070)
胎粪吸入综合征(meconium aspiration syndrome,MAS)是胎粪吸入引起的常见新生儿呼吸系统疾病。MAS 常引起持续肺动脉高压、肺出血、心力衰竭、败血症等并发症,病死率可达11%~13%[1],严重威胁了新生儿的生命健康。因此,及时有效的治疗新生儿MAS 是新生儿科方向研究的热点问题。目前治疗MAS 的药物主要包括肺表面活性物质、糖皮质激素、氨溴索等。肺表面活性物质对提高患儿氧合功能有重要作用[2-3]。布地奈德是一种局部抗炎活性较强的吸入性糖皮质激素,能够减轻肺部炎症,提高通气与换气功能[4]。有研究表明,肺表面活性物质联合布地奈德治疗MAS 效果显著[5-6]。本研究旨在探讨布地奈德联合肺表面活性物质治疗MAS 对血气指标的影响及安全性分析。
1 资料与方法
1.1 一般资料 本研究选取2017 年1 月-2018 年12 月我院住院MAS 患儿116 例,所有MAS 患儿诊断符合《实用新生儿科学》标准[7]:(1)明确的胎粪吸入史。(2)明确发生宫内窘迫或产时窒息。(3)足月、日龄24 h、有青紫、三凹征等表现。(4)X 线胸片提示肺部有斑片状云絮影或广泛颗粒状阴影。排除标准:先天性心脏病、气管食管瘘、心力衰竭、肝肾疾病及先天严重畸形等疾病。将116 例MAS 患儿随机(按照数字表法)分两组,每组各58 例,观察组与对照组患儿一般临床资料具有可比性,差异无统计学意义(P>0.05),见表1。本研究获得所有患儿家属签署的知情同意书。
1.2 治疗方法
1.2.1 基础治疗[8]入院后,2 组患儿迅速进行气道分泌物清理、抗感染、营养支持、保暖、电解质平衡的维持、酸碱平衡的维持等基础治疗。中度呼吸窘迫患儿(100≤PaO2/FiO2<200)采用鼻塞式气道正压通气,重度患儿(PaO2/FiO2<100)给予气管插管呼吸机辅助通气,好转后换成鼻塞式气道正压通气。
1.2.2 对照组治疗方法 所有患儿入院2 h 内在气管内滴入猪肺磷脂注射液(100 mg/kg,意大利Chiesi Farmaceutici S.p.A.)。
1.2.3 观察组治疗方法 入院2 h 内在气管内滴入布地奈德(澳大利亚AstraZeneca Pty Ltd)进行治疗(0.25 mg/kg),再滴入猪肺磷脂注射液(100 mg/kg)。治疗12 h 后观察两组患儿呼吸情况,若无改善或加重,观察X 线胸片,如提示肺部阴影出现增多且排除肺气漏,再给患儿滴加一次相同剂量的猪肺磷脂注射液。
1.3 观察指标
1.3.1 血气指标 分别在患儿入院时(0 h)、治疗12、24、48 h 时采集所有患儿动脉血1 mL,采用普朗PL2200 普朗血气分析仪进行检测:动脉血氧分压(PaO2)、动脉血二氧化碳分压(PaCO2)、经皮血氧饱和度(TcSaO2)、pH。

表1 两组患儿一般临床资料
1.3.2 并发症 记录患儿肺动脉高压、肺出血、心力衰竭、败血症等并发症情况。
1.3.3 治疗效果 48 h 后检查所有患儿X 线胸片,治疗前后比较,明显能观察到肺部炎症减少且患儿呼吸困难情况缓解即治疗有效;若胸片提示肺部炎症未减少即治疗无效。记录两组患儿住院时间和住院期间的平均氧疗时间。
1.4 统计学方法 采用SPSS 19.0 软件对数据进行分析。符合方差齐性和正态分布的计量资料用表示,两组间比较采用t 检验;计数资料比较用χ2检验。P<0.05 表示差异有统计学意义。
2 结果
2.1 不同治疗时间血气指标情况 观察组和对照组在治疗前(0 h)血气指标差异无统计学意义(P>0.05)。在治疗 12、24 和 48 h 后,两组血气指标改善效果显著(P<0.05),且改善程度随着治疗时间延长而明显提高(P<0.05)。比较不同治疗时间点,观察组较对照组在PaCO2下降更明显,PaO2和TcSaO2升高更显著(P<0.05);在不同治疗时间点观察组pH 高于对照组,差异无统计学意义(P>0.05),见表2。
表2 不同治疗时间两组患儿血气指标比较()
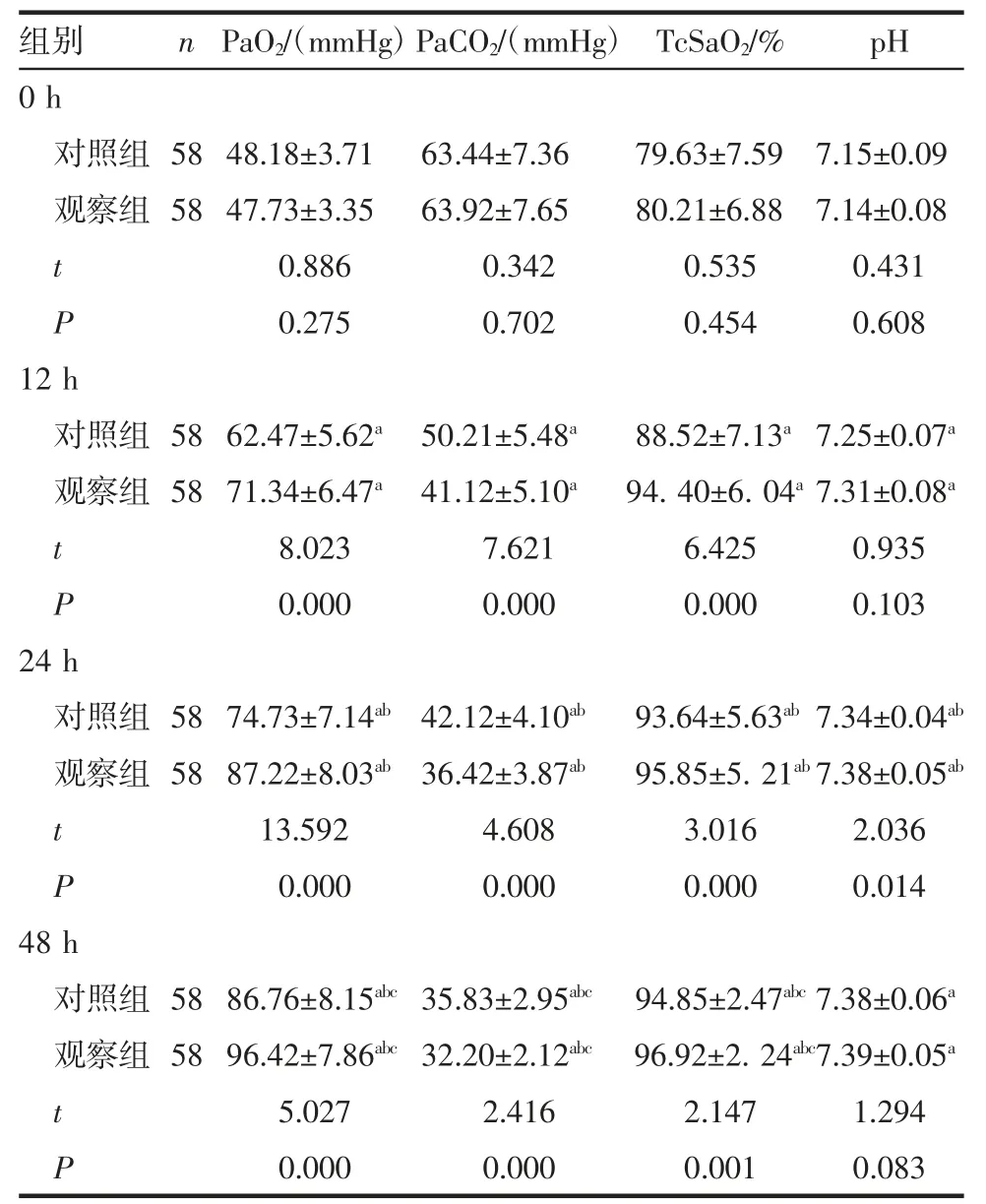
表2 不同治疗时间两组患儿血气指标比较()
注:a、b、c 分别为组内与 0、12、24 h 比较,P<0.05
组别n PaO2/(mmHg)PaCO2/(mmHg) TcSaO2/%pH 0 h对照组 58 48.18±3.71 63.44±7.36 79.63±7.59 7.15±0.09观察组 58 47.73±3.35 63.92±7.65 80.21±6.88 7.14±0.08 t 0.886 0.342 0.535 0.431 P 0.275 0.702 0.454 0.608 12 h对照组 58 62.47±5.62a 50.21±5.48a 88.52±7.13a 7.25±0.07a观察组 58 71.34±6.47a 41.12±5.10a 94.40±6.04a 7.31±0.08a t 8.023 7.621 6.425 0.935 P 0.000 0.000 0.000 0.103 24 h对照组 58 74.73±7.14ab 42.12±4.10ab 93.64±5.63ab 7.34±0.04ab观察组 58 87.22±8.03ab 36.42±3.87ab 95.85±5.21ab 7.38±0.05ab t 13.592 4.608 3.016 2.036 P 0.000 0.000 0.000 0.014 48 h对照组 58 86.76±8.15abc 35.83±2.95abc 94.85±2.47abc 7.38±0.06a观察组 58 96.42±7.86abc 32.20±2.12abc 96.92±2.24abc7.39±0.05a t 5.027 2.416 2.147 1.294 P 0.000 0.000 0.001 0.083
2.2 并发症分析 两组出现并发症以肺动脉高压为主,另出现肺出血、心力衰竭、败血症并发症。对照组并发症发生率为29.3%,观察组为10.3%,两组差异有统计学意义(χ2=6.562,P<0.05),见表 3。
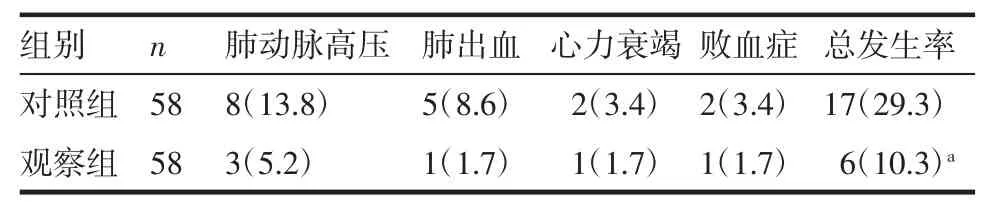
表3 两组患儿并发症发生情况分析[n(%)]
2.3 治疗效果分析 对照组有39 例48 h 胸片显示肺部炎症明显减少,即治疗总有效率为67.2%,观察组治疗总有效率为87.8%,明显高于对照组(χ2=7.139,P<0.05)。观察组平均氧疗时间减少约25 h(P<0.05),平均住院时间缩短近 1 周(P<0.05),见表4。

表4 临床疗效分析
3 讨论
MAS 是目前新生儿医生研究的重点方向之一,其发病机制主要是新生儿在胎粪吸入后导致呼吸系统炎性反应,进而引起肺泡上皮细胞的损伤,同时可能导致肺血管内皮细胞遭受破坏[9]。表面活性物质的活性易受到胎粪影响,主要原因是在胎粪内磷脂酶A2、蛋白水解酶均可直接抑制肺表面活性物质生成,对肺泡上皮细胞的产生进一步损伤,加剧机体酸中毒及缺氧状态[10]。有研究表明蛋白酶抑制剂可保护肺泡上皮细胞屏障功能免受胎粪诱导的损伤[11]。肺表面活性物质的缺少,可引起肺透明膜和肺泡的不同程度的萎缩,补充外源性肺表面活性物质来治疗MAS,避免了肺泡的萎缩而产生的呼吸系统功能受损。在治疗MAS 时,肺表面活性物质得到适当的补充,可使肺泡间隙受到体内蛋白影响降低,从而进一步促进PS 分泌,肺泡稳定性得到进一步增强,且有利于肺泡扩张,进而缓解肺部通气[12]。
研究表明,MAS 患儿体内存在多种炎症因子,同时相关促炎症反应的酶类水平明显升高,提示炎症相关因子的表达水平升高可能在MAS 的发病机制中起重要作用[13]。布地奈德用于治疗MAS,主要是利用较强的抗炎作用,其可能机制是通过减轻抗炎抗体的酶促反应,使得合成和释放支气管收缩物质减少,起到抑制支气管平滑肌收缩,降低气道阻力的作用[14-15]。布地奈德主要通过肝脏清除,经尿排出体外,代谢产物相对激素活性低,对患儿不良反应影响较小,对治疗MAS 起重要作用。
动物实验发现,表面活性剂与布地奈德联合治疗对支气管肺泡灌洗(broncho alveolar lavage, BAL)中性粒细胞计数、氧化损伤、肺内细胞因子水平和mRNA 表达以及肺水肿形成的减少最有效,可减轻肺部炎症和氧化修饰[16-17],表明了这种治疗组合在MAS 治疗具有应用前景。有研究表明,呼吸窘迫综合征采用肺表面活性物质与布地奈德联合治疗,可明显改善其血气情况[18]。肺表面活性物质与布地奈德的联合应用于治疗MAS,不仅能改善PaO2/FiO2、TcSaO2、PaO2、PaCO2等,其临床效果好和安全性高[4-5]。
本研究在猪肺磷脂注射液的基础上,联合使用布地奈德治疗MAS,结果发现观察组患儿血气指标PaO2、PaCO2、TcSaO2和 pH 得到有效改善,改善效果比对照组患儿更显著。布地奈德的联合应用,协同促进了肺表面活性物质的合成与释放,在抑制炎症的同时,提高了患儿肺通气。因此,患儿治疗有效性得以提高至87.8%,且常见并发症发生率低至10.3%。住院平均时间缩短近1 周,住院期间氧疗平均时间也明显缩短。提示联合用药治疗MAS 效果显著,安全性更高。
鉴于本研究样本数量有限、仅单中心研究,需进一步扩大研究样本数量和开展多中心研究,以便更充分的说明联合用药的临床效果。

