赖氨酸对紫玉米芯花青素热稳定性影响的研究
华燕菲,贾艳菊,段嘉婧,生庆海
(河北经贸大学生物科学与工程学院,河北石家庄 050061)
0 引言
紫玉米(Zea mays L.)是一种特殊的玉米品种,其表皮与芯呈紫黑色,富含3-(3",6"-二丙二醛糖苷)、天竺葵苷-3-糖苷、丙二醛对应物等多种天然花青素[1-2]。紫玉米芯花青素主要以酰基化形式存在[3],稳定的红色黄烷阳离子的相对比例更高[4],在食品添加剂和化妆品的开发中具有很大应用价值。花青素属于类黄酮色素,具有抑制脂肪生成、抗氧化、抗肿瘤、调节免疫系统等功能[5-8],但在光照、温度、pH值、糖、亚硫酸盐和金属离子等影响下,花青素的化学结构极易发生改变[9]。尤其许多食物在生产加工过程中的热处理,会极大地影响花青素的含量[10]。
实际生产应用中,常需要加入其他辅助物质来保持花青素良好的稳定性。近年来,氨基酸或蛋白质对花青素稳定性影响的研究逐渐展开。研究发现,某些氨基酸对花青素具有良好的辅色作用,胡能兵等人[11]试验得出甲硫氨酸是对紫色辣椒叶片色素的最佳氨基酸类辅色剂;Chung C等人[12]研究发现色氨酸能通过氢键与花青素相互作用来提高饮料中花青素的稳定性。赖氨酸化学名称为2,6-二氨基己酸,在玉米中含量较高[13],是一种常见食品添加剂,可用于改善食品的色、香、味及质地[14]。极易被机体吸收,在促进蛋白质合成、能量代谢、矿物质吸收、骨骼代谢、治疗病毒感染、减轻焦虑等方面均有着很好的效果[15]。但目前国内外关于赖氨酸对花青素稳定性方面的研究鲜有报道,试验通过热降解加速试验,研究在2种pH值环境下赖氨酸对于紫玉米芯花青素热稳定性的影响,为紫玉米芯花青素产品在食品工业中的应用提供理论参考。
1 材料与方法
1.1 材料、试剂与仪器
紫玉米芯花青素浓缩液的制备:以紫色玉米芯粉为原料,按料液比1∶30加入质量分数5%的醋酸溶液,浸提24h后,抽滤得到花青素粗提液。然后,通过SP207大孔树脂分离,再经旋转蒸发得到浓缩的花青素溶液。
柠檬酸(分析纯),天津市恒兴化学试剂制造有限公司提供;柠檬酸钠(分析纯),天津永大化学制剂有限公司提供;赖氨酸(食品添加剂),深圳市振芯嘉贸易有限公司提供。
HH-6型数显恒温水浴锅,江苏省金坛市荣华仪器制造有限公司产品;722型分光光度计,上海析谱仪器有限公司产品。
1.2 试验方法
1.2.1 赖氨酸-紫玉米芯花青素溶液的配制
将一定量的赖氨酸分别溶于pH值3.0和pH值5.4的缓冲液中制成质量分数0,1%,3%,5%的赖氨酸溶液,使用移液枪取1 mL紫玉米花青素浓缩溶液加入到200 mL赖氨酸溶液中,配制成混合溶液。
1.2.2 不同条件下紫玉米芯花青素吸收光谱的研究
使用移液枪吸取不同质量分数pH值3.0和pH值5.4的赖氨酸-紫玉米芯花青素溶液(0,1%,3%,5%),用722型分光光度计于400~600 nm的波长范围内扫描并绘制吸收光谱曲线,记录吸光度。
1.2.3 热降解动力学参数的测定
郭村有八百年历史,是旧时宁国、徽州、池州三府交界之地,兴旺的时候,村里有十座祠堂,店铺毗连,商贾云集。
参照焦宇知等人[16]的方法,将pH值3.0和pH值5.4的不同质量分数赖氨酸-紫玉米芯花青素溶液(0,1%,3%,5%)置于85℃恒温水浴锅中加热3 h,且每隔1 h于510 nm处测定吸光度,以ln(A/A0)为y轴,t为x轴作图得斜率-k,根据k计算热降解半衰期(t1/2)与热降解率P。按照朗伯-比尔定律和阿伦尼乌斯公式计算如下:

式中:A——t时刻色素溶液吸光度;
A0——色素溶液初始吸光度;
k——热降解反应常数;
t——时间,h;
t1/2——热降解半衰期,h;
P——热降解率,%。
每个试验均重复4次,利用Excel 2016软件处理分析试验数据,结果用平均数±标准差表示,并用Graphpad Prism 8.0软件绘图,并使用SPSS 22.0软件对热降解率指标进行方差显著性分析和Ducan多重比较分析,p<0.05表示数据差异有统计学意义。
2 结果与分析
2.1 不同质量分数赖氨酸对于紫玉米芯花青素溶液吸收光谱的影响
pH值3.0时不同质量分数赖氨酸对紫玉米芯花青素吸收光谱的影响见图1。

图1 pH值3.0时不同质量分数赖氨酸对紫玉米芯花青素吸收光谱的影响
在pH值3.0时,添加不同质量分数赖氨酸对紫玉米芯花青素溶液的吸收光谱无明显影响,最大吸收峰均在510 nm处。加入质量分数0,1%,3%,5%赖氨酸质量分数花青素溶液对应的最大吸光度依次为0.213,0.202,0.189,0.185。随着赖氨酸添加量的增加,吸光度值逐渐降低,这表明在pH值3.0环境下,赖氨酸对花青素具有减色效应。
pH值5.4时不同质量分数赖氨酸对紫玉米芯花青素吸收光谱的影响见图2。
在pH值5.4时,添加不同质量分数赖氨酸对紫
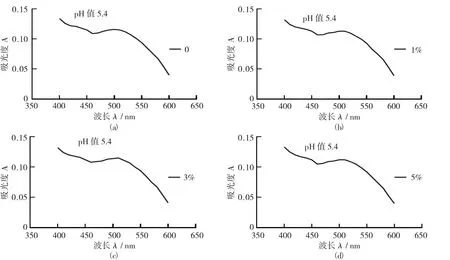
图2 pH值5.4时不同质量分数赖氨酸对紫玉米芯花青素吸收光谱的影响
玉米芯花青素溶液的可见吸收光谱无明显影响。于波长510 nm处,添加0,1%,3%,5%赖氨酸质量分数的花青素溶液的吸光度依次为0.115,0.113,0.115,0.112,表明在弱酸条件下,添加赖氨酸对花青素颜色没有影响。花青素溶液在pH值3.0时的吸光度明显高于pH值5.4时的吸光度,这与王新广,Luna-Vital D等人[17-18]得出的结果相一致。这是因为紫玉米芯花青素在较低pH值更易保证黄烷阳离子的优势[19],使花青素稳定[20]。
2.2 pH值3.0时不同质量分数赖氨酸对紫玉米芯花青素热降解率的影响
pH值3.0时不同质量分数赖氨酸对紫玉米芯花青素热降解率的影响见图3。

图3 pH值3.0时不同质量分数赖氨酸对紫玉米芯花青素热降解率的影响
在pH值3.0条件下,对不同质量分数的赖氨酸-紫玉米芯花青素混合溶液(0,1%,3%,5%) 进行85℃恒温水浴3 h,紫玉米芯花青素的热降解率基本呈现随赖氨酸质量分数、加热时间的增加而增加的趋势。赖氨酸质量分数对紫玉米芯花青素的热降解率均有极显著的影响(p<0.01)。添加1%,3%,5%赖氨酸的热降解率为20.07%±1.02%,19.34%±0.66%,21.56%±1.22%,极显著高于未添加赖氨酸的紫玉米芯花青素溶液的热降解率12.79%±1.55%(p<0.01),添加1%赖氨酸的和添加3%,5%赖氨酸质量分数的花青素溶液热降解率的差异不显著(p>0.05),添加5%的热降解率显著高于添加3%的热降解率(p<0.05)。结果表明,在pH值3.0条件下,添加赖氨酸可降低花青素溶液的稳定性,使花青素热降解率显著升高。
2.3 pH值5.4时不同质量分数赖氨酸对紫玉米芯花青素热降解率的影响
pH值5.4时不同质量分数赖氨酸对紫玉米芯花青素热降解率的影响见图4。
在pH值5.4条件下,添加赖氨酸对紫玉米芯花青素的热降解率具有极显著影响(p<0.01),花青素的热降解率基本呈现随赖氨酸质量分数增加而增加的趋势,加热3 h均达最大值。添加0,1%,3%,5%质量分数的赖氨酸所对应的热降解率依次为18.64%±0.69%,18.81%±0.46%,22.15%±0.74%,22.73%±1.18%。添加0和1%赖氨酸的花青素溶液的热降解率无显著差异(p>0.05),添加质量分数3%和5%赖氨酸的花青素溶液的热降解率无显著差异(p>0.05),添加质量分数3%,5%赖氨酸的花青素溶液的热降解率极显著高于添加质量分数0,1%赖氨酸的花青素溶液的热降解率(p<0.01)。结果表明,在pH值5.4条件下,添加赖氨酸的质量分数超过3%时,可降低花青素的热稳定性。
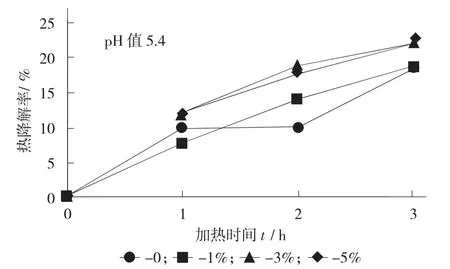
图4 pH值5.4时不同质量分数赖氨酸对紫玉米芯花青素热降解率的影响
2.4 不同质量分数赖氨酸对紫玉米芯花青素热降解动力学参数的影响
赖氨酸质量分数对紫玉米芯花青素的热降解参数影响见表1。

表1 赖氨酸质量分数对紫玉米芯花青素的热降解参数影响
研究表明,在紫玉米芯花青素中添加赖氨酸后,其热降解变化情况遵循一级热降解动力学模型。添加赖氨酸可导致紫玉米芯花青素在热降解过程中半衰期的缩短,pH值为3.0时,添加质量分数1%,3%,5%赖氨酸组的花青素半衰期比未添加赖氨酸组分别降低了38.67%,40.67%,45.53%;pH值为5.4时,添加质量分数1%,3%,5%赖氨酸组的花青素半衰期比未添加赖氨酸组的分别降低了9.82%,23.57%和23.93%。
添加赖氨酸可增大花青素的热降解速率常数:pH值为3.0时,添加质量分数1%,3%和5%的赖氨酸组花青素的热降解速率常数比对照组的分别增加了0.029 1,0.031 7,0.038 6;pH值为5.4时,添加质量分数1%,3%,5%赖氨酸组的花青素降解速率常数比对照组的分别增加了0.091 2,0.034 8,0.052 4。结果表明,溶液中添加赖氨酸能够降低紫玉米芯花青素的热稳定性,且加入的赖氨酸质量分数愈高,紫玉米芯花青素的热稳定性愈差。
3 结论
在pH值3.0和5.4下,添加不同质量分数赖氨酸对紫玉米芯花青素的吸收光谱无明显影响,pH值3.0时赖氨酸对花青素有减色效应。紫玉米芯花青素颜色受pH值影响较大,在pH值3.0的环境中稳定性相对较高,因此紫玉米芯花青素主要适合于酸性产品的制备。
在pH值3.0和5.4下,于85℃下恒温水浴处理3 h,添加赖氨酸均可增加花青素溶液的热降解率,且随着质量分数增加,花青素的热降解反应常数逐渐增加、半衰期逐渐降低。可见,赖氨酸的添加可降低花青素的热稳定性。

