不同干燥工艺对药用大黄功效组分的影响△
丁一明,商彤,石玥,赵婷,2,张媛,2,李莉,魏胜利,2*
1.北京中医药大学 中药学院,北京 102488;2.中药材规范化生产教育部工程研究中心,北京 100102; 3.首都医科大学 附属北京中医医院,北京 100010;4.北京市中药研究所,北京 100035
大黄为蓼科植物掌叶大黄RheumpalmatumL.、唐古特大黄R.tanguticumMaxim. ex Balf及药用大黄R.officinaleBaill.的干燥根和根茎[1]。目前,大黄广泛应用于医药及医药化工领域,是一种常用的大宗中药材,也是我国驰名中外的传统出口药材[2-3],具有很高的经济价值,可以作为扶贫产业推广发展[4]。课题组前期研究发现,可依据大黄有效成分之间的含量和比例,将大黄中的有效成分划分成不同的功效组分型,即根据蒽醌类、二蒽酮类等成分的含量组成比例及差异,将大黄划分为泻下攻积型、清热泻火型及凉血解毒型,从而为大黄药材的定向培育、加工和中医合理用药提供参考[5-8]。
产地加工是药材生产与品质形成的重要环节[9]。大黄根及根茎粗大,自然干燥困难,干燥时间长,在加工过程中易出现糠心、发霉、变质、变色等现象[10],造成其有效成分的流失。2015年版《中华人民共和国药典》(以下简称《中国药典》)规定,大黄切瓣或段,穿绳成串干燥或直接干燥。目前有关干燥工艺对大黄药材质量的影响已有报道,胡会娟等[11]以唐古特大黄为实验材料,研究表明大黄在50 ℃条件下干燥,其番泻苷A含量最低;宋平顺等[12]研究发现,大黄适宜的干燥方法是45 ℃恒温干燥;房庆伟等[13]研究表明,药用大黄在干燥60 ℃干燥15 h时,结合蒽醌类含量最高。上述研究缺少对大黄药用部位的区分及对切片厚度这一产地加工重要因素的考察,缺乏一定的系统性。
本研究以药用大黄为例,以大黄4类功效组分(鞣质类、二蒽酮类、游离蒽醌类、结合蒽醌类)含量为指标,对大黄干燥过程中的3个主要因素(药用部位、切片厚度、干燥温度)进行系统比较,探索不同功效类型大黄的最适宜产地加工工艺,为大黄精准饮片的定向干燥工艺奠定理论和技术基础。
1 材料
高效液相色谱仪(Agilent,型号:1200);万分之一电子分析天平(METTLER TOLEDO,型号:ME104);十万分之一电子分析天平(Sartorius,型号:BT 25S);超声清洗器(江苏省昆山市超声仪器有限公司,型号:KQ5200D);电热恒温水浴锅(天津市泰斯特仪器有限公司,型号:DK-98-ⅡA);旋转蒸发器(上海亚荣生化仪器厂,型号:RE52CS);高速万能粉碎机(天津市泰斯特仪器有限公司,型号:FW100型);电热恒温干燥箱(天津市通利信达仪器厂,型号:101-A型)。
没食子酸对照品(批号:Y19M8C36143)、儿茶素对照品(批号:P20O7F23087)、番泻苷A对照品(批号:P01S8F42887)、番泻苷B对照品(批号:Y23M8Y17128),大黄酸对照品(批号:T30A8F42628)、大黄酚对照品(批号:T23A8F42188)、大黄素对照品(批号:C18F8Q29652)、芦荟大黄素对照品(批号:T28D6F8264)、大黄素甲醚对照品(批号:T26A8F34784)纯度均大于等于98%,购自上海源叶生物科技有限公司;HPLC用甲醇和乙腈为色谱纯(Fisher);其他试剂均为分析纯;水为屈臣氏蒸馏水。
新鲜药用大黄于3—4月采自四川平武地区,均为3年生栽培大黄。经北京中医药大学魏胜利教授鉴定为蓼科植物药用大黄R.officinaleBaill.的根和根茎。为排除大黄个体差异、保持样品的均一性,选取15株大小一致的药用大黄,以大黄横截面圆心为基准,将根或根茎分别纵切5瓣,随机切成1、3、5 cm段,混匀后放入30、40、50、60、70 ℃烘箱中干燥,样品处理干燥方法见表1。

表1 干燥样品及处理方法
2 方法
采用《中国药典》大黄项下总蒽醌的含量测定方法测定结合蒽醌类成分含量,采用课题组前期已经建立的测定方法[14]测定游离蒽醌类、二蒽酮类、鞣质类成分含量,通过双因素方差分析的方法,分别对大黄泻下攻积、清热泻火、凉血解毒3类功效成分的含量进行分析。
具有泻下攻积功效的结合蒽醌类成分以大黄酸苷、大黄素苷、大黄素甲醚苷、芦荟大黄素苷、大黄酚苷的含量总和计算,二蒽酮类成分以番泻苷A和番泻苷B的含量总和计算;具有清热泻火功效的游离蒽醌类成分以大黄酸、大黄素、大黄素甲醚、芦荟大黄素、大黄酚的含量总和计算;具有凉血解毒功效的鞣质类成分以没食子酸和儿茶素的含量总和计算[4]。
采用SPSS 24.0统计软件进行数据分析。采用双因素方差分析对各项指标的均值进行显著性分析,当分析结果为显著性差异时,通过比较偏Eta方(ηP2)判定干燥温度和切片厚度对各功效组分变异的贡献率大小。0.2≤ηP2<0.5表示低度影响效应,0.5≤ηP2<0.8表示中度影响效应,ηP2≥0.8表示高度影响效应。
3 结果
3.1 干燥温度、切片厚度及其互作效应对药用大黄根茎功效组分的影响
对不同干燥方法下药用大黄根茎4类功效组分的质量分数(见表2)进行以干燥温度和切片厚度为控制变量的有交互作用的双因素方差分析(见表3)。结果显示,不同干燥温度、不同切片厚度以及两者的互作效应下药用大黄根茎中鞣质类、二蒽酮类、游离蒽醌类、结合蒽醌类成分含量差异有统计学意义(P<0.01)。表明干燥温度、切片温度以及互作效应对药用大黄根茎中鞣质类、二蒽酮类、游离蒽醌类、结合蒽醌类含量均有极显著影响。
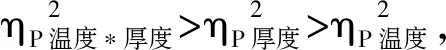

表2 不同干燥方法下药用大黄根茎和根4类 功效组分的质量分数 mg·g-1
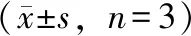
表3 干燥温度和切片厚度对药用大黄根茎4类功效组分成分含量的影响
对不同厚度和干燥温度药用大黄根茎中鞣质类、二蒽酮类、游离蒽醌类、结合蒽醌类含量进行比较。结果表明,鞣质类、二蒽酮类、游离蒽醌类、结合蒽醌类含量变化趋势均不明显,可能与其互作效应较大有关。其中鞣质类质量分数以样品4(60 ℃,1 cm)最高,为10.43 mg·g-1,以样品2(70 ℃,3 cm)最低,为6.96 mg·g-1,两者相差1.49倍。以鞣质类含量为指标,药用大黄根茎的最适宜干燥条件为干燥温度60 ℃,切片厚度1 cm;二蒽酮类质量分数以样品4(60 ℃,1 cm)最高,为10.66 mg·g-1,以样品2(70 ℃,3 cm)最低,为5.39 mg·g-1,两者相差1.97倍,由此可知对于二蒽酮类成分,药用大黄根茎的最适宜干燥条件为干燥温度60 ℃,切片厚度1 cm;游离蒽醌类质量分数以样品8(50 ℃,3 cm)最高,为2.57 mg·g-1,以样品7(50 ℃,1 cm)最低,为1.18 mg·g-1,两者相差2.17倍。以游离蒽醌类为指标,药用大黄根茎最适宜干燥条件为干燥温度50 ℃、切片厚度3 cm;结合蒽醌类质量分数以样品12(40 ℃,5 cm)最高,为14.91 mg·g-1,以样品2(70 ℃,3 cm)最低,为8.10 mg·g-1,两者相差1.84倍。以结合蒽醌类含量为指标,药用大黄根茎最适宜干燥条件为干燥温度40 ℃,切片厚度5 cm。
3.2 干燥温度、切片厚度及其互作效应对药用大黄根功效组分的影响
对不同干燥方法下药用大黄根4类功效组分的质量分数(见表2)进行以干燥温度和切片厚度为控制变量的有交互作用的双因素方差分析(见表4)。结果显示,不同干燥温度、不同切片厚度以及两者的互作效应下药用大黄根中,鞣质类、二蒽酮类、游离蒽醌类、结合蒽醌类成分含量差异有统计学意义(P<0.01)。表明干燥温度、切片温度以及互作效应对药用大黄根中鞣质类、二蒽酮类、游离蒽醌类、结合蒽醌类含量均有极显著影响。
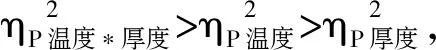

表4 干燥温度和切片厚度对药用大黄根四类功效组分成分含量的影响
4 结论与讨论
干燥温度和切片厚度对药用大黄4种功效组分的影响效应不同,以鞣质类、二蒽酮类和游离蒽醌类含量为指标,温度和厚度的互作效应为药用大黄根茎和根的主要影响因素。以结合蒽醌类为标准,温度为根茎中各指标含量的主要影响因素,厚度为根中各指标的主要影响因素。
大黄是典型的多功效中药材,与其泻下攻积功效相关的有效成分主要为二蒽酮类、结合蒽醌类成分,二蒽酮类成分泻下效力较强,结合蒽醌类成分较弱,番泻苷A为大黄泻下攻积最强的有效成分[15]。在根茎切片厚度为3 cm时,随干燥温度升高,大黄二蒽酮类含量呈降低趋势。这可能和二蒽酮类、结合蒽醌类成分在高温受热过程中易发生降解[16-17]有关,本实验结果亦符合传统认识“炮制减弱生大黄的攻泻作用”[18]。药用大黄根茎与根中结合蒽醌类成分的含量在高温干燥条件下较低,而游离蒽醌类成分的含量在高温干燥条件下较高,这可能与结合蒽醌类成分在高温受热过程中易降解为游离蒽醌有关[19]。本研究中鞣质类含量变化趋势不明显,这可能与没食子酸含量在高温受热过程中大幅增加,儿茶素含量则会降低有关[20],对于大黄不同干燥工艺对大黄鞣质类成分的影响,仍需要进一步探索。
综上所述,可以通过降低干燥温度或增加切片厚度的干燥工艺,定向加工泻下攻积型大黄;通过提高干燥温度或减小切片厚度的干燥工艺,定向加工出清热泻火型大黄,为大黄精准药材的定向生产提供指导,并为其他精准药材的定向加工及临床应用提供理论依据。