L360钢在H2S/CO2共存体系中的腐蚀行为及腐蚀预测模型
廖柯熹,赵建华,夏 凤,周飞龙,赵 帅,景 红
(1. 西南石油大学 石油与天然气工程学院,成都 610500; 2. 中国航空油料有限责任公司 成都分公司,成都 610202; 3. 中石化上海油气分公司,上海 200120)
H2S/CO2广泛存在于油气田地层中,随着油气田的开发,越来越多的H2S/CO2作为伴生气被开采,这些气体溶于采出液后,溶液为酸性,对管道有很强的腐蚀性,会导致管道发生穿孔或断裂。采出天然气中高含量H2S/CO2已成为制约气田安全生产的重要因素[1]。
管道中影响H2S/CO2共存体系的因素包括H2S分压、温度、流速、CO2分压等[2-5]。马新元[6]探讨了分压、流速、腐蚀产物膜、Cl-等因素对CO2与H2S腐蚀的影响,但未针对H2S/CO2混合气体的影响因素进行分析;王霞等[7]研究了流速对L360钢在H2S/CO2条件下腐蚀速率的影响,研究表明流速越快,L360钢的腐蚀速率越高。目前,关于H2S/CO2共存体系中各因素对腐蚀的影响还不明确。
研究表明,分压比决定了腐蚀反应的控制机理,进而影响材料在H2S/CO2共存体系中的腐蚀速率。罗戏雨等[8]研究了两种气体的竞争协同效应和分压比机理以及可能的影响因素;钱进森等[9]的研究表明,在高分压比(pCO2/pH2S=400)条件下,材料在H2S/CO2混合体系中的腐蚀速率仅为在单纯CO2体系中的1/6;但也有研究表明,pCO2/pH2S<14时,腐蚀速率不会明显变化,14
张智等[12]利用短期高温高压反应釜试验得出试样在H2S/CO2条件下的腐蚀速率,并在此基础上进行了进一步的腐蚀速率预测,利用数理统计方法建立了考虑腐蚀时间效应的腐蚀速率预测模型,精度较高。
本工作采用高温高压釜研究了L360钢在H2S/CO2共存体系中的腐蚀行为,并在此基础上建立了更精确的腐蚀速率预测模型,以期为H2S/CO2共存体系中材料的腐蚀预测提供借鉴。
1 试验
1.1 试样
试验选用现场油气田管道建设常见的L360钢,其化学成分见表1。在管道上切割部分样品,并采用线切割将其加工成50 mm×10 mm×3 mm的腐蚀试片,试片表面进行机械抛光处理,设计共进行9组试验,其中每组试验包含5片试样,用于腐蚀失重试验和电化学试验[13]。试样的处理过程如下:先用去离子水清洗试样表面杂质并用石油醚除油,再采用无水乙醇浸泡清洗5 min后取出吹干,将处理好的试样用滤纸包好后放入干燥器内保存,最后采用精度为0.1 mg的天平称量[14]。
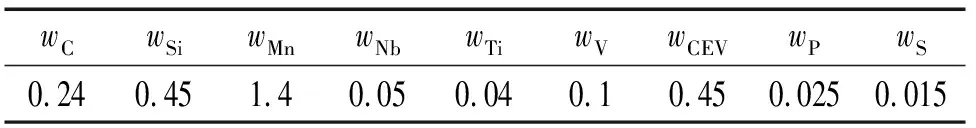
表1 L360钢的化学成分Tab. 1 Chemical composition of L360 steel %
由于气田集输管道中的水为地层采出水,故本试验按照地层水的测验结果配置模拟溶液,计算得到模拟溶液的配方见表2,溶液pH为7,采用N2除氧4 h后待用。

表2 模拟地层水溶液的配方Tab. 2 Formula of simulated formation water solution mg·L-1
1.2 试验方法
本工作进行9组L360钢腐蚀试片正交试验,试验方案见表3。试验采用美国PARR-4848高温高压动态反应釜[15-16]。试验前,向试验溶液中通N2除氧30 min,再在釜内装入试验溶液和试样进行气相腐蚀试验,釜内每次试验加水量为150 mL,水位未到试片放置的高度。密封反应釜后继续用N2除氧30 min,通过预定流速设置反应釜试片架的转速,缓慢升温至指定温度。先通入H2S至预定分压,再通入CO2至预定分压,最后通入N2至总压为6 MPa,每组试片在反应釜内连续进行3 d腐蚀试验。
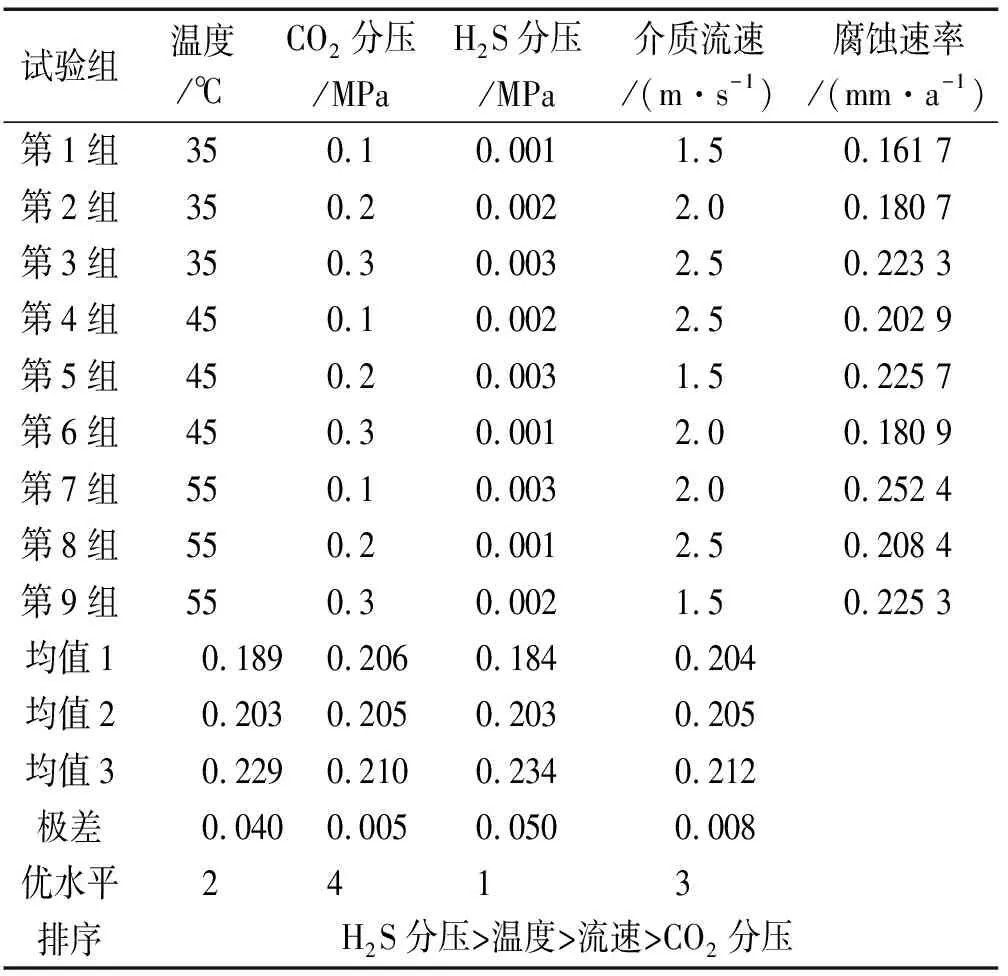
表3 正交试验表Tab. 3 Orthogonal experimental table
试验过程遵照GB/T 16545-2015《金属和合金的腐蚀 腐蚀试样上腐蚀产物的清除》执行,试验后任意选取3片试样,去除腐蚀产物后,置于干燥器内24 h后取出、称量,按式(1)计算腐蚀速率。采用扫描电子显微镜(SEM)、能谱仪(EDS)和X射线衍射(XRD)技术对剩余2片试片进行腐蚀产物形貌观察和腐蚀产物成分分析。

(1)
式中:Vp为腐蚀速率,mm/a;m0和m1分别为试片腐蚀前后的质量,g;S为试片的表面积,cm2;t为试片在腐蚀介质中浸泡的时间,h。
2 结果与讨论
2.1 L360钢的腐蚀速率
由表3可见:在9组试验条件下,L360钢的腐蚀速率为0.161 7~0.252 4 mm/a,且试样在55 ℃、CO2分压0.1 MPa、H2S分压0.003 MPa、流速为2.0 m/s条件下的腐蚀速率最大,在35 ℃、CO2分压0.1 MPa、H2S分压0.001 MPa、流速1.5 m/s条件下的腐蚀速率最小。根据表3结果,各影响因素的重要程度由大到小依次为:H2S分压(0.050)>温度(0.040)>流速(0.008)>CO2分压(0.005)。
由表3还可见:当CO2/H2S分压比为33~300时,随着温度的升高,离子间的交换和腐蚀反应加快,平均腐蚀速率增大;随着CO2分压的增大,腐蚀速率先出现缓慢降低的趋势,这是因为在基体表面生成的腐蚀产物膜对基体起到了一定的保护作用,腐蚀速率降低,继续增加CO2分压,平均腐蚀速率也逐渐增大。BROWN等[16]认为腐蚀环境中气相H2S分压较低时,试样表面虽然未能形成具有保护性的FeCO3膜,但腐蚀速率仍有明显降低,不过这种效果会随着H2S分压在一定范围内的增加而减弱;当H2S分压不断增大腐蚀速率随之增大,这是因为在一定范围内H2S含量增加会增加溶液的酸性,平均腐蚀速率增大;随着介质流速的增大,腐蚀性介质的流动和传质加快,腐蚀速率增大[17]。
2.2 腐蚀产物表征
根据2.1节试验结果,选取CO2/H2S分压比为33、100、200、300条件下的腐蚀试片进行腐蚀产物表面形貌观察和成分分析。由图1可见:在第7组(pCO2/pH2S=33)和第1组(pCO2/pH2S=100)试验条件下,试样表面的腐蚀产物膜较疏松多孔,对材料的保护作用较差;在第8组(pCO2/pH2S=200)和第6组(pCO2/pH2S=300)试验条件下,试样表面的腐蚀产物膜呈片状,且表面疏松多孔,也难以对基体起到良好的保护作用。各组试验条件下试样表面腐蚀产物的元素含量如表4所示,腐蚀产物的XRD图谱如图2所示。结合EDS和XRD检测结果可知,腐蚀产物主要是FeS,反应由H2S主导控制,与正交试验结果相符[18]。

(a) 第7组试样

(b) 第1组试样

(c) 第8组试样

(d) 第6组试样图1 不同试验条件下,试样表面腐蚀产物形貌Fig. 1 Morphology of corrosion products on the surface of samples under different test conditions
选取腐蚀速率最大的试片(第7组试样)进行去膜处理,观察其表面形貌,发现试样表面呈现均匀腐蚀,在高倍下才能观测到少量局部腐蚀坑,如图3所示。由于反应釜内模拟的整个腐蚀体系为气相,离子交换速度较慢,腐蚀程度明显低于在液相中的;且在流动状态下,液膜在试片同一水平表面趋于均匀,有助于减轻局部腐蚀。因此,在流动条件下L360钢在H2S/CO2共存体系中,腐蚀以均匀腐蚀为主,存在少量局部腐蚀坑[19]。
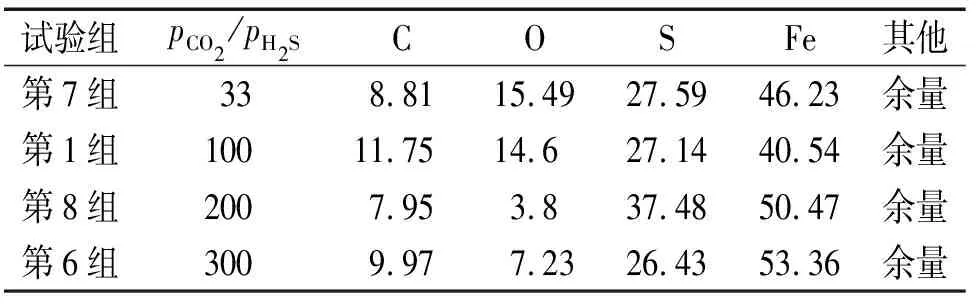
表4 各组试样表面腐蚀产物的化学成分(原子分数)Tab. 4 Chemical composition of corrosion products on the surface of each group of samples (atom fraction) %

图2 试样表面腐蚀产物的XRD图谱Fig. 2 XRD patterns of corrosion products on the surface of samples
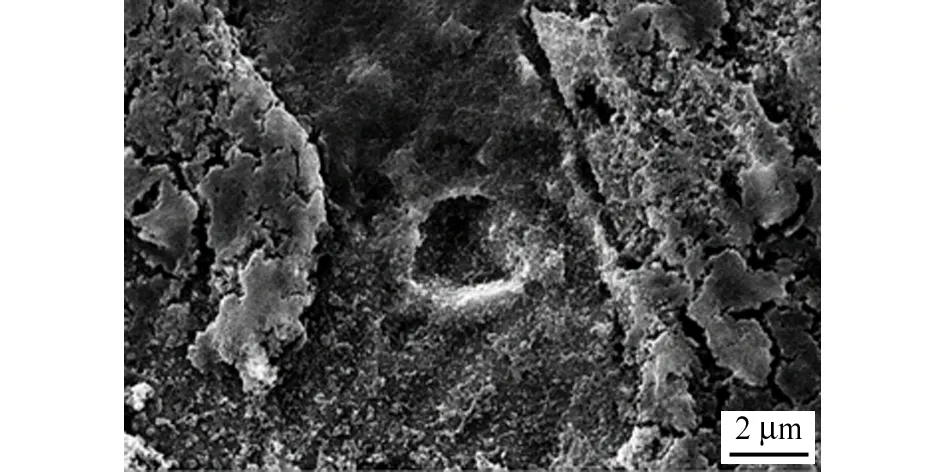
图3 第7组试样去除腐蚀产物后的表面形貌Fig. 3 Surface morphology of group 7 sample after removal of corrosion products
2.3 腐蚀机理
反应釜底部加入模拟地层水,一段时间后釜内气相含水量处于饱和状态,一旦气体在钢体表面析出形成液膜,H2S、CO2腐蚀性气体会溶解在试片表面液膜中发生电化学反应,H2S和CO2可电离生成H+,H+进一步还原为H2,阴极反应如式(2)~(9)所示,阳极反应主要为Fe的溶解,反应过程如式(10)~(11)所示。H2S与CO2都能在液膜中溶解,从而增加H+浓度并促进电化学腐蚀过程的进行。另外,相比于HCO3-,HS-在基体表面具有更好的化学吸附性,会加速基体腐蚀,溶解后的HS-具有一定的排他性,会抑制CO2形成的腐蚀性组分(H2CO3、HCO3-)与Fe反应。反应生成的FeS和FeS1-x等腐蚀产物会在基体表面形成疏松多孔覆盖物;FeCO3覆盖在基体表面能形成致密的保护膜,但该保护膜只在CO2/H2S分压比高时才能形成,在其他分压比条件下难以对钢体起到良好的保护作用,腐蚀产物生成反应如式(12)~(14)所示[20]。L360钢在CO2/H2S分压比为33~300的流动体系中,反应由H2S主导控制[21-22]。
阴极反应:

(2)

(3)

(4)

(5)

(6)

(7)

(8)

(9)
阳极反应:

(10)
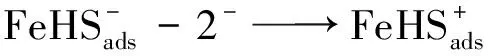
(11)
产物的生成:

(12)
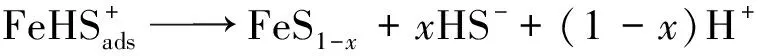
(13)

(14)
2.4 L360钢在H2S/CO2共存体系中的腐蚀速率预测模型
常见的腐蚀速率预测机理模型主要依据H2S/CO2共存体系下的腐蚀主导因素界定,影响H2S/CO2共存体系下L360钢腐蚀行为的因素主要有温度、H2S分压、CO2分压、流速。腐蚀速率模型建立过程如式(15)~(20)所示。
vcorr=k*f(T,pH2S,pCO2,v)=K*fT(T)*
fH2S(pH2S)*fCO2(pCO2)*fv(V)
(15)
lnvcorr=lnfT(T)+lnfH2S(pH2S)+
lnfCO2(pCO2)+lnfv(v)+C
(16)
式中:K为其他因素的影响;fT(T)为温度的影响函数;fH2S(pH2S)为H2S分压的影响函数;fCO2(pCO2)为CO2分压的影响函数;fv(v)为流速的影响函数;C为常数项。
根据表3提到的各影响因素的排序可知,在CO2/H2S分压比为33~300时,腐蚀反应由H2S主导控制。常见的H2S/CO2体系中H2S为主导的模型如式(17)所示,该模型只考虑H2S分压和CO2分压对腐蚀速率的影响。
lnvcorr=AlnpH2S+B(lnpH2S)2+KlnpCO2+C
(17)
上述模型考虑了CO2/H2S分压比对腐蚀速率的影响,但并未考虑温度与流速的影响。由于本工作的正交试验以温度、H2S分压、CO2分压、流速的影响为主要考虑因素。故进一步考虑温度和流速对腐蚀的的影响,在CO2/H2S体系中其他影响因素不改变的条件下,温度对腐蚀速率的影响可用式(18)表示[23]:
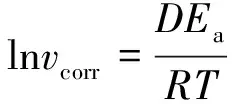
(18)
式中:R为普适气体常量,J/(mol·K);T为绝对温度,K。
基于正交试验得到的不同流速下管道的腐蚀速率,提出了其他影响因素不改变条件下流速对管道腐蚀速率的影响公式,见式(19):
lnvcorr=Elnv
(19)
结合式(17)~(19),提出了L360管道在不同H2S分压、CO2分压、温度以及流速下的腐蚀速率预测模型,式中通过系数调整不同影响因素对腐蚀速率的影响权重,见式(20)。
lnvcorr=AlnpH2S+B(lnpH2S)2+KlnpCO2+
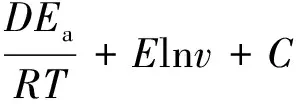
(20)
式中:A、B、K、C、D、E为待确定的系数,Ea为钢材的反应活化能。
为了确定腐蚀预测模型中的各系数,选取9组L360钢腐蚀速率正交试验的前7组代入式(18),采用MATLAB软件中的多元线性回归方程分析和拟合,得到流动状态下L360钢在H2S/CO2共存体系下的腐蚀速率预测模型的各项系数,如式(21)所示。腐蚀速率实测值与MATLAB拟合值如图4所示,分析结果表明,实测值与拟合结果吻合度良好。将第8、9组腐蚀速率的实测值带入式(21),计算误差分别为3.06%和9.71%,最大的误差不超过10%,这表明提出的腐蚀预测模型具有较高的精度。


图4 实测值与拟合值的对比分析Fig. 4 Comparative analysis of measured values and fitted values
该模型适用于温度35~55 ℃,H2S分压0.001~0.003 MPa,CO2分压0.1~0.3 MPa,流速1.5 ~2.5 m/s的含硫湿天然气管道。
3 结论
(1) 根据三水平四因素的正交试验结果,可知各影响因素对腐蚀速率的影响程度排序:H2S分压(0.050)>温度(0.040)>流速(0.008)>CO2分压(0.005);随着温度的升高、流速的增大、CO2分压的增大、H2S分压的增大,腐蚀速率呈上升趋势。
(2) 对试样表面腐蚀产物进行SEM、EDS、XRD表征,确定了CO2/H2S共存体系分压比为33~300时,腐蚀产物主要为FeS,反应过程主要由H2S控制,腐蚀形态多以均匀腐蚀为主,部分位置存在局部腐蚀坑。
(3) 基于常用的H2S/CO2共存体系腐蚀速率模型,建立了L360钢材在气相环境中的腐蚀速率预测模型,该模型不仅考虑了H2S与CO2分压,还考虑了温度与流速对管道腐蚀速率的影响,利用MATLAB多元线性回归方法结合7组试验数据拟合出了该腐蚀预测模型的各项系数,并对剩余2组试样的腐蚀速率进行验证计算,结果表明建立的模型误差小于10%,精度较高。

