困难条件新型冠状病毒肺炎患者行经皮扩张气管切开术1例体会
曹鹏宇 张中伟 李颖川
(1.上海市公共卫生临床中心 上海 201508;2.复旦大学附属眼耳鼻喉科医院耳鼻咽喉头颈外科 上海 200031;3.上海交通大学附属第六人民医院重症医学科 上海 200233)
2019年12月以来,湖北省武汉市发现了多例新型冠状病毒肺炎患者。该病作为急性呼吸道传染病已纳入《中华人民共和国传染病防治法》规定的乙类传染病,按甲类传染病管理[1]。2020年2月11日世界卫生组织(WHO)正式将该病命名为coronavirus disease-19(COVID-19)[2]。COVID-19由新型冠状病毒(2019 novel coronavirus,2019-nCoV)感染引起,国际病毒分类委员会重新命名这种病毒为严重急性呼吸道综合征冠状病毒2型(severe acute respiratory syndrome coronavirus-2,SARS-CoV-2)[3]。
COVID-19以发热、乏力和干咳为主要表现,部分患者会有气促和腹泻[4]。重型患者多在发病1周后出现呼吸困难和(或)低氧血症,严重者可快速进展为急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)、脓毒症休克、代谢性酸中毒和出凝血障碍及多器官功能衰竭等[1]。氧疗是COVID-19患者的重要治疗手段,特别是危重患者,经常需要经气管插管和有创机械通气[4]。
气管切开术是最古老的手术之一,传统开放式外科气管切开术(surgical tracheotomy,ST)一直是被广泛使用的标准术式[5],适应证包括上呼吸道梗阻、下呼吸道分泌物潴留或预期需要超过10~14 d的机械通气[6]。经皮扩张气管切开术(percutaneous dilatation tracheotomy,PDT)最早于1985年由Ciaglia报道,由于操作相对简单,单人可在床边完成,重症监护医师更愿意、更适合采用这种术式[7]。我们在此次疫情期间,在上海市公共卫生临床中心参与1例危重型COVID-19患者的PDT,在此分享从术前准备到手术过程的体会和思考。
1 资料与方法
1.1 病例资料 女性,57岁。因“发热3 d”入院。患者2月3日出现发热,体温38.5 ℃,伴咳嗽,少许白痰,无气喘,无腹泻。胸部CT:肺部感染(图1、2),留观采样,2月5日咽拭子结果显示2019-nCoV核酸检测阳性。2月6日转入上海市公共卫生临床中心隔离治疗。流行病学史:无湖北旅行史,否认接触COVID-19患者。身高165 cm,体重75 kg。既往有高血压病史、糖尿病史多年。诊断:COVID-19、高血压病、糖尿病。2月8日晚,患者高流量吸氧时(氧浓度90%),氧饱和度维持在90%左右,考虑进展为危重型,给予气管插管机械通气后,氧饱和度维持在96%左右。2月17日上午,行床旁气管切开术。
1.2 术前准备 COVID-19患者的上、下呼吸道分泌物均可以检测出病毒[1]。气管切开术过程中,患者的血液、口腔分泌物和下呼吸道分泌物容易溅出,若无充分保护,医护人员被感染的风险非常高。基于2003年SARS期间对“非典”患者进行气管切开的经验[8],进行术前准备。此例患者体态偏胖,颈部短粗,皮下组织厚,颈段气管触摸不清,遂请耳鼻咽喉头颈外科医师参与手术。
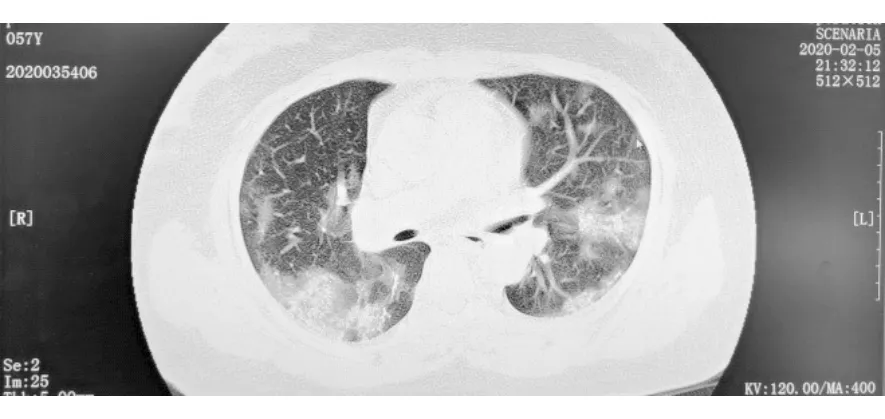
图1 患者2月5日入院时肺部CT表现
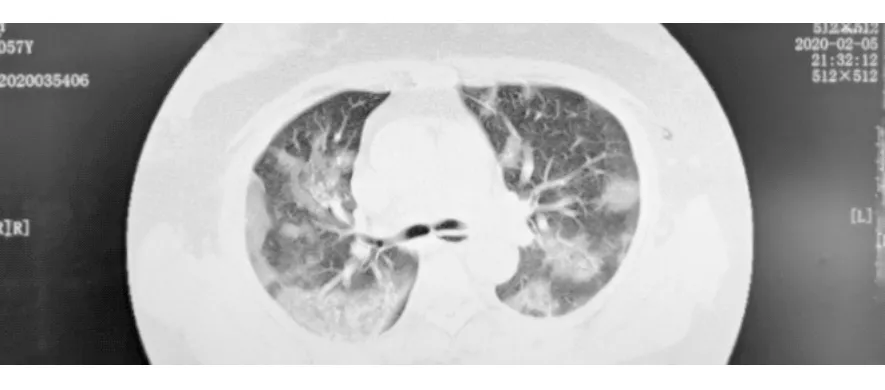
图2 患者2月5日入院时肺部CT表现
1.2.1 手术环境和手术人员 手术在重症监护室负压病房内进行。手术参与人员包括重症监护医师2人(1人参与手术,1人负责监视患者生命体征变化),耳鼻咽喉头颈外科医师1人,护士2人。
1.2.2 防护设备和手术器械 在清洁区内更换隔离衣和工作鞋,按照三级防护标准穿戴全部防护用品(表1)[9]。穿戴顺序:清洗双手,戴一次性防水帽,戴N95口罩,穿一次性防水长鞋套,穿一次性防水隔离防护服,穿防水短鞋套,戴双层医用乳胶手套,戴动力送风过滤式呼吸器及头罩,穿戴完毕后进入污染区。手术前穿一次性外科手术衣和一次性外科手套。手术器械包括PDT包1套、常规气管切开包1套(备用)、硅胶气管套管1副、负压吸引器和电刀(备用)。

表1 医护人员个人防护等级
注:有条件时,或者在武汉等疫情高发区,可提升医护人员个人防护级别,如急诊接诊时穿戴二级防护用品;接触患者时均穿戴三级防护用品;二级以上防护有条件时可使用动力送风过滤式呼吸器。
1.3 手术过程要点 先行PDT,ST作为备选。①气管插管全身麻醉,使患者肌肉完全松弛,充分镇静和镇痛,确保患者没有咳嗽反射或任何其他动作。②气管切开手术开始前将呼吸机吸入氧浓度调高至100%。③以环状软骨下2横指,颈部中线为穿刺点,带水穿刺针垂直向气管方向进针,抽及气泡,留下套管,导丝引入气管内前,先将气管插管拔到穿刺点上方。④以穿刺点为中心,横行切开约1.5 cm,扩张气管壁时应停止机械通气。⑤置入气管套管时必须确保患者无咳嗽,插入气管套管后充气。⑥将气管套管与呼吸机连接,确认通气正常没有漏气后,颈部固定气管套管。⑦取出气管导管,整理全部手术器械,脱手术衣和手套,手术结束。呼吸机逐渐回调至术前模式。
1.4 脱卸防护设备 进入缓冲区后脱卸防护用品。脱卸顺序:手卫生→取下动力送风过滤式呼吸器和头罩→手卫生→脱短鞋套→脱外层手套→手卫生→半脱隔离服→手卫生→脱内层手套→手卫生→脱隔离服→手卫生→脱长鞋套→手卫生→脱N95口罩和帽子→手卫生→鞋底消毒→手卫生→离开缓冲区→戴一次性帽子和医用口罩→前往淋浴区沐浴后更换隔离衣。
2 结果
手术过程顺利,切口无明显渗血,无皮下气肿。患者经气管套管机械通气,氧饱和度为96%左右,其他生命体征稳定。经过治疗后,2月26日复查肺部CT,肺部炎症渗出较入院时大部分吸收(图3)。
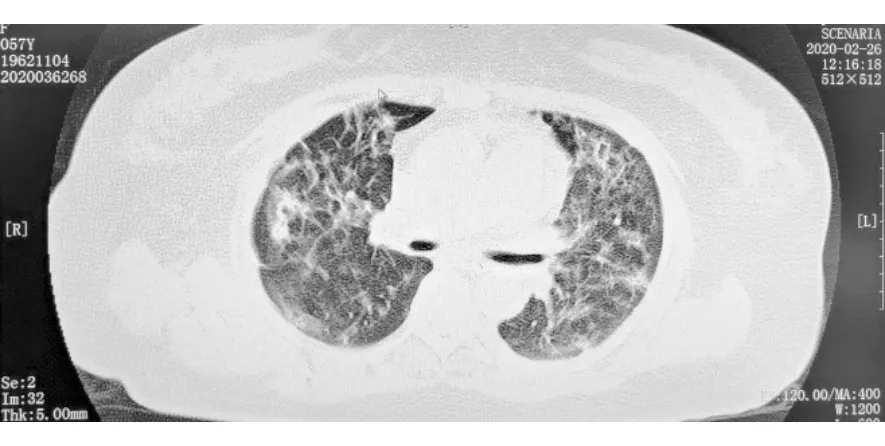
图3 患者气管切开9 d后2月26日肺部CT表现
3 讨论
3.1 ST和PDT的比较 Jackson在1909年发明标准的ST,使其成为一项安全的技术,并沿袭使用至今[10]。随着机械通气和ICU的出现,气管切开术适应证从最初解除急性呼吸道梗阻拓展为建立人工气道的手段之一。ST通常在手术室由耳鼻咽喉科医师完成,需要助手配合,费时较长,对术者要求高,这些特点限制了非耳鼻咽喉科医师掌握此手术。PDT通过经皮肤穿刺入气管并在气管中插入导丝,穿刺点应在第一、二气管环之间或第三、四气管环之间进行。Ciaglia方法使用不同尺寸的亲水涂层扩张器逐级扩张气管前组织,最终允许气管套管插入气管[7]。
PDT因手术时间短、操作简便,单人可以在ICU床边完成,减少重症患者来回转运的潜在危险[7]。尽管ST也可在床边进行,但是从节约费用的角度,在国外PDT仍然更有优势。在国内可能恰恰相反,由于目前PDT一次性手术器械仍需进口,导致PDT的耗材费用反而成为劣势。PDT其他的优势包括切口小,拔管后创面愈合快,瘢痕小;气管套管与周围组织贴合更紧密,使术后发生皮下气肿、出血和切口溢痰、切口局部感染等机会较少[11]。
PDT是开放式气管切开术的安全替代选择,就围手术期并发症发生率而言,没有资料表明两者孰优孰劣[12]。PDT应该被添加到耳鼻咽喉科医师的外科气道手术列表中,手术应该由有能力在PDT失败时,具备紧急开放气道或颈部探查能力的外科医师实施[13]。ST比PDT更有优势的适应证包括:紧急气管切开术;解剖标志触摸不清(非常肥胖、颈短或牛颈、甲状腺肿大、环状软骨摸不到或气管明显偏移);气管造口部位的恶性肿瘤[7]。本例COVID-19患者是1例超重女性,体重指数为27.5,属于超重上限[14],颈部短粗,解剖标志触摸不甚清楚,ICU医师认为独自进行PDT有不确定的风险,遂请求耳鼻咽喉科医师协助手术。同时准备一套ST手术器械,如果PDT失败转行ST,最终成功完成PDT。
在肥胖或有颈部畸形患者中,如果遇到解剖标志(如环甲膜) 定位不清,气管不易触及辨别时,上气道超声扫描可以提供重要的解剖学信息,包括气管前区和气管旁区[15]。超声是安全、快速、可重复、便携和广泛使用的工具,可以在PDT之前识别颈部脆弱结构,如血管和甲状腺,使针头和扩张器远离危险结构,从而避免血管并发症[16]。超声扫描使气管环清晰可见,有利于确认正确的气管穿刺位置和保持正中线[17]。与仰卧位胸部X线片相比,超声对筛查气胸更为灵敏(超声诊断气胸的时间为7 min,而X线为80 min)[18]。因此,超声引导下PDT是一项安全、便捷、省时的气管切开术,尤其适于PDT初学者和单独对颈部条件不好的患者进行,并且超声诊断气胸比X线检查更有优势。
3.2 COVID-19患者气管切开术的麻醉 行ST或PDT时,局部麻醉或全身麻醉都可以使患者获得良好耐受。采用何种麻醉方式取决于原发疾病、颈部条件、术者习惯和手术地点。局部麻醉手术时由于咳嗽反射更易发生喷溅[19-20]。在ICU床边手术时,患者多数已处于气管插管状态[21],对患者进行镇静、镇痛或全身麻醉更方便,在保证通气条件下进行手术操作会更从容。基于SARS患者气管切开的经验[8],我们建议对COVID-19患者进行气管切开时必须采用气管插管全身麻醉,使患者肌肉完全松弛,避免主动喷溅呼吸道分泌物。手术过程中给予100%氧气,切开气管壁时暂停机械通气,以防呼吸机压力导致被动喷溅分泌物。置入气管套管充气后,再接呼吸机重新恢复机械通气。麻醉关键是在整个手术过程中确保患者没有咳嗽反射和任何其他动作,避免喷溅分泌物,减少病原体传播,减少医护院内感染机会。
3.3 COVID-19患者气管切开术的时机 目前认为ICU内患者早期进行气管切开术(插管10 d内)可以获得更长的无需机械通气天数、更短的ICU停留时间、更少的镇静药物剂量,不会增加气管切开相关死亡率,减少长期死亡率[21]。与气管插管相比,气管切开术有利于改善呼吸力学,清除气道分泌物,减少喉溃疡发生率,利于提高营养,改善患者舒适度[22]。也有学者[23]总结SARS的治疗经验后认为,在重症SARS患者中,有创机械通气应慎用,气管切开术对治疗无特殊积极意义。
15%~30%的COVID-19患者会出现ARDS。国内外临时治疗指南对出现ARDS时治疗的建议,除了有创机械通气,也包括对有难治性低氧血症患者进行体外膜肺氧合(extracorporeal membrane oxygenation,ECMO)治疗[1,24]。血液净化技术可清除体内多余的水分和毒素,还可清除细胞因子和炎性介质,因此连续性肾脏替代治疗 (continuous renal replacement therapy,CRRT)也是危重型COVID-19患者的治疗手段之一[25]。ECMO和CRRT过程中均需持续抗凝[26-27],因此有易出血倾向。故对危重型COVID-19患者,是否进行气管切开术需由ICU医师综合多因素考虑,包括疾病进展程度、插管时间、患者年龄、基础疾病、家属意愿等。对气管切开时机要有预判,如果预期进行ECMO或CRRT,至少在相应治疗开始前24~48 h进行手术。尽量避免在抗凝状态下行气管切开,利于减少术中和术后出血。由于COVID-19属于全新传染病,无论对于疾病的病理生理特征,还是诊疗模式都没有成熟方案遵循,对于危重型病例的治疗更需要不断观察总结,适时做出调整,预判比较困难。因此本例患者虽然没达到需要ECMO或CRRT的程度,但在治疗过程中病情稳定,逐渐恢复,因气管插管时间将超过10 d而行气管切开术。
3.4 对COVID-19患者诊疗的防护要求 2019-nCoV主要通过呼吸道飞沫和密切接触传播,有症状的COVID-19患者和无症状的感染者都是传染源,潜伏期在1~14 d,人群普遍易感[1]。从感染人数上看,MERS有2 000多人患病,SRAS有8 000多人患病,而COVID-19目前已有80 000多人患病,且感染人数还在不断上升,全球各地陆续出现感染者[28]。2019-nCoV的基本传感数(R0)也比SARS冠状病毒高[29]。这表明2019-nCoV传染性强、潜伏期长,有更强的传播能力。医疗单位应该根据工作岗位和职责不同给医护人员配备不低于相应防护等级的防护用品,减少院内感染机会[9]。在COVID-19患者的监护病房里,需要采集患者各种样本,进行气道护理、口腔护理、吸痰、深静脉置管、气管插管和气管切开术、呼吸机辅助呼吸、ECMO或CRRT等护理和治疗,必须配备最高等级的三级防护。有条件者应当配备动力送风过滤式呼吸器,有助于降低呼吸负荷,减少眼镜和头罩面屏内起雾,改善佩戴舒适度,提高防护可靠性。脱卸防护用品时,动作缓慢,幅度不宜过大。每个脱卸动作之间严格强调手卫生,避免手部触碰隔离服外表面。一旦有触碰或可疑触碰立即进行手卫生消毒。
综上所述,对危重型COVID-19患者,是否进行气管切开术需由ICU医师综合多因素考虑,尽量避免在抗凝状态下手术。ICU医师对COVID-19患者进行PDT是安全、方便的选择。对于颈部条件不好的患者,可以请耳鼻咽喉科医师协助或采取超声引导下PDT。手术过程中确保患者处于肌松状态,没有咳嗽反射和任何其他动作,避免喷溅分泌物。对于接诊或处置COVID-19患者,操作人员应该采用三级防护标准的防护用品。
——工会参与尘肺病预防实用指南》—— 检查要点20 为劳动者提供适宜的个人防护用品,并确保正确使用和良好维护(连载六)

