4 826 例免疫抑制剂及相关器官移植用药致药品不良反应自发报告分析Δ
高 奥,郭代红,姚 翀,赵鹏芝(中国人民解放军总医院医疗保障中心药剂科,北京 100853)
免疫抑制剂主要用于抑制各种对机体不利的免疫反应,如器官移植排斥反应和自身免疫性疾病,常用类别包括钙调磷酸酶抑制剂、糖皮质激素、抗代谢/增殖药和烷化剂等[1-2];因某些肿瘤的治疗机制与免疫抑制相关,故免疫抑制剂也用于抗肿瘤治疗。 移植手术已成为人体器官衰竭终末期的常规且有效的治疗手段,但由于免疫排斥存在,术后需长期应用免疫抑制剂,发生药品不良反应(adverse drug reaction,ADR)的概率增加。 为此,本研究采用回顾性研究方法,对中国人民解放军ADR 监测中心收集到的目标药物所致ADR 及从中筛查出的器官移植用药所致ADR 进行对比分析及讨论,旨在为临床合理使用免疫抑制剂提供参考。
1 资料与方法
1.1 资料来源与方法
采用回顾性研究方法,提取2009 年1 月1 日至2019 年1 月1 日中国人民解放军ADR 监测中心收集的ADR 自发报告中,来自151 家医院第一怀疑药品为免疫抑制剂的ADR 报告[3];并根据《WHO 不良反应术语集》中首选术语(preferred term,PT)对ADR 报告进行规范化整理。 纳入标准:根据《新编药物学》(第17 版)、《临床用药指南》(第3 版)对免疫抑制剂规范分类,结合国内外文献检索[1-2],共计27 个品种;依照《药品不良反应术语使用指南》的ADR/药品不良事件关联性评价标准,判断为“肯定”“很可能”和“可能”的有效报告,纳入为免疫抑制剂及相关器官移植用药致ADR 报告;然后,根据ADR 报告中“既往病史”“临床诊断”以及“不良反应表述”等内容,从中筛查出明确为器官/组织移植患者的相关ADR报告,纳入为相关器官移植用药致ADR 报告。
1.2 统计学方法
利用Excel 2013 软件进行数据整理,采用SPSS 22.0 统计学软件进行数据统计分析;采用χ2检验,P<0.05 表示差异有统计学意义。
2 结果
2.1 ADR 报告概况
共收集免疫抑制剂致ADR 报告4 826 例,其中相关器官移植用药致ADR 报告442 例(占9.16%)。 4 826 例ADR 报告中,一般的ADR 为4 151 例(占86.01%),包括一般的ADR 3 843例(占79.63%)、新的一般的ADR 308 例(占6.38%);严重的ADR 为675 例(占13.99%),包括严重的ADR 654 例(占13.55%)、新的严重的ADR 21 例(占0.44%)。 442 例相关器官移植用药致ADR 报告中,一般的ADR 为367 例(占83.03%),包括一般的ADR 337 例(占76.24%)、新的一般的ADR 30 例(占6.79%);严重ADR 为75 例(占16.97%),包括严重的ADR 74 例(占16.74%)、新的严重的ADR 1 例(占0.23%)。
2.2 发生ADR 患者的性别与年龄分布
4 826 例发生ADR 的患者中,男女之比为1 ∶1;≥60 岁老年患者中发生严重的ADR 病例数所占比例为16.49%(186/1 128),明显高于<60 岁患者中发生严重的ADR 病例数所占比例(13.22%,489/3 698),差异有统计学意义(P=0.006)。442 例相关器官移植用药发生ADR 的患者中,男女之比为2.09 ∶1;因老年患者样本量少,严重的ADR 病例数所占比例偏差大,故未进行统计学分析。
2.3 发生ADR 的给药途径分布
4 826 例ADR 的给药途径中,静脉给药最为多见,共3 585 例(占74.29%),包括静脉滴注3 397 例、静脉注射188 例;442 例相关器官移植用药致ADR 中,静脉给药引发的ADR 共240 例(占54.30%),包括静脉滴注233 例、静脉注射7 例,见表1。

表1 发生ADR 的给药途径分布Tab 1 Distribution of administration routes of ADR
2.4 ADR 发生时间分布
4 826 例ADR 中,发生于用药后2 ~<7 d 的ADR 病例数所占比例最高(21.57%);442 例相关器官移植用药致ADR中,发生于用药后≥15 d 的ADR 病例数所占比例最高(21.95%),见表2。
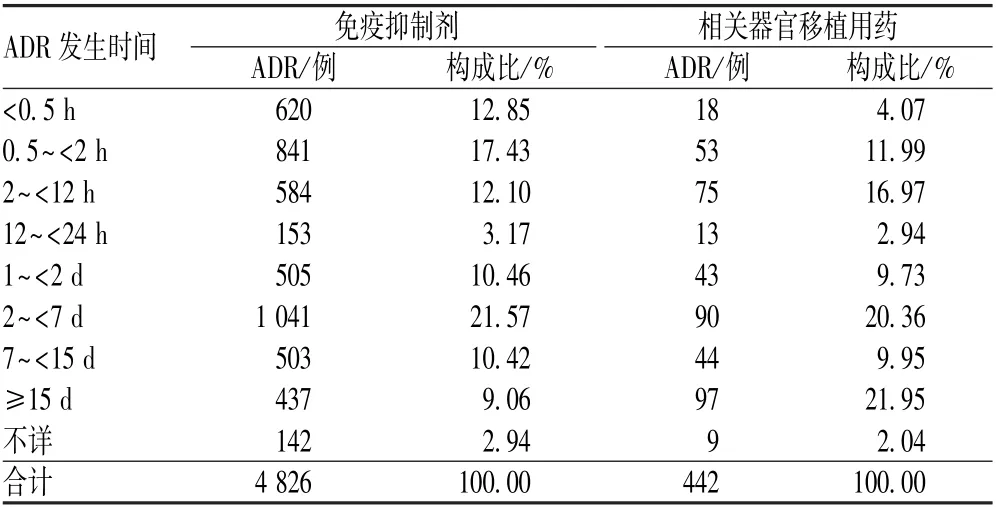
表2 ADR 发生时间分布Tab 2 Distribution of occurrence time of ADR
2.5 引发ADR 的药品种类分布
4 826 例ADR 共涉及27 种免疫抑制剂,引发ADR 病例数排序居前3 位的为糖皮质激素、抗体和烷化剂,引发ADR 病例数排序居前5 位的药品为甲泼尼龙、地塞米松、环磷酰胺、甲氨蝶呤和利妥昔单抗,见表3。 442 例相关器官移植用药致ADR 涉及20 种免疫抑制剂,引发ADR 病例数排序居前3 位的为钙调磷酸酶抑制剂、抗体和抗代谢/增殖药,引发ADR 病例数排序居前5 位的药品为环孢素、他克莫司、抗淋巴/胸腺细胞球蛋白、吗替麦考酚酯和甲泼尼龙,见表4。
2.6 ADR 累及器官和(或)系统及主要临床表现
4 826 例ADR 主要累及胃肠系统、全身和皮肤及其附件,主要临床表现为恶心、呕吐、皮疹、肝功能异常和发热;严重的ADR 以血液系统不良反应为最多,见表5。 442 例相关器官移植用药致ADR 主要累及全身、胃肠系统和神经系统,主要临床表现为发热、腹泻、白细胞减少、肝功能异常和恶心;严重的ADR 以血液系统不良反应为最多,见表6。
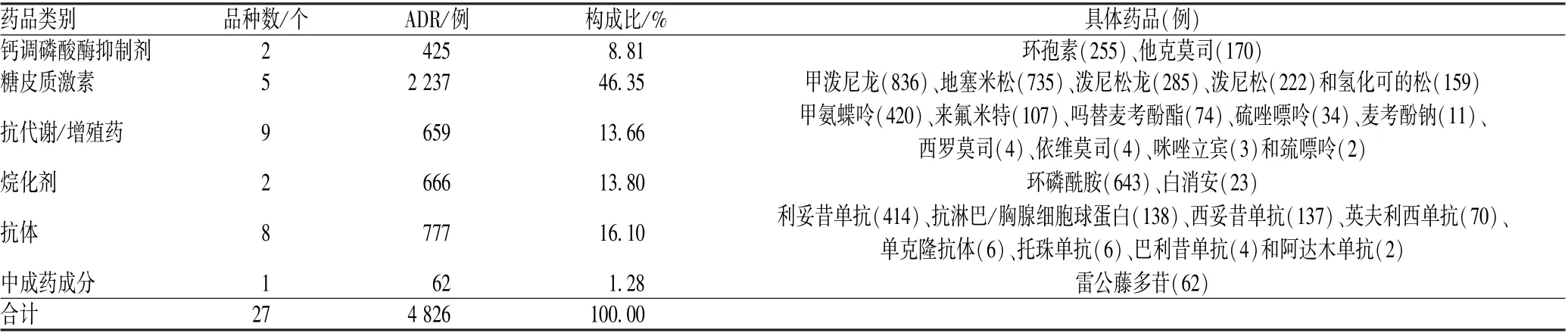
表3 引发ADR 的药品种类分布Tab 3 Distribution of categories of ADR-inducing drugs

表4 引发ADR 的相关器官移植用药种类分布Tab 4 Distribution of categories of ADR-inducing drugs in related organ transplantation
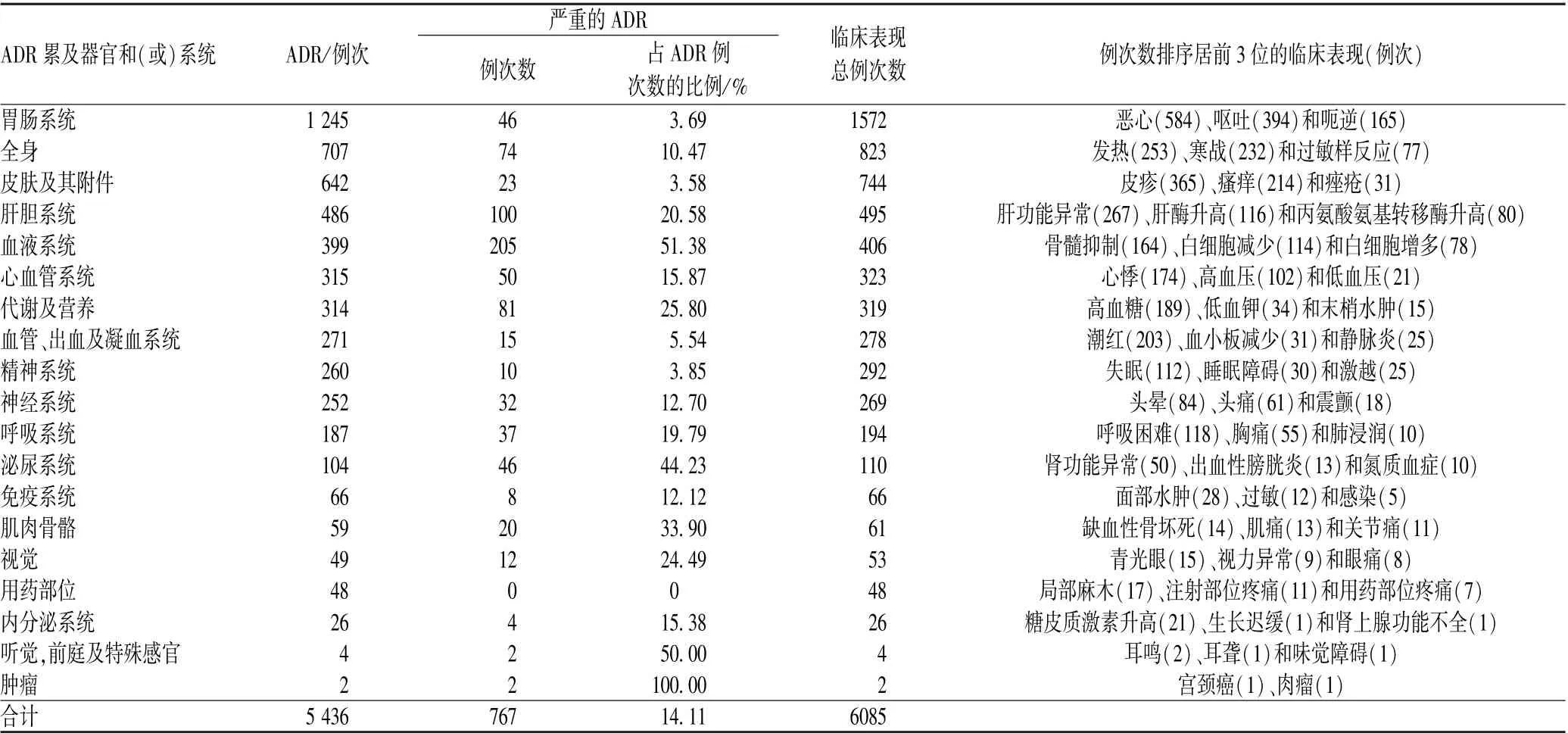
表5 ADR 累及器官和(或)系统及主要临床表现Tab 5 Systems and (or) organs involved by ADR and main clinical manifestations
2.7 患者的转归情况
4 826 例发生ADR 的患者中,4 314 例(占89.39%)经治疗后痊愈或好转,4 例死亡;442 例相关器官移植用药发生ADR 的患者中,379 例(占85.75%)经治疗后痊愈或好转,1 例死亡,见表7。 死亡病例情况见表8。
3 讨论
3.1 ADR 与个体因素
本研究纳入的4 826 例免疫抑制剂致ADR 报告中,男性、女性患者构成比基本相等;而442 例相关器官移植用药致ADR 报告中,男女之比为2.09 ∶1,虽为自发报告,但也可反映出临床接受移植手术的男性患者远超女性患者,朱姝娟等[4]的研究结果亦有相似表现,主要是受到传统家庭观念、经济因素以及社会因素等多方面影响,而国外也存在着接受移植后将丧失医疗保险资格以及某些宗教思想对女性接受移植手术的负面影响等情况。 ≥60 岁老年患者中严重的ADR 病例数所占比例显著高于<60 岁患者,其主要原因是因为老年人生理机能减退,免疫功能降低,易感染各类疾病,且联合用药的概率较高,用药依从性较差。 世界卫生组织的一项统计结果显示,约14%的老年人死于不合理用药,而非死于自然衰老或疾病[5-6]。因此,对老年人的用药指导应引起药师的重视。 本研究纳入的4 826 例报告中,患者年龄主要集中于30~44 岁,相较于442 例相关器官移植用药致ADR 报告的45~59 岁更趋于年轻化,推测是目前成功接受移植手术患者的年龄分布的反映;尽管年龄不是影响移植手术的主要因素,但年龄相关疾病会影响术前评估,导致年龄较大的患者更难获得手术机会。

表6 器官移植用药致ADR 累及器官和(或)系统及主要临床表现Tab 6 Systems and (or) organs involved by ADR induced by medication in related organ transplantation and main clinical manifestations
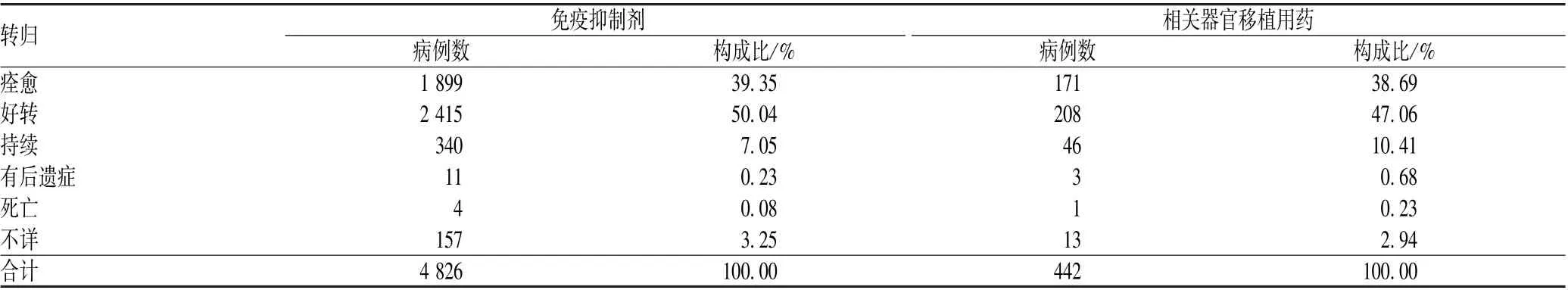
表7 发生ADR 患者的转归情况Tab 7 Outcomes of patients with ADR

表8 死亡病例情况Tab 8 Cases of death
3.2 引发ADR 的给药途径及发生时间
本研究结果显示,引发ADR 的给药途径中,最主要的为静脉给药,其次为口服给药;且442 例相关器官移植用药致ADR报告中口服给药病例数所占比例高于4 826 例ADR 报告中口服给药病例数所占比例,其原因在于移植术后患者需要长期用药,而口服为出院后最便捷的给药途径。 口服给药后需经消化道吸收,ADR 多表现为轻度胃肠系统损害;而静脉给药能够很快达到需要的血药浓度,起效快,但由于药物直接进入血液,ADR 的发生率和严重程度会高于口服给药[7]。 因此,医师需根据患者病情和治疗需要,选择适宜的药品剂型及给药方式。
本研究结果显示,ADR 主要发生于用药后2 ~<7 d(占21.57%),其次为用药后0.5~2 h(占17.43%),与寇炜等相关研究结果类似[8]。 主要原因为体内不同器官或系统对免疫抑制剂的敏感度和代偿性不同,胃肠道不良反应最容易发生在用药后0.5~2 h,而骨髓、肝胆有一定的代偿能力,故ADR 发生时间相对较晚。 相关器官移植用药致ADR 主要发生于用药后≥15 d(占21.95%),应该是术后代谢紊乱,有害代谢产物难以排除,进而累积,导致ADR 发生。 移植术后患者应定时进行体内血药浓度监测,并及时调整药量或更换药品,以减少ADR 发生。
3.3 免疫抑制剂种类及重点药品
4 826 例ADR 主要涉及糖皮质激素、抗体和烷化剂。 甲泼尼龙和地塞米松等糖皮质激素作为最早被应用的免疫抑制剂,虽然ADR 较多,但因其药理作用具有不可替代性,仍广泛应用于抗变态反应,风湿、类风湿及肾病综合征等自身免疫性疾病和器官移植的急性排斥反应。 环磷酰胺作为烷化剂的代表药品,除用于器官移植术的免疫抑制治疗外,对白血病、恶性淋巴瘤及进行性自身免疫性疾病也具有显著疗效。 抗肿瘤药甲氨蝶呤经剂量、用法调整后,可作为免疫抑制剂用于治疗银屑病关节炎、红斑性狼疮和多发性肉芽肿等。 利妥昔单抗是第1 代抗CD20 单克隆抗体,主要用于非霍奇金淋巴瘤、滤泡性中央型淋巴瘤、肉芽肿病和血管炎等疾病[9-10]。
442 例相关器官移植用药致ADR 主要涉及钙调磷酸酶抑制剂、抗体和抗代谢/增殖药,这与器官或组织移植免疫抑制治疗指南推荐的治疗方案用药相吻合[11-15]。 术前的免疫诱导、术后的免疫抑制维持治疗是一个长期的动态过程,影响因素很多,需根据患者监测情况进行个体化药物治疗。
3.4 ADR 累及器官和(或)系统、主要临床表现及患者转归
本研究结果显示,ADR 累及的器官和(或)系统以胃肠系统和全身为主,主要临床表现为恶心、呕吐、发热和寒战等;累及肝胆系统的主要临床表现为肝功能异常、肝酶升高等;严重的ADR 以血液系统不良反应多见,主要临床表现为骨髓移植、白细胞减少等。 而相关器官移植用药致ADR 中的神经系统损害更为突出,主要临床表现为头痛、震颤等。 值得关注的是,文献报道,移植术后患者由于长期使用免疫抑制剂可能有引发肿瘤的风险[16-18],而本研究的自发报告中则少见。
与4 826 例免疫抑制剂致ADR 总体情况比较,相关器官移植用药致ADR 报告中治疗后痊愈或好转的病例数所占比例更小,应该是与移植术后患者机体状态有关,其ADR 持续时间相对较长,因为患者为了维持生命必须坚持服药,所以选择承受较轻的ADR。 4 例死亡报告中,2 例为抗体类药品相关过敏反应,发生于用药后30 min 内,提示过敏性反应是抗体类免疫抑制剂的风险关注重点;1 例为来氟米特治疗肾病综合征2 个月后发生间质性肺炎导致呼吸衰竭引起死亡,系国内报道的首例来氟米特引发间质性肺炎致死病例;1 例为肾移植术后服用环孢素6 年引发肉瘤并扩散造成弥漫性血管内凝血导致死亡,提示临床长期使用免疫抑制剂时应密切监护,及早发现恶性肿瘤特别是皮肤肿瘤,及时予以干预[19]。
3.5 免疫抑制剂应用的风险防范思考
免疫抑制剂的发现与使用为器官或组织移植提供了前所未有的支持,但术后患者仍需长期抗排斥反应,不良反应无法避免。 学者们一直致力于寻找更好的解决方案,包括开发疗效好、不良反应小的新药,尝试免疫检查点阻断、诱导混合嵌合体和过继细胞转移等新方法[20-21]。 而在现有技术水平下,既要合理用药以减少患者病痛,又要保障患者术后存活时间和生活质量,应考虑在治疗开始前坚持个体化评估,选择合适的治疗方法及药物;治疗开始后定期进行血药浓度监测,及时调整用药剂量或给药方式;尤其是针对老年患者进行重点监护,及时有效干预,尽可能防范严重的ADR 发生。

