酒石酸辅助均匀沉淀法制备TiO2/氧化锡锑
王亚男,马坤怡,王佳爽,钱建华,邢锦娟,刘琳
(1.渤海大学辽宁省功能化合物的合成及应用重点实验室,辽宁锦州,121013;2.东北大学 材料科学与工程学院,辽宁 沈阳,110819;3.辽宁石油化工大学化学化工与环境学部,辽宁抚顺,113001)
核-壳粒子因其核与壳之间的协同作用,在催化[1-2]、磁性复合材料[3]、靶向药物[4]等领域中被广泛应用。因此,合理设计和制备具有不同性能的核-壳结构材料是研究的重点。目前,核-壳复合粉体的制备方法主要有机械混合法[5-6]、水(溶剂)热法[7]和基体包覆法,如共沉淀法[8]、均匀沉淀法[1]和Pechini 法[9]等,其中,因沉淀剂缓慢水解释放氢氧根可以有效地控制粒子的大小和形状而合成超细氧化物及其他复合材料,均匀沉淀法已被广泛应用。采用无机/无机包覆技术对无机核体粒子进行表面改性,所得复合填料填入高电阻率的高分子基质中制成抗静电涂料、塑料及纤维等导电/抗静电材料,可避免出现一系列静电吸引及静电放电等危害问题。因此,基于二氧化钛优异的理化性能如散射性能和化学稳定性等,以二氧化钛为基核,表面包覆无机导电壳层材料制成核-壳复合导电填料的研究已成为热点。锑掺杂二氧化锡(ATO)具有高导电性、良好的光学透明性、红外阻隔性能、化学稳定性等优点[10-11],是理想的壳层材料。目前,制备复合导电粉体的方法中,共沉淀法由于Sn4+和Sb3+极易水解,需依靠大量盐酸来抑制水解,对应消耗大量碱共沉淀,对环境造成一定的污染,同时共沉淀时并不能实现真正掺杂;溶胶-凝胶法虽然工艺简单且所得产物组成及粒度可控,但原料一般为金属有机醇盐附加一些有机溶剂,成本较高且有一定的毒性[12]。因此,采用酒石酸辅助均匀沉淀法制备TiO2/ATO,一方面,为了避免由于碱性沉淀剂的直接加入而导致局部OH—浓度过高的现象,采用了均匀沉淀法;另一方面,利用络合原理使体系中的金属阳离子与酒石酸根配体络合,在一定条件下逐步释放构晶阳离子,使其达到原子级的均匀混合,解决了制备过程中的两大难题。此方法为低成本制备二氧化钛基浅色复合导电粉体以及其他功能复合材料提供了新的思路。在此,本文作者以TiO2为基核,锡锑氯盐的乙醇溶液为包覆溶液,尿素为均匀沉淀剂,采用酒石酸辅助均匀沉淀-热处理法制备核-壳结构TiO2/ATO复合导电粉体。该复合材料可作为导电专用填料应用于其他基料中制成导电、抗静电材料。
1 实验
1.1 试剂与仪器
实验试剂有尿素(Urea,天津光复科技发展有限公司生产)、聚乙烯吡咯烷酮(PVP,天津市光复精细化工研究所生产)、酒石酸(TA,天津百伦斯生物技术有限公司生产)、结晶四氯化锡(SnCl4·5H2O,天津市致远化学试剂有限公司生产),以上试剂均为分析纯;还有三氯化锑(SbCl3,天津市科密欧化学试剂有限公司生产,化学纯)和二氧化钛(TiO2,锦州钛业有限公司生产)。
实验仪器包括S-4800冷场发射扫描电镜(日本日立有限公司);JEM-2100F 场发射透射电子显微镜(日本电子株式会社);K-Alpha型X线光电子能谱仪(美国赛默飞世尔科技公司);Rigaku Ultima IV 型X 线粉末衍射仪(日本理学株式会社公司);IRTracer-100型傅里叶变换红外光谱仪(日本岛津);Pyris Diamond型热重分析仪(美国PE公司);SXL-1208 型程序箱式电炉(上海精宏实验设备有限公司);769YP-24B型粉末压片机(中国天津科器高新技术公司);RTS-8型四探针电阻率测试仪(广州四探针电子科技有限公司)。
1.2 复合材料制备
按锡锑物质的量比为10:1 分别称取一定量的SnCl4·5H2O 与SbCl3溶解于35 mL 无水乙醇中,再加入0.10 g的酒石酸,配制成包覆液A。称取2.0 g尿素,加入75 mL去离子水,磁力搅拌溶解,加入1.8 g TiO2,0.018 g PVP 搅拌混和均匀,超声分散60 min,配制成混合浆液B。在反应温度为90 ℃时,通过蠕动泵以0.4 r/min速度将包覆液A逐滴加入到混合浆液B 中,滴加完毕后在90 ℃下继续冷凝回流5 h。反应得到的前驱浆液静置冷却1~2 h,经过滤、洗涤,90 ℃下干燥12 h 后,研磨,所得前驱粉体于空气氛围中550 ℃下煅烧2 h,即得TiO2/ATO复合粉体。
1.3 电阻率测试
利用压片机直径为20 mm 的模具在30 MPa 下将待测样品粉体压成厚度小于4 mm的薄圆片,采用游标卡尺测量样片厚度。采用四探针测试仪测量电阻率,电阻率计算公式如下:

式中:ρ为样品电阻率,Ω·cm;D为样品直径,mm;S为平均探针间距,mm;W为样品厚度,mm;Fsp为探针间距修正系数;F(D/S)为样品直径修正因子;F(W/S)为样品厚度修正因子;I为探针1和4的电流,μA;U为探针2和3间电压,μV。
2 结果与讨论
2.1 复合材料的微观形貌及物相结构
图1(a)和1(c)所示分别为基核TiO2的SEM照片和酒石酸辅助合成的TiO2/ATO复合材料的TEM照片。可见:基核TiO2表面光滑,呈近球状,粒径为200~300 nm(图1(a))。热处理后,沉淀物结晶成ATO 粒子包裹在TiO2表面(图1(c)),包覆壳层与TiO2核有较明显区别,说明形成了核-壳复合结构,即为TiO2/ATO。TiO2/ATO 复合材料的EDS 图(图1(d))及XPS谱图(图2)都进一步表征了其化学组成,经计算可知,Ti,Sn 和Sb 的物质的量比与初始投料比基本一致。图1(e)~1(h)所示为TiO2/ATO的元素面扫描图。从图1(e)~1(h)可以看出:复合物中存在Ti,O,Sn 和Sb 4 种元素,且壳层的Sn和Sb 较均匀地分布在核体TiO2表面,ATO 与TiO2达到均匀复合。
图1(b)所示为无酒石酸辅助合成的TiO2/ATO的SEM 照片。从图1(b)可见:TiO2核外包覆粒子存在较严重的团聚现象,部分基核的外表面未形成有效包覆。对比图1(c)可以看到,加入酒石酸辅助合成的复合材料外层包覆粒子团聚现象明显得到改善,可能是因为反应过程中金属离子先与酒石酸形成络合物,然后随着体系pH变化,缓慢释放Sn4+和Sb3+,所以最终的包覆粒子更加均匀地分布在核外。
图3所示为基核TiO2、复合前驱体、TiO2/ATO及ATO 的XRD 图谱。由图3 可见:复合前驱体的特征峰位均与核体一致,只含金红石型TiO2相,说明复合前驱体的外层沉淀物呈无定型态。ATO和TiO2/ATO 在2θ为26.5°,33.8°,37.6°及51.7°的位置出现了四方相SnO2的衍射峰,未检测到锑氧化物的分相,而EDS 和XPS 结果(图1(d)和图2)又显示Sb的存在,综上分析可得,Sb已经掺杂进入SnO2晶格中。根据XRD 数据并运用Scherrer 公式计算包覆层ATO晶粒的平均粒径Dave:

式中:k=0.89,为谢乐常数;λ=0.154 056 nm,为X 线波长;β为衍射峰的半峰宽;θ为布拉格衍射角。分别选取TiO2/ATO在26.5°处对应的(110)晶面及51.7°处对应的(211)晶面的衍射峰半峰宽来计算,所得包覆粒子ATO的平均粒径为12.3 nm。
2.2 复合前驱体的热重分析

图1 基核TiO2和TiO2/ATO的微观形貌及其EDS分析Fig.1 Microtopography of TiO2,TiO2/ATO and EDS
图4所示为TiO2和复合前驱体的热重曲线。从图4可以看出:在200 ℃以下,由于脱除表面吸附水及其他吸附杂质小分子,基体TiO2质量损失率约为2%,750 ℃以下保持稳定,高于750 ℃的质量变化可能是其生产过程中残余原料TiCl4等的氧化引起。包覆前驱体总的质量损失率为8.4%,受热温度小于100 ℃时,快速失去粉体表面的吸附水,质量损失率约为1.8%。在247.5 ℃以下,前驱体逐渐失去结构水或配位水,其质量损失率约为2.9%。在247.5~316.0 ℃,可能发生残余中间体-金属络合物、酒石酸、NH4Cl及Sb2(CO3)3等的分解反应以及Sb(Ⅲ)向Sb(V)转变的氧化反应;而高于316.0 ℃时,Sb(V)转变为Sb(Ⅲ)的反应趋势加强,此段质量损失缓慢,在247.5~750.0 ℃时,总的质量损失率达3.7%。当温度高于750.0 ℃后,样品几乎无质量损失,说明反应已经基本结束。

图2 TiO2/ATO复合材料的XPS谱图Fig.2 XPS full scanned spectrum of TiO2/ATO

图3 ATO、TiO2、前驱体和TiO2/ATO的XRD图Fig.3 XRD patterns of ATO,TiO2,precursor and TiO2/ATO

图4 TiO2和包覆前驱体的TG曲线Fig.4 TG curves of TiO2 and coated precursor
2.3 酒石酸与尿素对复合材料导电性能的影响
图5所示为其他实验条件相同的情况下,不同酒石酸或尿素加入量下TiO2/ATO 复合材料的电阻率的变化曲线。酒石酸的在体系中既起到提供中间体络合配体的作用,同时也复合尿素起到调节pH 作用。尿素加入量一定,当包覆液中无酒石酸时,包覆液滴入基体悬浮液中,Sn4+和Sn3+直接水解,形成的前驱沉淀物成团聚集,最终导致包覆粒子团聚现象明显,如图1(b)所示,所以部分自团聚的包覆粒子未有效包覆在核表面,造成复合粉体电阻率较高(图5)。当酒石酸加入量较少时,Sn和Sb的络合作用较弱,Sn4+和Sn3+较快水解,导致包覆层粒子过大且粒径不均匀,因此所制复合粉体电阻率较大。而酒石酸加入量过多时,中间体金属络合物较为稳定,不易释放金属离子,沉淀反应受到阻碍,所得样品的电阻率也较大。酒石酸加入量一定,当尿素量较少时,酸效应减弱,金属与配体结合较为稳定,金属阳离子释放缓慢,沉淀反应诱导期较长,导致复合材料中包覆层ATO 粒径较大,外层导电网络连接性较差;当尿素量较多时,尿素水解释放的OH—浓度较高,沉淀反应较强,金属离子络合作用较弱,导致包覆层粒子团聚较为严重[13],复合粉体导电性也降低。综上分析可得,Sn-TA 及Sb-TA 络合物中金属阳离子Sn4+,Sb3+的释放难易程度与酒石酸-尿素体系pH 有关,H+溶度越高,酸效应越强;OH—溶度越高,沉淀反应越强,二者均不利于金属离子络合反应的发生,因此合适配比的沉淀剂与配合剂能很好地控制络合反应与沉淀反应达到相对平衡。当酒石酸与Sb 物质的量比为1:1,尿素与Sn 物质的量比为5:1时,所制复合粉体的电阻率最低,其平均值为6.85 Ω·cm。

图5 不同酒石酸及尿素用量下TiO2/ATO的电阻率Fig.5 Resistivity of TiO2/ATO at different addition amounts of tartaric acid and urea
2.4 复合材料反应机制
图6(a)所示为锡盐、锑盐和酒石酸的乙醇溶液(溶液1),锡盐和锑盐的乙醇溶液(溶液2)及酒石酸的乙醇溶液(溶液3)和酒石酸固体的FTIR图谱。从图6(a)可以看出:在3 620~3 200 cm-1处拓宽的吸收带为O—H的伸缩振动峰,乙醇或羧酸分子因氢键效应发生缔合作用,所以峰形较宽。1 655 cm-1处为O—H 的弯曲振动峰[14],对于溶液1 和3,C=O的伸缩振动峰也因氢键效应峰位向低波数方向移动,与δ(O—H)重合,而TA在1 736 cm-1处对应于ν(C=O)。图6(a)中谱线4 的3 477 cm-1和3 252 cm-1处分别对应酒石酸结晶水及其二聚体的O—H。在2 976~2 886 cm-1和1 452~1 385 cm-1处的吸收峰分别为溶剂乙醇—CH3和—CH2的伸缩振动重叠峰和变形振动重叠峰。在1 390 cm-1处的特征峰对应于Sn—O—C[15],与1 385 cm-1处的峰重合,所以溶液1和2此处峰稍强于溶液3。在1 087 cm-1和1 286 cm-1处分别为乙醇及酒石酸C—O 的伸缩振动峰,在1 046 cm-1处为C—O—H 的摇摆振动峰。溶液1~3 在879 cm-1处的特征峰均为ν(C—C)。在1 128 cm-1和890 cm-1处分别为酒石酸C—C的骨架振动峰及伸缩振动峰。
由图6(b)可知:2个前驱体样品在3 441 cm-1和1 643 cm-1处O—H 的特征峰明显比基体和煅烧后复合粉体的强,说明经包覆反应后,在核体TiO2外表面生成了Sn 或Sb 的水解沉淀物。在839~426 cm-1处为M—O (M=Ti,Sn,Sb)耦合的特征峰区[16],包括560 cm-1处出现ν(Sn—O)的伸缩振动峰[11],而前驱体经热处理得到TiO2/ATO,其对应的Sn—O 与Sb—O 峰显著增强,所以在此波数范围内表现为明显的宽峰。前驱体-1为没有加入TA所制得的样品,TiO2/ATO-1 为前驱体-1 煅烧后所得复合粉体,前驱体-2 和TiO2/ATO-2 分别为TA辅助作用下所得的前体及最终产品。对比前驱体-1 及前驱体-2 可以看出:前驱体-2 的FTIR 谱图中并未发现TA-Sn 和TA-Sb 络合物的特征峰,说明最终前躯体中沉淀物并不是以络合沉淀物形式存在。
利用酒石酸(TA)辅助均匀沉淀法包覆基体制得前驱体时,锡盐和锑盐是溶解于以乙醇为溶剂附加酒石酸的溶液中,其中锑离子最大配位数是6,且具有3 个空sp 轨道,可与乙醇羟基氧原子成键,羟基中的氢原子被解离,与三氯化锑电离的氯离子结合生成氯化氢气体,同样,锡离子也可与羟基氧原子成键,不同包覆溶液的pH 如表1 所示。由表1 可以看出:含有SnCl4·5H2O 和SnCl3的包覆溶液1和2的溶液pH更低,进一步验证说明HCl的生成,具体反应式如下:

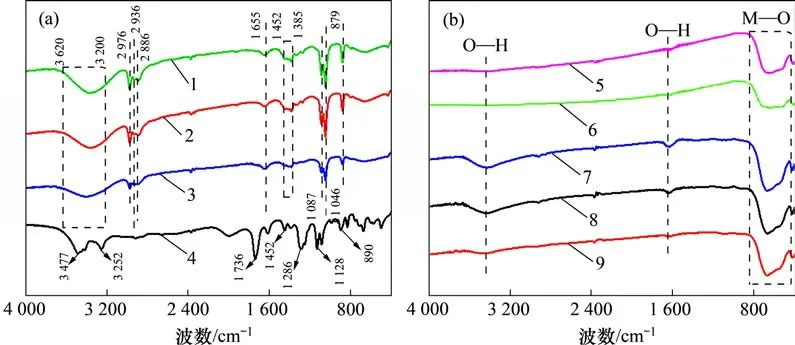
图6 不同包覆液和TiO2/ATO及其前驱体的FTIR图谱Fig.6 FTIR spectra of different coating solutions,TiO2/ATO and its precursor
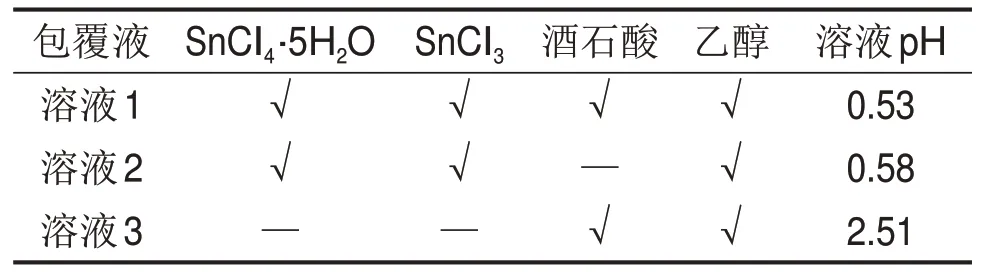
表1 不同包覆溶液的pHTable 1 pH of different coating solutions


酒石酸是一种常用的络合剂,其分子中有2个羧羟基氧和2个醇羟基氧,能与金属离子配位。酒石酸参与Sb3+络合解离、沉淀包覆反应过程示意图如图7所示。由图7可见:当包覆液滴入基体浆料水溶液中,部分Sb 以配阴离子[Sb2(C4H2O6)2]2-和[Sb(OH)(C4H2O6)]2-形式存在(以下分别以[Sb2L2]2-和[Sb(OH)L]2-表示),Sn 与酒石酸根(L4-)则形成了多核配合物[Snx(C4H2O6)y]4x-4y(以下以[SnxLy]4x-4y表示)[17],且配合反应与沉淀反应同时存在,互为竞争反应,其过程反应式如下:

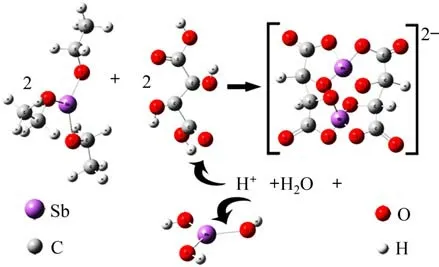
图7 酒石酸参与Sb(OH)3生成反应过程示意图Fig.7 Schematic diagram of TA participating in formation of Sb(OH)3 precipitate

经上述反应得到的前躯体再经煅烧,包覆层中的Sb(OH)3和Sn(OH)4分别脱水生成SnO2和Sb2O3,Sb2O3进一步被氧化为Sb2O5并固溶于SnO2晶格中,形成取代或填隙型固溶体[18-19],其主要反应式如下:
复合导电材料TiO2/ATO 复合材料的形成过程示意图如图8所示。

图8 TiO2/ATO复合材料的形成机制示意图Fig.8 Schematic diagram of formation mechanism of TiO2/ATO composite
3 结论
1)以氯化锑(Ⅲ)、氯化锡(Ⅳ)的乙醇溶液为包覆剂,尿素为沉淀剂,采用酒石酸辅助均匀沉淀法制得复合前驱体,再经550 ℃煅烧制备了TiO2/ATO(四方相)复合导电粉体。
2)酒石酸分别与Sb和Sn形成单核或多核配合物中间体,尿素水解缓释氢氧根进一步控制金属阳离子释放速度,使得沉淀包覆反应逐步进行,所得复合粉体外层ATO 包覆粒子粒径均匀,为12.3 nm。
3)在反应条件相同时,在酒石酸和尿素等原料合适的配比下,所制复合粉体具有较低的电阻率,为6.85 Ω·cm。

