木豆化学成分和药理活性研究进展
蔡佳仲,戴 湾,张嫩玲
1广州中医药大学科技创新中心,广州 510405;2广州中医药大学脾胃研究所,广州 510405;3贵州医科大学药学院,贵阳 550025
木豆(Pigeon pea,Cajanuscajan(L.) Millsp.)也叫树豆、三叶豆,为豆科(Leguminosae)木豆属(Cajanus)植物,我国主要分布于海南、云南、福建、台湾、广东、广西、四川等地。原产地或为印度,现热带和亚热带地区普遍有栽培[1,2]。木豆作为中药,始载于《陆川本草》和《泉州本草》。木豆具有清热解毒、补中益气、利水消肿、止血止痢、排痈肿等功效,民间常用于治疗血淋、痔血、痢疾等肠道疾病以及水肿、痈疽、脚气等疾患。而木豆叶也具有解毒消肿之功,可用于治疗小儿水痘以及痈疽肿毒等[2,3]。木豆作为一种药食两用植物,综合价值较高,在医药领域也具有良好的应用前景。其含有丰富的黄酮和茋类成分,在治疗骨质疏松和股骨头坏死、治疗高血糖和高血脂、神经损伤保护、心脑缺血损伤保护以及抗氧化、抗肿瘤等方面具有很好的药理活性。现将木豆化学成分和药理活性的研究进展进行综述,以便对其药用资源更好地进行开发和利用。
1 木豆化学成分研究
从上世纪七八十年代开始,国内外学者对木豆的活性成分进行了一系列的研究表明,其主要化学成分为黄酮(flavonoids)和茋类(stilbenes,二苯乙烯类)化合物,同时还含有香豆素、甾体、三萜类等其他成分。黄酮和茋类化合物被认为是木豆叶的主要活性成分。
1.1 黄酮类化学成分
迄今为止,木豆中已报道了分离鉴定的黄酮类化学成分有30多个(见表1和图1),主要包括黄酮类(flavones)(5个,1~5)[4,5]、异黄酮类(isoflavones)(14个,6~19)[6-12]、二氢异黄酮类(isoflavanones)(3个,20~22)[9,13,14]、二氢黄酮类(flavanones)(8个,23~30)[4,10,12,15-17]、黄酮醇类(flavonols)(3个,31~33)[18]和查尔酮类成分(chalcones)(2个,34和35)[19,20]。

表1 木豆中黄酮类成分
1.1.1 黄酮和异黄酮类成分
木豆叶中黄酮类和异黄酮类成分由于其广泛的生理活性而备受学者关注。1999年,Lin等[4]从对金黄色葡萄球菌具有较强抑制作用的木豆叶乙酸乙酯部位分离得到apigenin(1)、luteolin(2)、isovitexin(3)和vitexin(4)4个黄酮类化合物。Wu等[5]从木豆叶乙醇提取物中分离得到另一个黄酮类成分orientin(5)。
本课题组近年从木豆叶乙酸乙酯部位分离并鉴定出3个异黄酮成分,分别为genistin(6)、sissotrin(7)和ononin(8)[6]。早在1979年,Bhanumati等[7,8]就从木豆中分离得到两个新异黄酮类成分cajaisoflavone(9)和5,7,2′-trihydroxy isoflavone-7-O-β-D-glucoside(10),其中化合物(9)含有木豆化学成分普遍特有的异戊烯基。随后,Dahiya等[9]也从木豆中分离鉴定出两个新异黄酮类化合物11、12和一个已知异黄酮成分cajanin(13)。其中化合物11也含有异戊烯基结构,而化合物12则在黄酮母核6/7位上连接一个呋喃环。Duker-Eshun等[10]采用活性追踪法从木豆中得到3个具有抗疟活性的异黄酮类化合物2′-hydroxygenistein(14)、biochanin A(15)和genistein(16)并确定其结构。近年,Liu等[11]也从木豆叶中分离到异黄酮prunetin(17)和pratensein(18)。Neeraj等[12]也从木豆叶中分离到具有一定抑制TNF-α和IL-1β活性的异黄酮genistein-8-C-β-D-glucoside(19)。
1.1.2 二氢黄酮和二氢异黄酮类成分
从上世纪七十年代开始,就有学者陆续从木豆中发现一系列具有显著生物活性的二氢黄酮和二氢异黄酮类化合物。1977年,Preston等[13]从木豆根的甲醇提取物中分离鉴定了1个具有抗真菌活性的二氢异黄酮化合物cajanone(20)。随后,Dahiya等[9]也从木豆中得到1个二氢异黄酮类成分cajanol(21)。Bhanumati等[14,15]也从中分离得到1个二氢异黄酮2′-O-methylcajanone(22)和1个二氢黄酮cajaflavanone(23)并确定其结构。其他学者也相继从木豆中分离并鉴定了一系列二氢黄酮类化合物,包括naringenin-7,4′-dimethyl ether(24)[4]、pinostrobin(25)[10]、7,4′-dimethoxy flavanone(26)[12]和7-methyl glabranin(27)[12]等。本课题组近年也从木豆叶中分离并鉴定了3个二氢黄酮类成分,分别为naringenin-7-methyl ether(28)[16]、5,7-dihydroxy-8-prenylflavone(29)[16]和naringenin-3′-isoprenyl-7-methyl ether(30)[17],后两个化合物均连接异戊烯基。
1.1.3 其他黄酮类成分
Green等[18]基于核磁共振(NMR)和高效液相色谱(HPLC)技术从木豆荚甲醇提取物中分离得到3个黄酮醇类成分 quercetin(31)、quercetin-3-methyl ether(32)和quercitrin(33)。而Cooksey和Ajaiyeoba等[19,20]则分别从木豆中分离得到2个查尔酮pinostrobin chalcone(34)和cajachalcone(35),并确定其结构。
1.2 茋类化学成分
茋类化合物是木豆中的主要活性成分之一,也是木豆的特征性化合物。由于其独特的药效和生物学功能,近年成为国内外研究的热点。该类化合物具有二苯乙烯母核,木豆中的茋类化合物的取代基分布在A环,尚未见到B环有取代基的情况。取代基主要为异戊烯基、甲氧基和羟基。目前有报道的木豆中茋类及其衍生物将近30种(36~62,见表2和图2)。

表2 木豆中茋类成分
续表2(Continued Tab.2)
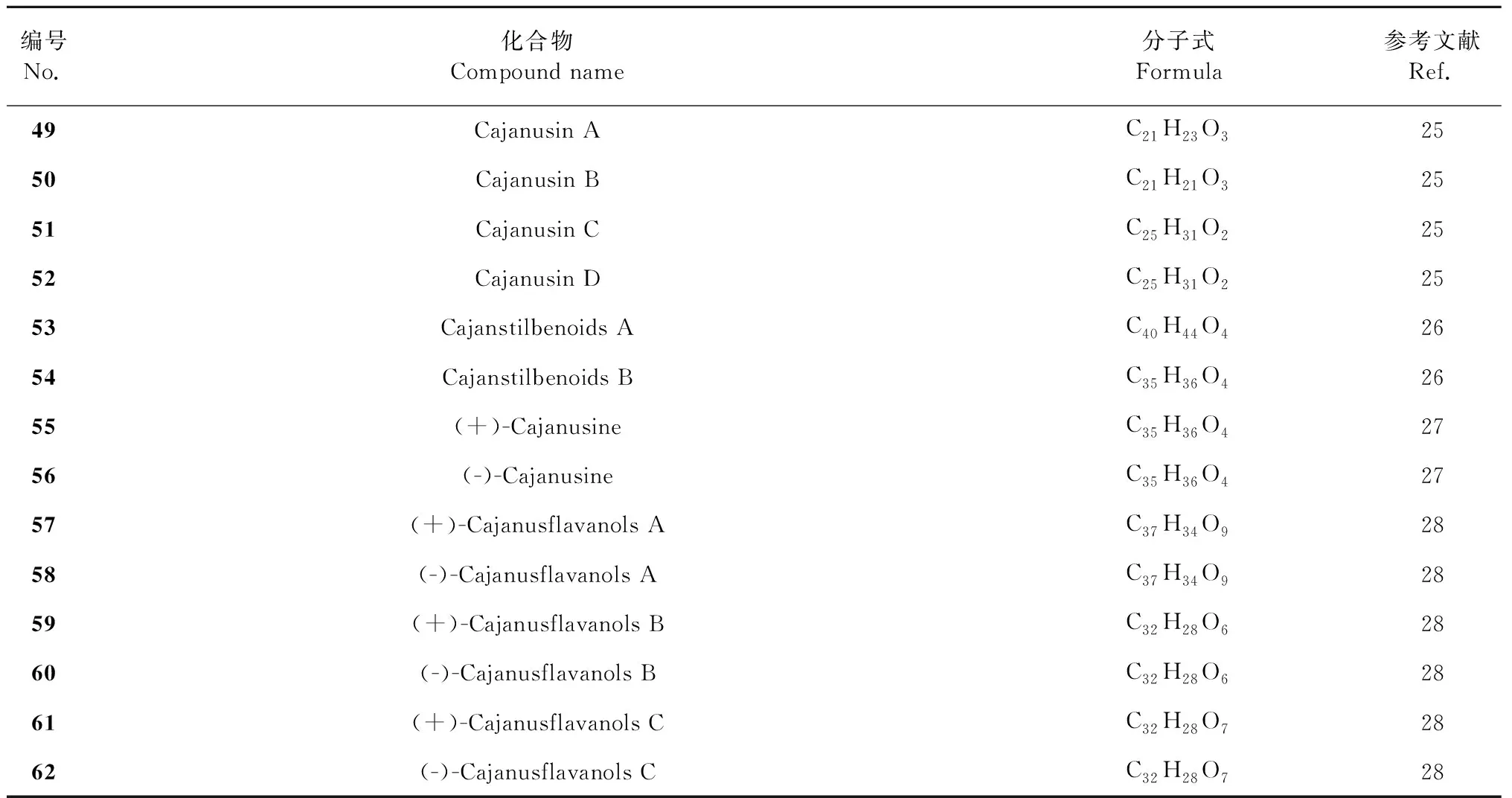
编号No.化合物Compound name分子式Formula参考文献Ref.49Cajanusin AC21H23O32550Cajanusin BC21H21O32551Cajanusin CC25H31O22552Cajanusin DC25H31O22553Cajanstilbenoids AC40H44O42654Cajanstilbenoids BC35H36O42655(+)-CajanusineC35H36O42756(-)-CajanusineC35H36O42757(+)-Cajanusflavanols A C37H34O92858(-)-Cajanusflavanols A C37H34O92859(+)-Cajanusflavanols B C32H28O62860(-)-Cajanusflavanols BC32H28O62861(+)-Cajanusflavanols C C32H28O72862(-)-Cajanusflavanols CC32H28O728
1982年,Cooksey等[19]从木豆叶甲醇提取物中发现了2个具有抗真菌活性的木豆茋酸类化合物6-hydroxy-4-methoxy-3-prenyl-2-styrylbenzoic acid(36)和cajaninstilbene acid(37),并确定其结构。天然茋酸在自然界较为少见,这些化合物多为植物防御素(phytoalexins)。随后中国医学科学院Chen等[21]从木豆叶乙醇提取物中分离得到了茋类成分longistylin A(38)和longistylin C(39)以及木豆茋酸(37)。本课题组也从木豆叶中分离得到3个新茋类化合物,分别命名为cajanstilbene H(40)[22]、cajanolactone A(41)[23]和木豆茋酸cajanonic acid A(42)[23]。其中(40)结构中具有(38)的5-羟基取代和1-氯代-2,3-丙二醇单元结构,并显示出促进骨髓间充质干细胞成骨分化的潜能。这种含有卤素的茋类成分在天然产物中并不多见,也是从木豆里面发现的第一个含卤素化合物。而(41)则在母核结构7、8位双键和芳环上的邻位羧基之间形成了内酯结构,也属于异香豆素成分。随后课题组又从木豆叶中分离得到另外2个新茋类化合物,分别命名为cajanotone(43)和cajanamide A(44),以及一系列的已知茋类及其类似物3-methoxy-2-(3-methylbut-2-enyl)-5-(2-phenylethyl)-phenol(45)、amorfrutin A(46)、pinosylvin monomethyl ether(47)[16]。其中,化合物44在母核结构7、8位双键和芳环上的邻位酰胺之间形成了内酰胺结构,而化合物45和46是茋类类似物,其母核结构7、8位双键发生氢化加成。He等[24]也从木豆叶中分离得到另一个木豆茋酸2-hydroxy-4-methoxy-6-(2-phenylcinyl)-benzoic acid(48)。Wu等[25]从木豆叶中分离得到3个新茋类及其类似物cajanusin A(49)、cajanusin B(50)、cajanusin C(51)和一个已知茋类cajanusin D(52),并确定其化学结构。化合物49母核结构7、8位双键也发生了氢化加成。
此外,国内学者也陆续报道了木豆叶中一系列结构新颖的茋类二聚物和黄酮茋类杂合化合物。本课题组从木豆叶中发现了两个新的的茋类二聚物cajanstilbenoids A(53)和cajanstilbenoids B(54)[26]。暨南大学Ye等[27,28]也从木豆叶中分离得到1对互为对映异构体并具有新化学骨架结构的茋类二聚物(+)-cajanusinehe(55)和(-)-cajanusine(56),并发现了3对互为对映异构体的黄酮茋类杂合化合物(+)-cajanusflavanols A(57)、(-)-cajanusflavanols A(58)、(+)-cajanusflavanols B(59)、(-)-cajanusflavanols B(60)、(+)-cajanusflavanols C(61)和(-)-cajanusflavanols C(62),并确定其化学结构。
1.3 其他成分
除了黄酮和茋类成分,木豆中还有许多三萜类化合物lupeol(63)[8]、α-amyrin(64)[8]、β-amyrin(65)[8]、betulinic acid(66)[10,12]等,甾体类化合物β-sitosterol(67)[4,21]、stigmasterol(68)[6]、β-daucosterol(69)[29]等,以及其他成分salicylic acid(70)[6]、catechol(71)[6]、uracil(72)[6]、p-hydroxybenzoic acid(73)[29]、n-docosane(74)[29]、stearic acid(75)[29]、laccerol(76)[21]等(化合物63~76,见图3)。

图2 木豆中茋类化合物结构Fig.2 The structure of stilbenes from C.cajan
2 药理活性
现代研究表明,木豆具有多种药理活性,包括治疗骨质疏松和股骨头坏死、治疗高血脂和糖尿病、神经损伤保护、心脑缺血损伤保护、抗氧化、抗肿瘤等。
2.1 治疗骨质疏松和股骨头坏死
骨质疏松是以成骨不足、骨量低、骨组织微环境退化和骨折可能性增加为特征的全身代谢性骨疾病,常见于老年人。骨质疏松性骨折也成为严重影响老年人健康的公共健康问题。而中医药在这方面应用历史悠久,前景广阔。
以木豆叶为主要成分的“通络生骨胶囊”(生脉成骨胶囊)是广州中医药大学第一附属医院袁浩教授结合多年临床实践联合企业研发的治疗股骨头坏死的有效中药制剂。其疗效在临床和实验均得到多次验证。Yuan等[30]通过600例股骨头坏死患者的多中心随机、双盲、双模拟和阳性药对照临床研究设计,证明了“通络生骨胶囊”在临床上能更好地改善患者的髋关节功能,促进股骨头坏死的修复,且安全可靠。而Liu等[31]也通过实验验证了“通络生骨胶囊”对大鼠应力缺失性骨质疏松模型的改善作用。结果表明,与模型组比较,通络生骨胶囊用药组的血清碱性磷酸酶含量、骨小梁面积、成骨细胞个数以及骨小梁个数显著升高,骨小梁厚度显著增加。提示了“通络生骨胶囊”具有促进骨生成作用,可用于应力缺失骨质疏松防治。

图3 木豆中其他成分化学结构Fig.3 The structure of other compounds from C.cajan
另有研究表明,木豆叶提取物在不提高血清雌二醇水平、不引起子宫内膜增生的情况下,能显著改善雌激素缺乏导致的骨丢失[32]。而木豆叶茋类提取物可抑制由雌激素缺乏或维甲酸导致的大鼠股骨头骨丢失,表现为明显增加大鼠骨小梁数量、骨小梁面积、改善骨小梁的结构等,与雌激素的作用接近[33,34]。这些研究表明,木豆叶抗雌激素缺乏或维甲酸导致的骨丢失作用可能是通过促进成骨细胞功能和抑制破骨细胞形成来实现的。茋类化合物是木豆叶治疗骨质疏松的主要活性成分之一。
基于此,本课题组也开展了木豆茋类单体成分抗骨质疏松的药理研究。结果发现cajanstilbene H(40)和cajanolactone A(41)在剂量和时间依赖条件下能够显著促进人骨髓间充质干细胞成骨分化[22,35]。机制研究表明,化合物41是通过激活Wnt/LRP5/β-catenin信号通路,增加细胞碱性磷酸酶活性和胞外钙沉积促进骨髓间充质干细胞成骨分化[35]。由此可见,木豆茋类成分具有潜力研发成抗骨质疏松的候选新药。
2.2 治疗高血脂和糖尿病
木豆提取物和单体成分在体内外均显示出显著的治疗高血脂和糖尿病活性。
Luo等[36]研究了木豆叶茋类提取物对高脂模型小鼠血脂和肝脏脂质的影响。结果显示,木豆茋类提取物可显著降低异常升高的血清和肝脏中总胆固醇和甘油三酯含量,并上调肝脏组织CYP7A1和LDL-R的基因表达水平,抑制肝脏脂质的蓄积,其作用可能与促进肝脏LDL-R表达和增加肝脏胆固醇向胆汁酸转化有关。另有研究报道,木豆提取物在体内能够通过促进高脂饮食诱导的肥胖仓鼠胆固醇转化为胆汁酸,从而发挥降血脂作用[37]。其甲醇提取物在体外能够通过下调HepG2细胞PCSK9基因表达,增加细胞中LDLR蛋白而起到调节脂质平衡和降胆固醇作用[38]。
本课题组邱声祥和沈小玲教授等[23]发现了木豆茋酸成分cajanonic acid A(42)在体内能显著降低db/db小鼠血糖和ob/ob小鼠血脂,其机制可能与抑制PPARγ和PTP1B活性,提高胰岛素信号通路敏感性相关,从而起到降糖减肥双重功效。随后,沈小玲教授团队进行了化合物42对脂质代谢和2型糖尿病的作用机制研究。实验结果表明,化合物42能明显降低诱导分化成熟的小鼠3T3-L1脂肪细胞总脂肪和甘油三酯含量,通过抑制脂肪吸收与合成相关基因表达,减少脂肪细胞甘油三酯的合成,抑制细胞过度肥大,减少游离脂肪酸的释放,从而起到改善脂肪细胞脂质代谢平衡作用[39]。同时,其能够通过恢复胰岛素抵抗、抑制脂肪细胞分化、调节体内外脂质平衡而治疗2型糖尿病[40]。
2.3 神经损伤保护
由于木豆在传统中医中可用于缓解疼痛而作为镇静剂,因此Nicholson等[41]进行了黄酮成分pinostrobin(25)对小鼠大脑中突触神经节去极化的抑制作用研究。结果表明,(25)作为电压门控钠离子通道抑制剂,能够抑制钠通道激活的小鼠大脑突触神经节去极化,降低神经细胞兴奋性,起到镇静缓解疼痛作用,其镇静作用优于卡马西平。同时,有学者报道[42],木豆叶水提物能抑制脑疼痛并增加抗氧化能力,对睡眠剥夺大鼠记忆损伤和记忆障碍具有保护作用。
Liu等[43-45]也通过实验证明了木豆叶醇提物在体外能够促进皮质酮诱导的PC12神经细胞增殖,逆转皮质酮对PC12细胞造成的损伤,而起到神经细胞损伤保护作用。该团队进一步揭示了木豆茋酸cajaninstilbene acid(37)保护皮质酮诱导的PC12神经细胞损伤的作用机制。其能够通过抑制线粒体凋亡通路、氧化和内质网应激介导的细胞凋亡,降低胞内钙离子浓度和caspase-3活性,防止皮质酮诱导的PC12细胞凋亡,从而起到保护皮质酮诱导的PC12神经细胞损伤作用。
以上研究结果表明木豆及其茋类活性成分对阿尔茨海默病认知缺失和记忆丧失可能有一定治疗效果。
2.4 心脑缺血损伤保护
木豆叶水提物对大、小鼠脑缺血缺氧损伤具有一定的保护作用。木豆叶水提物可显著降低急性脑缺血再灌注模型小鼠脑内MDA含量,提高SOD活力,显著减少急性脑缺血再灌注模型大鼠脑组织的含水量及脑指数。提示木豆叶水提物对脑缺血时脑组织中细胞膜及微血管膜的稳定性有一定的保护作用[46]。
木豆叶提取物对心肌缺血再灌注损伤大鼠也有保护作用。木豆叶提取物能够显著降低大鼠缺血性心律失常的严重程度和发生率,缩小心肌梗死范围,减轻心肌细胞肿胀和炎性细胞浸润,对抗心肌缺血-再灌注引起的大鼠心功能紊乱[47,48]。
这些作用对开发以木豆叶为主的复方防治心脑血管病新药具有重要意义。
2.5 抗氧化
Wu等[5,49]采用DPPH法测定了木豆叶醇提物和水提物的体外抗氧化活性。实验结果显示醇提物抗氧化活性优于水提物,而乙酸乙酯部分则显示出更优活性,其IC50值为194.98 μg /mL。与白藜芦醇相比,木豆茋酸成分(37)具有更强的抗氧化性能、DNA损伤保护活性和黄嘌呤氧化酶抑制活性。(37)对DNA氧化损伤具有良好的保护作用。Lai YS等[50]也通过实验发现木豆醇提物对过氧化氢和脂多糖处理的RAW264.7巨噬细胞具有显著的抗氧化和抗炎作用。木豆醇提物可防止巨噬细胞的抗氧化酶活性降低和脂质过氧化,抑制巨噬细胞中TNF-a、IL-1b和IL-6等炎症因子产生。
这些结果表明,木豆具有良好的抗氧化作用,可作为天然的氧化剂应用于食品、药品、保健品以及化妆品等领域。
2.6 抗肿瘤
木豆活性成分对多种肿瘤细胞的生长具有明显抑制作用。课题组测试了4个新茋类成分cajanotone(43)[16]、cajanamide A(44)[16]、cajanstilbenoid A(53)[26]和cajanstilbenoid B(54)[26]对人肝癌细胞HepG2、乳腺癌细胞MCF-7、人肺癌细胞A549的细胞毒作用。实验结果表明,(53)对上述3种肿瘤细胞的抑制活性明显强于其他3个化合物,其半数抑制浓度IC50为2.14~2.56 μM之间。Luo等[51]也报道了黄酮类成分cajanol(21)在体外对人乳腺癌细胞MCF-7的细胞毒机制。化合物21在24、48和72 h的半数抑制浓度IC50分别为83.42、58.32和54.05 μM,其机制可能是通过细胞周期阻滞和ROS介导的线粒体依赖信号通路诱导肿瘤细胞凋亡。随后,Liang等[52]也研究发现(21)可通过干扰雌激素受体相关的PI3K信号通路抑制人前列腺癌PC-3细胞增殖。Fu等[53]揭示了木豆茋酸成分(37)抗乳腺癌增殖机制,可能与其影响肿瘤细胞DNA损伤反应和引起细胞周期阻滞和凋亡相关。
2.7 其它作用
此外,其他研究表明,木豆提取物及其活性成分还具有抗疟[10,20]、抗菌[13]、抗病毒[54]、松弛血管平滑肌[55]等药理活性。
3 结语
中药木豆始载于《陆川本草》和《泉州本草》,因其清热解毒、补中益气、利水消肿、止血止痢、排痈肿之功,民间常用于治疗血淋、痔血、痢疾以及水肿、痈疽、脚气等疾病,具有较高的药用价值[2,3]。我国木豆资源丰富,作为药食两用的植物,一方面富含黄酮和茋类等活性物质;另一方面具有治疗骨质疏松和股骨头坏死、治疗高血糖高血脂、神经损伤保护、心脑缺血损伤保护、抗氧化、抗肿瘤等药理活性,有很高的医药价值。迄今为止,国内外学者对木豆进行了大量的化学研究,分离到的黄酮和茋类化合物有六十多个,并进行了多种药理作用和临床制剂研究。广州中医药大学袁浩教授结合多年临床实践联合企业开发了以木豆叶为主要成分的“通络生骨胶囊”(生脉成骨胶囊),在治疗股骨头坏死方面疗效显著,广泛应用于临床。虽然木豆在骨科医学具有较大的的应用前景,然而目前对其研究还有诸多不足,缺乏中医药的系统性和整体观,缺乏药效物质群之间作用机制的系统研究。近年网络药理学已成为中药药理机制研究的热点。通过整合木豆化学成分和生物数据库,结合生物信息学、化合物-蛋白靶点“钩钓技术”、分子对接和构效关系等技术,构建“木豆活性成分-蛋白靶点-疾病网络”的预测模型,从“整体观”系统分析木豆在中医骨科及其他药理的作用靶点和网络机制,并通过体内外实验验证木豆成分结构与活性之间、活性与疾病之间的相关性,系统阐明其中医药作用机制和物质基础。
中药木豆中蕴藏着巨大的新药创制资源。然而,目前对于木豆民间传统应用于血淋、痔血、痢疾等消化道疾病的现代药理研究仍少见报道。因此,作者预测,关于木豆的消化药理应用可能是今后该中药资源研发的一个重要方向。综上,当前木豆的药用开发仍需大量的基础研究,但其药用开发前景十分广阔。

