水泥熟料若干参数的方程式推导
黄宁康
(广西理工职业技术学校, 广西 南宁 530031)
水泥生产中的熟料煅烧是整个生产工艺过程中最重要的环节,其中用于生产控制的计算参数很重要。在以往的有关文献资料中,对这些参数的推导桀骜难懂,要让人透彻地理解,实在是勉为其难。为此,笔者根据人们普遍都掌握的求解化学方程式的方法,推导出各个参数,使读者看得懂、记得住。
1 石灰饱和系数(KH)的推导
1.1 石灰极限含量
按古特门与杰耳的观点,水泥熟料中酸性氧化物(即Fe2O3、Al2O3、SiO2)形成碱性最高的矿物为铁铝酸四钙(C4AF)、铝酸三钙(C3A)、硅酸三钙(C3S)。为方便计算,我们将C4AF 表示为“CF”和“C3A”,熟料中石灰(即氧化钙CaO)极限含量可据此计算。
首先计算生成C3S 所需氧化钙(CaO)。如熟料中二氧化硅含量已知,以SiO2(%)表示,设需要的氧化钙为x,列化学方程式:
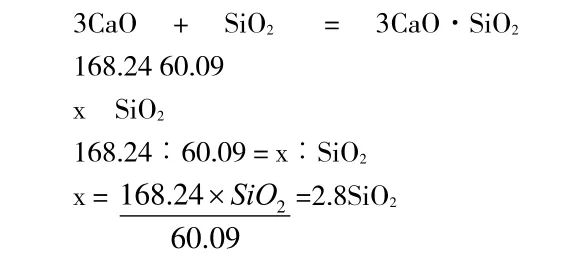
然后计算生成C3A、“CF”矿物所需氧化钙。如熟料中三氧化二铝、三氧化二铁含量已知,分别以Al2O3(%)、Fe2O3(%)表示,设需要的氧化钙为y、z,分别列化学方程式:

所以熟料中石灰极限含量为:CaO=2.8SiO2+1.65Al2O3+0.35Fe2O3。
1.2 石灰饱和系数KH 的导出
前苏联学者金得和龙克由上式即石灰极限含量提出KH(石灰饱和系数)这个率值。他们认为水泥熟料各矿物形成的过程中,CaO 始终饱和Fe2O3和Al2O3,即反应完全,但SiO2就不同,为避免出现ƒ_cao,熟料中应该有C2S 存在,也就是说,水泥熟料中应该有四个矿物成分。因此SiO2应该稍为过量,使之呈“吃不饱”状态,所以在上式中的2.8SiO2前应有一个小于1 的系数,以KH 表示,即CaO=KH·2.8SiO2+1.65Al2O3+0.35Fe2O3,所以
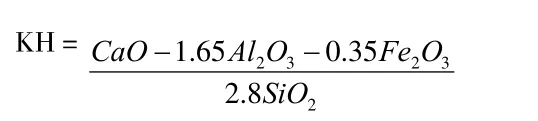
2 熟料矿物组成计算式的推导
2.1 碱度N 的引入
1 摩尔SiO2所能结合的CaO 的摩尔数叫碱度。水泥工业熟料的主要矿物为C3S、C2S、C3A、C4AF,生成这些矿物成分所需氧化钙为CaO-1.65Al2O3-0.35Fe2O3,相应的摩尔数表示为Mc=(CaO-1.65Al2O3-0.35Fe2O3)/56.08,相应的二氧化硅的含量以SiO2表示,其摩尔数为Ms=SiO2/60.09,所以熟料的碱度为

2.2 熟料中分别用于生成C3S、C2S 的SiO2 的百分比
用来形成C3S、C2S 的碱度(设为N1、N2),对应的生成C3S、C2S 所需CaO的摩尔数分别为C1、C2,列化学方程式:
3CaO + SiO2= 3CaO·SiO2
3 1
C1N1
3∶1=C1∶N1
C1=3N1
2CaO + SiO2= 2CaO·SiO2
2 1
C2N2
2∶1=C2∶N2
C2=2N2
解方程,得 N1=3KH-2,
N2=3(1-KH)。
说明:N1、N2其实就是熟料中分别用于生成C3S、C2S 的SiO2的百分比。
2.3 熟料中C3S、C2S 含量计算
以SiO2(%)表示已知的熟料中二氧化硅含量,按照上述说明,则其中(3KH-2)SiO2用于生成硅酸三钙,3(1-KH)SiO2用于生成硅酸二钙,生成的量分别以C3S、C2S 表示,列化学方程式:
3CaO + SiO2= 3CaO·SiO2
60.09 228.33
(3KH-2)SiO2C3S
60.09 ∶228.33=(3KH-2)SiO2∶C3S
2CaO + SiO2= 2CaO·SiO2
60.09 172.25
3(1-KH)SiO2C2S
60.09 ∶172.25=3(1-KH)SiO2∶C2S
解得C3S=3.8(3KH-2)SiO2
C2S=8.61(1-KH)SiO2
2.4 C3A、C4AF 含量计算
当熟料中三氧化二铝、三氧化二铁含量已知,分别以Al2O3(%)、Fe2O3(%)表示,同理可用解化学方程式的方法分别得出熟料中C3A、C4AF 含量的计算式:
C3A=3.04 Al2O3
C4AF=2.65(Al2O3-0.64 Fe2O3)
3 熟料烧成中高温液相量的计算
在熟料中三氧化二铝、三氧化二铁含量已知的情况下,也都可由化学方程式解出当IM>1.38 及IM<1.38 时的高温液相量,在此不再赘述。

