心率变异性的降低对难治性高血压患者夜间血压下降幅度减弱的影响
方子美,周明敏
在高血压和正常血压人群中,夜间血压下降幅度减弱(即非杓型高血压)被证实为独立的心血管危险因素[1]。然而,其生理病理机制尚不清楚。已有研究表明,夜间血压的正常下降不仅仅是由于睡眠固有的生理活动不足造成的被动现象,而是压力感受器阈值降低和交感神经系统活动减少的主动反馈[2,3]。另一方面,不论是在时域还是在频域上,心率变异性(HRV)是评估自主神经系统功能的最有价值的非侵入性方法[4]。HRV降低通常表明迷走神经-交感神经失调,交感神经过度活动或迷走神经紧张减少或两者兼而有之[5]。HRV的降低不仅在冠心病和心力衰竭的患者中,而且在糖尿病、高血压患者和老年人群中也是不良心血管预后的预测因子[6-8]。此外,HRV降低的血压正常者有更高的高血压发病风险,而对于HRV降低的高血压人群,则有更高的几率出现非杓型血压[9]。难治性高血压患者中非杓型血压的比例较高,这种血压昼夜节律在难治性高血压患者中是独立于其他心血管危险因素和平均24 h血压水平的心血管风险预测因子[10]。然而,据我们所知,在难治性高血压患者中,HRV参数与夜间血压下降之间的关系尚未被评估。此外,最近调查显示,难治性高血压患者阻塞性睡眠呼吸暂停综合征(OSAS)的患病率非常高,这可能会影响夜间的血压下降[11]。因此,本研究的目的是评价HRV降低与难治性高血压患者不同血压昼夜节律之间的关系,并观察了OSAS的存在对此关系的潜在影响。
1 资料与方法
1.1 研究对象这是一项横断面研究, 2016年3月至2017年12月共212例难治性高血压患者纳入研究。排除标准: ①继发性高血压患者;②近期家庭或身边发生重大事件而失眠者;③合并其他系统严重疾病者。所有参加者都给予书面知情同意,并通过黄石市中心医院伦理委员会批准。所有高血压患者均符合难治性高血压定义[11],即应用了足量且合理联合的3种降压药物(包括利尿剂)后,血压仍然在目标水平(140/90 mmHg,1 mmHg=0.133kPa)之上,或至少需要4种降压药物才能使血压达标。
1.2 方法所有患者均进行了全面的临床检查(特别注重了对心血管危险因素和靶器官损害的评估),包括:实验室检查、2D超声心动图、24 h动态血压监测(ABPM),24 h动态心电图监测(Holter)和颈动脉-股动脉脉搏波速度(PWV)测量。其中,110例(52%)进行了多导睡眠描记。血脂异常定义为总胆固醇(TC)>6.22 mmol/L,高密度脂蛋白胆固醇(HDL-C)<1.04 mmol/L,三酰甘油(TG)>2.26 mmol/L[8]。心血管疾病定义为诊断冠心病、心力衰竭、脑血管疾病或外周动脉疾病。实验室检查包括空腹血糖、血清肌酐、血脂(TC、HDL-C、TG)以及24 h尿白蛋白。超声心动图评估左心室质量(LVM)和左室质量指数(LVMI),计算公式为:LVM(g)=0.8×1.04×[(左室舒张末内径+室间隔厚度+后壁厚度)3-左室舒张末内径3];LVMI(g/m2)=LVM/(0.0061×身高+0.0128×体重-0.1529)[2]。左心室肥大定义为男性LVMI>125 g/m2,女性LVMI>110 g/m2[2]。颈动脉-股动脉(主动脉)PWV是在ABPM或Holter检查后的清晨进行测量。
1.2.1 动态血压监测使用动态血压记录分析系统Mobil-O-Graph NG(德国Mobil公司)进行ABPM检查。所有患者在进行ABPM期间均使用抗高血压药物。ABPM检查的模式为:日间每15 min测量一次血压,夜间每30 min测量一次血压。评估的参数为24 h平均收缩压(SBP)、24 h平均舒张压(DBP)、日间SBP、日间DBP、夜间SBP及夜间DBP。夜间血压降低被表示为昼夜血压比率(连续变量)。所有研究对象均按照昼夜血压比率进行二分类:非杓型(昼夜血压比率> 0.9)、杓型(昼夜血压比率≤0.9)。
1.2.2 动态心电图监测采用24 h动态心电图监测仪(DMS300-4A,美国迪姆公司)进行Holter检查。计算患者的四个时域的HRV参数,分别为:所有正常RR间期的标准差(SDNN,单位为ms),5 min节段平均正常RR间期标准差(SDANN,ms),连续正常R-R间期差值的均方根(RMSSD,ms)与相邻R-R间期大于50 ms的百分比(PNN50)。
1.2.3 多导睡眠描记随机抽取110例患者,使用SW-SM2000CB多导睡眠分析诊断系统(美国凯迪泰公司)进行夜间标准多导睡眠图检查。由经验丰富的医生评估多导睡眠图,并计算呼吸暂停低通气指数(AHI),该指数表示每小时睡眠中呼吸暂停或低通气事件的次数,并对OSAS严重程度进行相应的分级:无OSAS(AHI≤5)、轻度OSAS(AHI 6~15)、中度OSAS(AHI 16-30)和重度OSAS(AHI>30)。
1.3 数据处理正态分布的连续性变量描述为均值±标准差,非正态分布的连续性变量则描述为中位数(四分位数区间)。使用非配对t检验(正态分布变量)、Mann-Whitney检验(非正态分布变量)和χ2检验(分类变量)对非杓型血压和杓型血压的患者进行基线特征比较。通过多元线性回归(以夜间-白天SBP比值和夜间-白天DBP比值为因变量)和多元Logistic回归(以非杓型SBP和DBP为因变量)评估不同夜间血压下降模式与HRV参数之间的独立相关性。两个多变量分析都针对以下协变量进行调整:年龄、性别、体质指数(BMI)、24 h平均动态血压、左心室质量指数、血清肌酐和白蛋白尿、使用抗高血压药物的数量、β受体阻滞剂的使用、糖尿病病史和心血管疾病病史。所有统计均采用SPSS 19.0,P<0.05被认为具有统计学差异。

表1 所有患者的基线特征
2 结果
2.1 基本特征表1描述了所有患者的基本特征。与杓型血压患者比较,非杓型血压患者年龄更大,血清肌酐水平更高,亚临床靶器官损害(左心室肥厚和主动脉僵硬度增加)和心血管疾病的发生率更高。非杓型患者的夜间血压高于杓型患者,而白天血压低于杓型患者。在110例进行多导睡眠描记术的患者中有91例(82.7%)患者患有OSAS。非杓型患者的AHI和严重OSAS(AHI>30)的患病率显著高于杓型患者。在HRV参数方面,非杓型患者比杓型患者有较低的SDANN。非杓型血压患者和杓型血压患者的抗高血压治疗的药物数量和种类,以及诊室和24 h平均动态血压间均无统计学差异。表2描述了不同OSAS严重程度患者的HRV参数,结果显示HRV参数与OSAS的严重程度均无显著关系。
2.2 多变量分析在多变量分析中,表3为多元线性回归分析,表4为Logistic回归分析,结果显示在调整潜在的混杂因素后,SDNN(P=0.007、0.004)、SDANN(P=0.008、0.003)均与夜间血压下降独立负向相关。SDNN的降低(<70 ms)(P=0.027、0.013)和SDANN的降低(<50 ms)(P=0.006、0.010)可作为非杓型的独立危险因素。
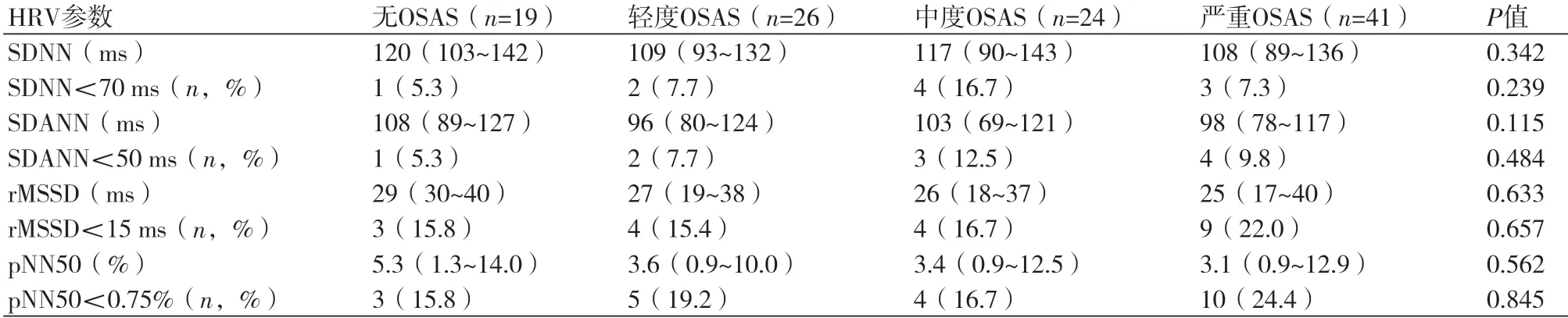
表2 不同OSAS严重程度分级的心率变异性参数
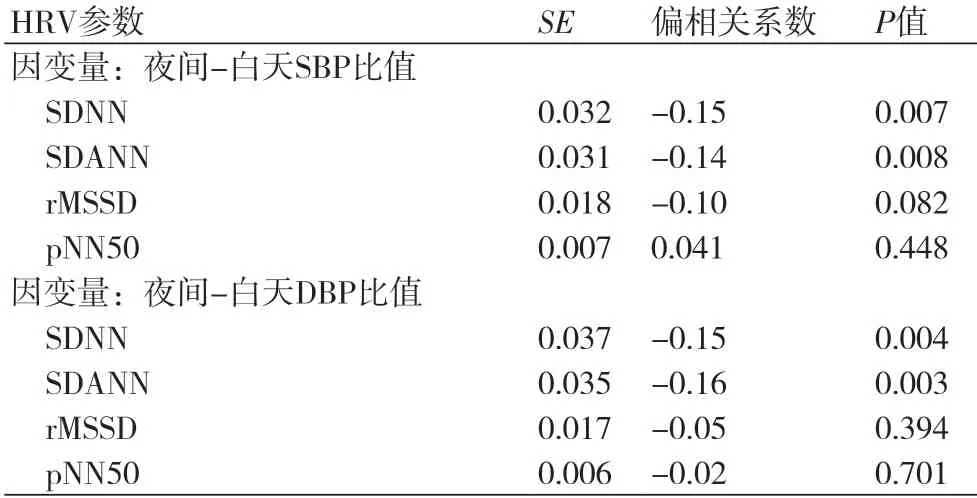
表3 昼夜血压比与心率变异性参数之间独立关系的多元线性回归分析

表4 非杓型与心率变异性参数独立关联的多元Logistic回归分析
3 讨论
这项针对难治性高血压患者的横断面研究有两个主要发现。首先,两个主要反映交感神经过度活动的HRV参数(SDNN和SDANN)的降低与夜间血压下降幅度减弱独立负向相关。其次,虽然OSAS与非杓型血压相关,但是其存在及其严重程度不会影响HRV降低与夜间血压下降之间的关系。这些观察结果提供了对昼夜血压节律的生理机制以及异常变异模式和心血管疾病风险之间病理联系的潜在见解。
目前,通过对最常用的HRV[9]、最不敏感的血清或尿去甲肾上腺素水平[12]以及最敏感的肌肉交感神经活性[13]进行评估时均发现,不管交感神经系统张力是否减弱,高血压患者夜间血压下降幅度减弱时交感神经活动增强。然而,大多数以前的报告并没有评估难治性高血压患者。因此,本研究将目前的研究扩展到这个重要但并未充分研究且具有非常高的心血管风险特征的高血压亚组[14]。结果显示,非杓型患者中SDNN<70 ms(13.5%vs. 5.1%)和SDANN<50 ms(14.3%vs.3.8%)的人数明显多于杓型患者。之前已有研究证明,非杓型患者较杓型患者具有更高的心血管发病率和死亡率风险[15]。这表明交感神经活动的增加部分解释了与异常昼夜血压变异模式相关的过度心血管风险。然而,研究对这个结论应该比较谨慎,因为HRV参数是反应交感神经活动的替代测量指标,而不是其直接测量指标。
尽管非杓型患者的OSAS患病率,特别是严重OSAS患病率高于杓型患者,但HRV参数与OSAS的存在或严重程度之间没有关系,OSAS既不影响也不混淆HRV降低与血压昼夜节律异常之间的关系。OSAS会增加睡眠期间的交感神经活动,因为每次呼吸暂停-呼吸不足发作时都会出现由低氧血症和高碳酸血症引起的化学感受性激素反射[16]。我们推测,由于高血压持续时间长,较高的血压水平和靶器官损害发生率,难治性高血压患者可能大大增加了交感神经系统活性,而OSAS的存在不能进一步增加交感神经系统活性。最近的一项研究[17]表明,OSAS对临床和动态血压水平影响不大,包括夜间血压,这在一定程度上支持了本研究假设。
据我们所知,研究首次探讨了HRV的降低对难治性高血压患者夜间血压下降幅度减弱的影响,为将血压变异性与心血管结果联系起来的病理生理学机制提供了见解。这项研究存在一些值得讨论的局限性。①鉴于研究是横断面设计,我们不能得出关于交感神经过度活动(HRV降低)和夜间血压下降幅度减弱之间的因果关系的结论。②如前所述,HRV参数是自主神经系统的替代测量指标,并且可能与肌肉交感神经活动的直接测量不相关[18]。③研究没有对所有难治性高血压患者进行多导睡眠描记术,而是随机抽取52%的患者。④目前关于杓型状态的定义有不同标准,且其发生机制仍不清楚。⑤本研究结果不能推广到轻度高血压患者。
总之,本研究提供的证据表明,与杓型难治性高血压患者相比,非杓型患者的HRV参数(SDNN和SDANN)降低,这主要反映了交感神经系统活动过度增强。此外,这种关联独立于已知的与非杓型状态相关的几个因素[9],例如年龄、肥胖、糖尿病等,尤其是与OSAS的存在无关。这些关系可以提供关于将血压变异性与心血管结果联系起来的病理生理学机制的见解。未来的前瞻性研究应该探讨交感神经过度活动是否是一种独立于夜间杓型状态的心血管风险指标。

