多排螺旋CT灌注成像联合图像三维重建技术定性诊断孤立性肺结节的价值▲
梁海胜 纪 律
(上海交通大学医学院附属第九人民医院放射科,上海市 201999,电子邮箱:lycghxb@163.com)
孤立性肺结节是早期转移瘤或周围型肺癌的表现形式,指在肺部单发、球形、边界清楚、直径≤3 cm,周围完全由充气的肺组织包绕,不伴肺不张、肺门淋巴结肿大和胸腔积液的病变[1]。早期诊断孤立性肺结节并判断其良恶性,对后续临床治疗方案的选择以及改善患者的预后具有重要意义,但其良恶性的鉴别一直是困扰临床医生的难题,目前国内尚无统一的鉴别标准[2-3]。多排螺旋CT参数如增强峰值、血容量和表面通透性均能反映恶性组织的病变情况,但单靠一种征象难以判断结节的良恶性[4]。随着计算机技术的发展,计算机辅助诊断技术尤其是图像三维重建技术的开发和应用,提高了孤立性肺结节的诊断准确性,但仍存在一定局限性[5]。本研究比较多排螺旋CT灌注成像、图像三维重建技术以两者联合定性诊断孤立性肺结节的效能,旨在为提高孤立性肺结节的诊断准确性提供参考。
1 资料与方法
1.1 临床资料 选择2015年1月至2017年1月我院收治的100例孤立性肺结节患者作为研究对象,其中男性68例,女性32例,年龄56~73(62.65±7.28)岁。纳入标准:(1)均经胸部X线片或CT证实存在孤立性肺结节,并经病理检查确诊;(2)患者的临床病历资料完整;(3)患者未经放化疗治疗;(4)患者了解本研究流程。排除标准:(1)严重心脑肝肾等器质性病变者;(2)无法进行影像学检查者;(3)对本研究相关药物过敏者;(4)依从性差,无法完成随访者。本研究经医院伦理委员会审查通过,所有患者均对本研究知情同意,自愿参加。
1.2 方法
1.2.1 多排螺旋CT灌注成像:(1)扫描方法。扫描仪器为飞利浦 Brilliance 128排256层iCT,管电压和电流分别设置为120 kV和150 mA。首先对胸部进行平扫,待明确结节的具体位置后,选择灌注范围为5 mm×8层,灌注范围应覆盖整个结节。采用非离子造影剂碘海醇作为对比剂(浓度为320 mg/mL),并用高压注射器经右前臂静脉埋置的套管针注入对比剂(速度为3.0 mL/s)。5 s后,在患者屏气最大时进行扫描,前期扫描维持30 s,暂停5 s,后期扫描20 s。(2)图像处理。采用飞利浦工作站对图像进行后处理,首先设定空气及骨的CT值范围,输入动脉选择与结节同一层面的大血管,在孤立性肺结节最大横截面处选择感兴趣区,同时避开灶内钙化、空洞,以及灶周围的临近血管,最后计算病变部位的增强峰值、血容量、表面通透性和灌注峰值时间。
1.2.2 图像三维重建:(1)扫描方法同多排螺旋CT灌注成像。(2)三维重建技术及图像处理。在飞利浦工作站内进行容积再现、多平面重建、最大密度投影、最小密度投影和表面遮盖显示。通过调整以上参数和位置,多角度反复观察孤立性肺结节的形态、边界特点及其与血管、胸膜的关系。调整对比度和亮度,获得图像的最佳观察视角。将所得图像传输至影像归档和通信系统,由两名经验丰富的放射科副主任医师按照双盲的原则进行阅片,判断并记录有无分叶征和血管集束征。
1.2.3 诊断标准:将随访结果和病理检查结果作为孤立性肺结节的临床诊断标准(金标准),其中良性结节25例,恶性结节75例。多排螺旋CT灌注成像中,如每分钟血容量≥5 mL/100 g或每分钟表面通透性≥20 mL/100 g或增强峰值>20 HU,则诊断为孤立性肺结节;三维重建图像以存在分叶征和血管集束征为诊断征象,具备其中1项,则诊断为孤立性肺结节。由两名具有多年阅片经验的副主任医师做出诊断(Kappa检验值大于0.85),如出现意见不一致时共同讨论得出结果。
1.3 统计学分析 采用SPSS 19.0软件进行统计分析。计数资料以例数和率表示,比较采用χ2检验;计量资料以(x±s)表示,比较采用t检验或t′检验。采用非条件多因素Logistic回归模型分析孤立性肺结节与CT参数之间的相关性。采用受试者工作特征(receiver operating characteristic,ROC)曲线分析增强峰值、血容量、表面通透性、分叶征、血管集束征以及所有指标联合诊断孤立性肺结节良恶性的价值,采用z检验比较ROC曲线下面积。以P<0.05为差异有统计学意义。
2 结 果
2.1 良恶性孤立性肺结节的螺旋CT参数比较 良性孤立性肺结节的增强峰值、血容量、表面通透性均低于恶性孤立性肺结节,灌注峰值时间长于恶性孤立性肺结节患者(均P<0.05),见表1。

表1 良恶性孤立性肺结节的螺旋CT参数比较(x±s)
2.2 螺旋CT参数和三维重建图像特征与良恶性孤立性肺结节的相关性 以孤立性肺结节的良恶性情况作为因变量,以螺旋CT参数增强峰值、血容量、表面通透性、灌注峰值时间,以及三维重建图像特征分叶征和血管集束征作为自变量,纳入非条件多因素Logistic回归模型中进行分析,变量赋值情况见表2。结果显示,增强峰值、血容量、表面通透性、分叶征、血管集束征均与恶性孤立性肺结节相关(均P<0.05),见表3。

表2 变量赋值情况
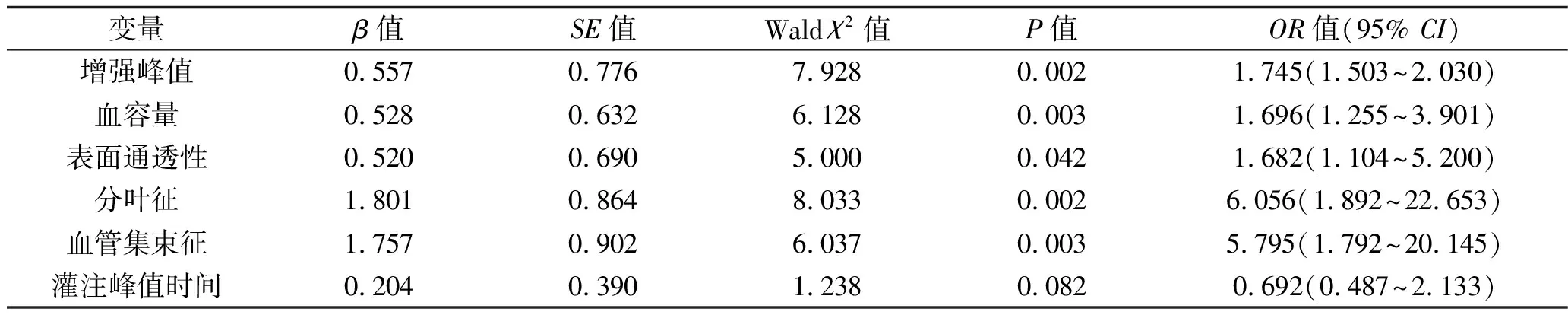
表3 良恶性孤立性肺结节与螺旋CT参数的相关性
2.3 多排螺旋CT灌注成像各参数、三维重建技术各参数及其联合诊断恶性孤立性肺结节的效能 增强峰值、血容量、表面通透性、分叶征、血管集束征五者联合诊断恶性孤立性肺结节的敏感性、特异性和准确率分别为97.4%、91.3%、96.0%,均高于单一指标。ROC分析结果显示,各指标联合诊断恶性孤立性肺结节的曲线下面积最大。见表4~5及图1。

表4 各个指标诊断良恶性孤立性肺结节结果(n)

表5 各指标诊断恶性孤立性肺结节的诊断效能

图1 各指标单独或联合诊断恶性孤立性肺结节的ROC曲线
3 讨 论
孤立性肺结节是圆形或近似圆形的病灶,由于其体积较小,且影像特征缺乏特异性,导致难以定性诊断,容易延误治疗,严重影响患者的预后,因而早期诊断至关重要[6]。CT灌注成像的原理是通过静脉注射造影剂来实现CT增强,随后进行连续动态扫描以观察微血管的分布和血流灌注,从而对组织状况进行判断[7]。CT检查可通过横断面成像显示患者大气道结构,多层螺旋CT灌注成像具有图像质量稳定、清晰度高、分辨率高、信噪比低等特点,能够弥补常规CT无法应用于层厚大、扫描速度提升难的弊端。但是CT轴位扫描只能通过计算层厚和层数得出孤立性肺结节的高度,无法显示周围血管,因而无法对孤立性肺结节的形态及其与周围血管的关系进行判断[8]。图像三维重建技术可将传统的二维图像转化为三维立体形态学,能够更清晰地显示肺结节的形态,为临床诊断提供更多依据,但该方法常需结合其他方法使用,以显示病变结构的细微变化,具有一定的局限性。
血容量是指某一区域各血管中血液体积的总和,用于反映血液灌注流量,受血管直径和毛细血管数量影响较大[9]。增强峰值为选择区域在灌注时间内所计算出的面积,反映的是扫描时间内感兴趣区CT值变化范围的面积,与局部病变恶化程度和微血管的数量相关[10]。表面通透性可以用来反映局部微血管内皮细胞的完整性和细胞壁的通透性。灌注峰值时间可反映造影剂在局部的扩散速度,与靶组织的血管结构相关[11]。本研究结果显示,良性孤立性肺结节的增强峰值、血容量、表面通透性均低于恶性结节,灌注峰值时间大于恶性结节(均P<0.05)。分析其原因可能为:肺组织恶性病变部位能够引起支气管动脉弯曲、支气管和微血管数量增加,因此通透性增加,故恶性组织增强峰值、血容量、表面通透性较高。理论上,良恶性组织的灌注峰值时间应该有差异,但本研究多因素分析结果显示,灌注峰值时间与孤立性肺结节的良恶性无相关性,可能是因为灌注峰值时间也与心排血量和循环相关,而本研究未考虑不同患者之间心排血量和循环功能的差异,因此该结论仍需进一步研究探讨。此外ROC曲线分析显示,多排螺旋CT参数增强峰值、血管容量、表面通透性在良恶性孤立性肺结节的鉴别诊断中均有一定的价值。
分叶征指因恶性病变组织向外周的增生速度不一而导致的多个弧形拱起。血管集束征是一支或多支到达肿块内部或肿块边缘的血管,在三维图上显示为多支血管集中于恶性病变组织[12]。本研究ROC曲线分析结果显示,分叶征和血管集束征对恶性孤立性肺结节均有一定的诊断价值。而相比于单个检测方法,多排螺旋CT灌注成像参数联合图像三维重建参数诊断恶性孤立性肺结节的曲线下面积、灵敏度、特异性和准确性均最大。一方面,多排螺旋CT通过扩大实际扫描范围能够有效地减轻容积效应,减少层漏的发生,通过扫描可提高纵轴分辨率,清晰地分辨结节病灶与肺部支气管[13]。另一方面,三维重建技术可以进行多角度、多层面的立体观察,其中容积再现可实现三维空间关系,进而充分地显示孤立性肺结节的形态学特征;多平面重建可通过任意角度全面反映孤立性肺结节的征象及其与周围组织的相关性;最大密度投影可以完整地展示局部恶变组织供血血管走向;最小密度投影则能更好地显示支气管形态及气道内情况[14-16]。因此,多排螺旋CT灌注成像联合图像三维重建技术能够更灵敏、特异、准确地分辨良恶性孤立性肺结节。
综上所述,多排螺旋CT灌注成像参数以及三维重建图像征象在孤立性肺结节的定性诊断中均有一定的应用价值,但两种技术联合时,定性诊断的敏感度、特异度和准确性更高。

