关于有机化学反应中电子转移的探讨
刘新明 ,孟团结,刘澜涛
(商丘师范学院 化学化工学院,河南 商丘 476000)
有机化学是化学、制药、材料、能源、生物等专业的一门非常重要的专业基础课,对后续课程如有机合成化学、药物化学、材料的制备、生物化学等起到支撑作用[1-4]。有机化学的教学也引起了大家高度重视,然而现在大多数高校有机化学课程学时安排均在54课时左右,甚至某些专业只有36课时。一些新的教学模式,如翻转课堂、混合式教学模式、小组合作学习、微信平台辅助教学等被应用于有机化学的教学中,取得了一定的教学效果[5-8]。对于有机化学的学习,仍有不少学生反映有机化学不好掌握,知识点太零碎,需要记忆的太多,还容易记混淆。如何深入浅出地将那些深奥的、零碎的有机化学知识点解释给学生,教给他们正确的有机化学的学习方法就显得非常重要了。学习有机化学就应该追本溯源,从有机化学反应实质上来理解,万变不离其宗,触类旁通,有机化学就会觉得不那么难懂了,慢慢地就会培养有机化学学习的信心和兴趣。而有机化学反应的本质就是电子的转移,掌握了这个本质,就可以将一个个的有机化学知识点连成线,串成网,就能融会贯通,游刃有余地在有机化学知识的海洋里享受[9-14]。本文以自由基反应与离子型反应、亲电加成反应的马氏规则、乙酰乙酸乙酯衍生物的分解三个典型案列来分析有机化学反应中电子的转移情况。
1 自由基反应与离子型反应
不少学生对丙烯和氯气在不同的条件下得到了完全不同的产物表示不太理解,高温或光照的条件下得到自由基取代产物,而在四氯化碳体系得到的是加成产物。为什么会产生这样的结果呢?我们可以从化学反应甚至化学键的实质来追本溯源,分析清楚这些基本问题,就会恍然大悟,也会彻底明白这些本就该是这样的反应了。本文以丙烯与氯气的自由基取代反应和亲电加成反应为例来讨论这个问题。
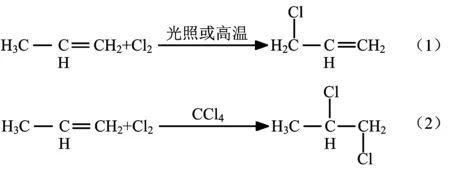
有机化学反应的实质就是旧的化学键在一定条件下发生断裂,产生碎片,然后碎片结合为新键,就完成了有机化学反应。并且旧键的断裂方式决定着新键的生成方式,就好像有米才能做米饭,有面粉才能做面食。如果旧键断裂了产生了自由基,后面只能发生自由基反应,如果旧键断裂产生了正负离子,当然就会发生离子型反应。以AB键为例来说明键的断裂。
(3)
(4)
化学键指的是分子中各原子间强烈的相互作用,那么AB化学键是如何形成的呢?首先, A、B两个原子各提供一个电子形成共用电子对,每个原子均达到8电子稳定结构,AB共价键就是A、B两个原子核对共用电子对的吸引力。AB键的断裂实质就是这对共用电子对的分配问题,应该只有两种方式:①平均分配,各自拿回自己提供的一个电子形成自由基;②不平均分配,B自身电负性强或在外界因素协助下,分得两个电子,就带一个负电荷,另一个A原子就无电子可分,相当于A原子失去了原来自己提供出来的1个电子,带1个正电荷。
回到最初的问题,因为氯分子在光照或高温的条件下发生均裂,产生了氯自由基,氯自由基进攻α氢,生成一个较稳定的烯丙基自由基,烯丙基自由基与一个氯分子反应就得到α氢被氯取代的产物和一个新的氯自由基。氯自由基不会进攻双键碳上的氢,因为这个烯氢是比较牢固的,所以只能发生自由基取代反应。而在四氯化碳体系,氯分子会发生异裂,产生氯正离子和氯负离子,氯正离子比氯负离子更活波,氯正离子带一个正电荷,他当然会和电子云密度更大双键发生作用,发生亲电进攻,因而在四氯化碳体系中会发生亲电加成反应。
2 亲电加成反应的马氏规则
马尔科夫尼可夫规则简称为马氏规则是有机化学中很重要的一个规则,是电子效应影响有机化学反应选择性的很好的体现。这是有机化学教学的重点也是难点之一,不少同学就是不明白,同样是两个双键碳,为什么大多数情况下,卤化氢与不对称烯烃加成时,氢原子主要加成到含氢较多的双键碳原子上( 5),而在某些情况下,氢原子又加到含氢少的双键碳原子上了(6)。
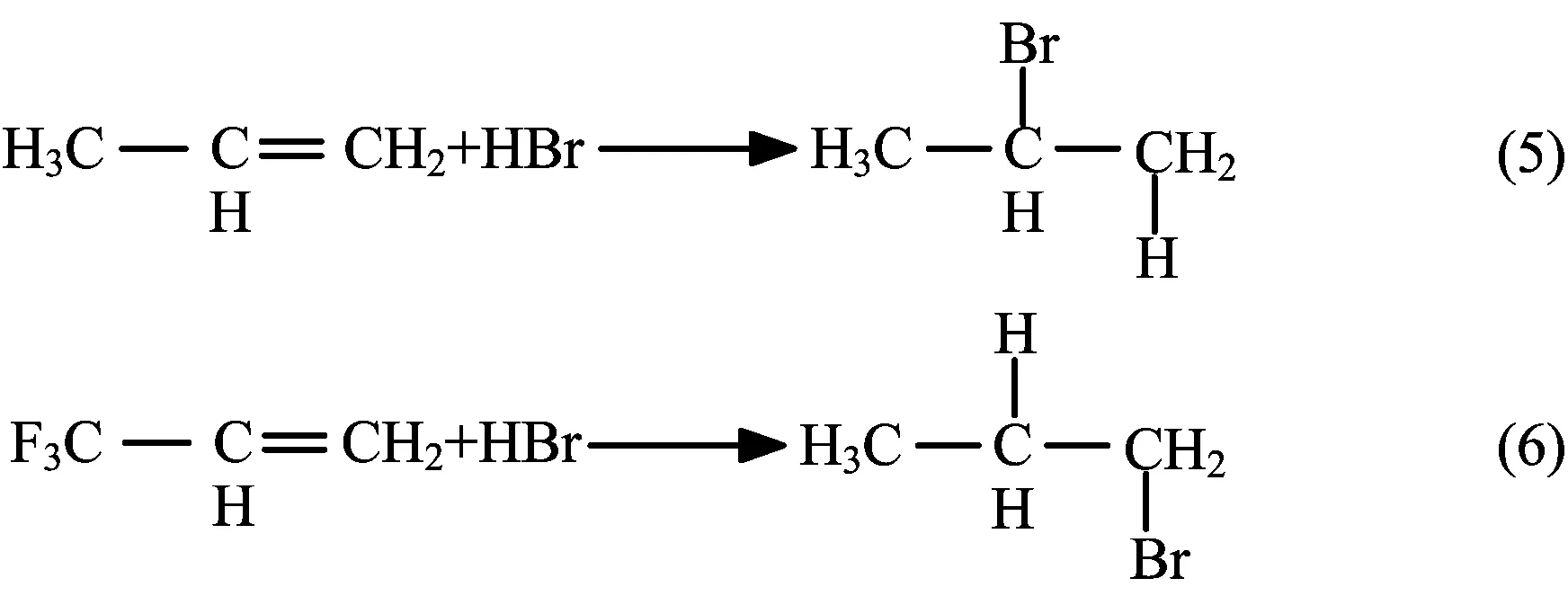
对于这个问题,我们首先需要明白烯烃与卤化氢的加成反应是亲电加成反应,亲电试剂在反应过程中可以接受电子或共享电子,所以在反应过程中它一般进攻电子云密度比较大的部位。

首先考察一下丙烯的电子云偏移情况,由于甲基的推电子作用,π电子更易流动,所以电子云偏向1号碳,溴化氢对烯烃的加成是一个亲电加成反应,氢离子首先对烯烃进行亲电进攻,当然就进攻电子云密度大的1号碳,也就是连接两个氢原子的碳原子。

而双键如果连接一个三氟甲基这样的拉电子基团,π电子就向2号碳原子偏移,使得2号碳上电子云密度更大,因而氢离子当然就会进攻2号碳,也就是含氢较少的碳,形式上不一样,实质上都是缺电子的氢离子进攻双键上电子云密度更大的碳原子,因为异种电荷相互吸引的作用力更大。
3 乙酰乙酸乙酯衍生物的分解
乙酰乙酸乙酯衍生物的酮式分解和酸式分解如下:
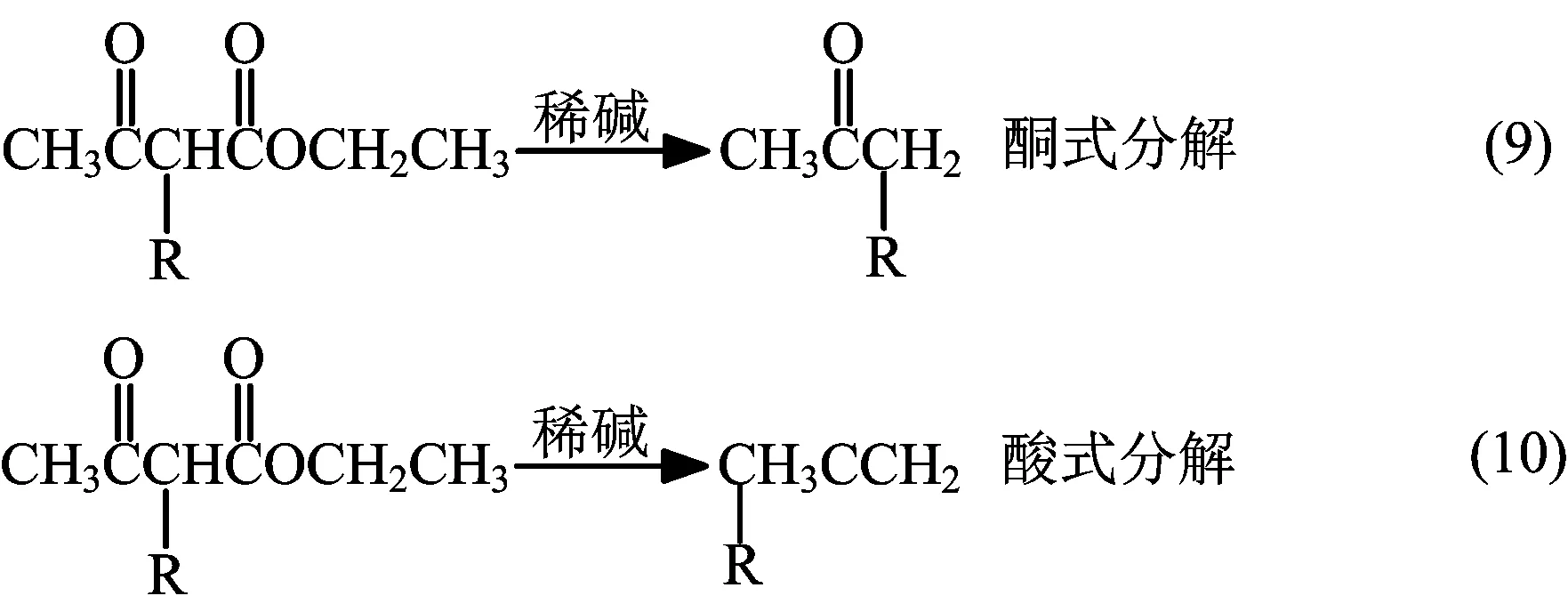
乙酰乙酸乙酯简称为三乙,是有机化学中非常重要的一个试剂,由于亚甲基连接两个强的拉电子基团使得亚甲基上的氢具有较大的活性,可以被醇钠夺取生成碳负离子,该碳负离子与卤代烃发生亲核取代反应就可以将烃基连接到乙酰乙酸乙酯上,该衍生物发生在稀碱溶液中会发生酮式分解得到甲基酮衍生物,而在浓碱溶液中会发生酸式分解得到羧酸。很多学生比较困惑,稀碱溶液和浓碱溶液的实质是一样的,都是氢氧化钠溶液,不同之处仅仅在于氢氧化钠的浓度,为什么会有不同的产物生成呢?
对这个问题的分析,依然可以从“异种电荷相互吸引”这个基本的原理来解释,对于羰基碳,由于氧的电负性大于碳,所以氧上会带部分负电荷,碳上带部分的正电荷,如果是浓碱体系,带负电的氢氧根离子就会同时对这两个羰基碳进行亲核加成反应,然后发生消除反应,就发生了酸式分解(11)。而如果在稀碱体系,氢氧根的浓度较低,无法同时进攻这两个羰基碳,那么就要看这两个羰基碳哪一个带的正电荷更多,它对氢氧根副离子的吸引力就更大,氢氧根负离子就会对该羰基进行亲核加成,加成产物在发生消除反应,脱去一分子乙氧基负离子就得到了酮式分解产物(12)。该问题的实质就是两个带部分正电荷的不同的羰基碳与带负电荷的氢氧根负离子的作用,如果氢氧根负离子的浓度够大,就会同时和这两个羰基碳反应发生酸式分解,而如果氢氧根负离子的浓度不够大,就只能有选择性地和一个羰基碳反应而发生酮式分解。


总之,如果能够从电子转移的角度来分析有机化学反应,有机反应尤其是离子反应和自由基反应就会变得很有规律。有机反应都是向着生成的活性中间体、过渡态或产物能量最低的方向进行,而活性中间体、过渡态以及最终产物的能量的高低又是由它们的电子的分布与运动决定的。所以我们只要掌握好了电子理论,用它来从本质上把握有机反应的话,有机反应就不再是那么没有规律。应该指出,无论分析的是有机化学现象还是其它问题,都要全面地、辨证地看待对象,尤其在几个相互矛盾的因素并存的情况下,首先要把握好哪一个才是主导因素。

