烟叶提取物合成酵母菌载纳米铁
石国荣,肖 苗,戴镇璇,陈 勇,侯懿轩,唐忠海
(1.湖南农业大学化学与材料科学学院,湖南 长沙 410128;2.湖南农业大学资源环境学院,湖南 长沙 410128;3.湖南农业大学食品科学技术学院,湖南 长沙 410128)
纳米铁具有强的还原性、较高的催化活性和优良的吸附性能,被广泛用于含卤有机物的还原脱卤、硝基化合物中硝基的还原、染料的还原脱色以及重金属离子的去除,是一种颇具应用潜力的环境友好型污染环境修复材料[1-2]。但纳米铁易团聚和氧化的缺点造成了其利用效率很低[3],而载体负载[4]和表面改性[5-6]都能提高纳米铁的利用效率,且经过载体负载后,纳米铁毒性也大为降低[7]。以硼氢化钠为还原剂的化学还原法是目前制备纳米铁的常用方法,所制备的纳米铁要保存在乙醇中或者需要添加聚合物或表面活性剂作为稳定剂,存在制备成本高、污染环境等问题。以茶叶[8]、桉树叶[9]、薄荷叶[10]等植物提取液为还原剂制备纳米铁不仅原料易得,而且绿色环保,提取液中的有机成分还能作为稳定剂覆盖在所合成的纳米铁表面,提高其稳定性。
铬在电镀、印染、工业制造等行业被广泛使用,所产生的大量含铬废水造成了严重的环境污染。在自然条件下,铬以Cr(Ⅲ)或Cr(Ⅵ)形式存在,Cr(Ⅵ)毒性很强,具有致癌性和致畸性,而Cr(Ⅲ)的毒性较弱,将Cr(Ⅵ)还原为Cr(Ⅲ)是降低Cr(Ⅵ)毒性的常用手段之一[11]。
酵母菌含有丰富的氨基、羟基、羧基和磷酸基团,其细胞壁和细胞膜构成的双层网状结构使其成为一种环境友好型生物吸附剂[12]和载体材料[13],已被广泛用于吸附重金属离子和有机污染物。作者以废弃烟叶提取液代替硼氢化钠合成酵母菌载纳米铁,优化纳米铁的合成条件,以Cr(Ⅵ)去除为目标,考察纳米铁去除Cr(Ⅵ)的反应活性,为纳米铁修复重金属污染提供一定的理论依据。
1 实验
1.1 材料、试剂与仪器
酵母菌,本实验室培养。废弃烟叶:于50 ℃下干燥、粉碎后过200 目筛,密封保存待用。
1,5-二苯基碳酰二肼、FeSO4·7H2O、乙醇、乙酸乙酯、丙酮、H2SO4和H3PO4均为分析纯;水为二次蒸馏水。
UV-2450型紫外光谱仪、XRD 6000型X-射线衍射仪,Shimadzu公司;SB25-16DTN型超声波清洗器,宁波新芝生物科技股份有限公司;RE-52AA型旋转蒸发仪,上海亚荣生化仪器厂。
1.2 方法
1.2.1 烟叶提取液的制备
称取1.0 g烟叶于100 mL锥形瓶中,按固液比(g∶mL,下同)1∶(10~40)加入提取溶剂,超声提取10~40 min或在室温下振荡提取1~6 h,过滤,清液在38 ℃以下浓缩至10 mL。
1.2.2 酵母菌载纳米铁的合成
称取50~300 mg酵母菌于50 mL离心管中,加入适量的FeSO4溶液,置于30 ℃水浴中搅拌30 min。在通N2条件下,加入一定量的烟叶提取液后开始计时,反应1.0~8.5 h后取出。在8 000 r·min-1条件下离心5 min,固体用无水乙醇洗涤至洗涤液无色,即得酵母菌载纳米铁。
1.2.3 酵母菌载纳米铁的反应活性
以Cr(Ⅵ)去除率表示酵母菌载纳米铁的反应活性。在5.00 mL浓度为100 mg·L-1的Cr(Ⅵ)溶液中加入合成的酵母菌载纳米铁,摇匀后置于30 ℃恒温水浴中进行搅拌反应并开始计时。定时取样,采用1,5-二苯基碳酰二肼紫外光谱法测定上清液中Cr(Ⅵ)浓度并计算Cr(Ⅵ)去除率。
2 结果与讨论
2.1 酵母菌载纳米铁的XRD表征(图1)

图1 酵母菌载纳米铁的XRD图谱Fig.1 XRD pattern of yeast supported iron nanoparticles
由图1 可以看出,在44.9°附近未见明显的Fe0衍射峰,说明酵母菌载纳米铁中无结晶状Fe0存在,这与文献[14]报道一致。
2.2 烟叶提取液制备条件优化
2.2.1 提取溶剂对纳米铁去除Cr(Ⅵ)反应活性的影响
分别在1.0 g烟叶中加入25 mL乙醇、丙酮、乙酸乙酯或蒸馏水,超声30 min制备烟叶提取液,然后在相同条件下合成酵母菌载纳米铁,提取溶剂对纳米铁去除Cr(Ⅵ)反应活性的影响如表1所示。
植物多酚类物质在植物提取液还原铁盐或亚铁盐制备纳米铁的反应中起重要作用[15],提取液中多酚类物质越多,其还原的铁盐或亚铁盐越多,所得纳米铁的还原性越强。烟草行业标准YC/T 202-2006[16]中,推荐采用50%甲醇提取烟草中的绿原酸、芸香苷等多
表1 提取溶剂对纳米铁去除Cr(Ⅵ)反应活性的影响
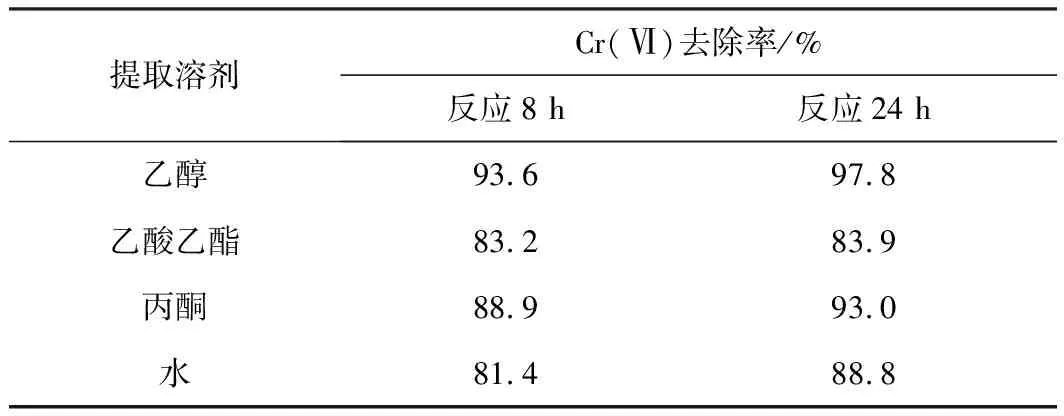
Tab.1 Effect of extraction solvent on Cr(Ⅵ) removal activity of iron nanoparticles
酚类物质。由表1可以看出,在4种烟叶提取液中,由烟叶乙醇提取液合成的纳米铁去除Cr(Ⅵ)的性能最好,反应24 h Cr(Ⅵ)去除率达到97.8%。因此,烟叶提取溶剂选用乙醇。
2.2.2 固液比对纳米铁去除Cr(Ⅵ)反应活性的影响
分别在1.0 g烟叶中加入10 mL、20 mL、25 mL和40 mL乙醇,超声30 min制备烟叶提取液,然后在相同条件下合成酵母菌载纳米铁,固液比对纳米铁去除Cr(Ⅵ)反应活性的影响如图2所示。
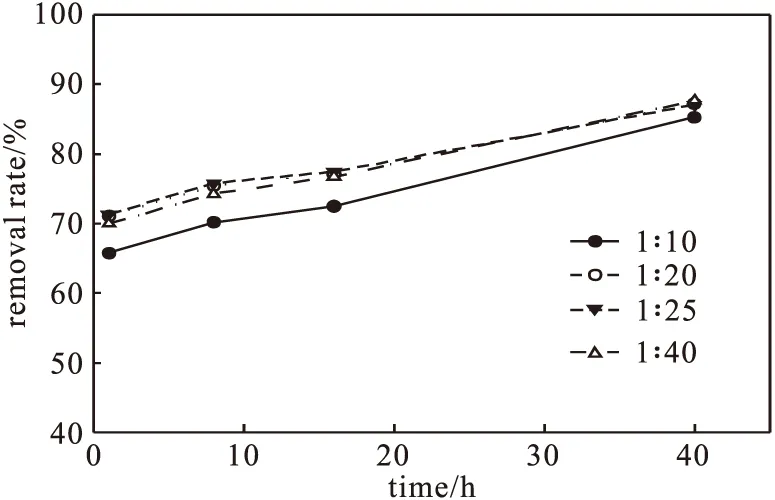
图2 固液比对纳米铁去除Cr(Ⅵ)反应活性的影响Fig.2 Effect of leaf mass-solvent volume ratio on Cr(Ⅵ)removal activity of iron nanoparticles
从图2可以看出,采用固液比为1∶20、1∶25、1∶40提取的烟叶提取液合成酵母菌载纳米铁,其去除Cr(Ⅵ)的反应活性相当。因此,选择固液比为1∶20。
2.2.3 超声时间对纳米铁去除Cr(Ⅵ)反应活性的影响
固定烟叶与乙醇的固液比为1∶20,将1.0 g烟叶分别用乙醇超声10 min、20 min、30 min和40 min制备烟叶提取液,然后在相同条件下合成酵母菌载纳米铁,超声时间对纳米铁去除Cr(Ⅵ)反应活性的影响如图3所示。
从图3可以看出,酵母菌载纳米铁对Cr(Ⅵ)的去除率随超声时间的延长而升高,当烟叶超声时间超过30 min后,所合成的纳米铁去除Cr(Ⅵ)的反应活性增强缓慢。因此,烟叶提取选择超声时间为30 min。

图3 超声时间对纳米铁去除Cr(Ⅵ)反应活性的影响Fig.3 Effect of ultrasonic time on Cr(Ⅵ) removal activity of iron nanoparticles
2.2.4 提取方式对纳米铁去除Cr(Ⅵ)反应活性的影响
取1.0 g烟叶加入20 mL乙醇,分别在30 ℃恒温水浴中振荡提取1 h、2 h、4 h和6 h制备烟叶提取液,然后在相同条件下合成酵母菌载纳米铁,振荡提取时间对纳米铁去除Cr(Ⅵ)反应活性的影响如表2所示。
表2 振荡提取时间对纳米铁去除Cr(Ⅵ)反应活性的影响

Tab.2 Effect of shaking extraction time on Cr(Ⅵ) removal activity of iron nanoparticles
由表2可以看出,振荡提取2~4 h所得烟叶提取液合成的酵母菌载纳米铁去除Cr(Ⅵ)的反应活性与超声提取30 min所得提取液合成的纳米铁相当,延长振荡提取时间到6 h,纳米铁去除Cr(Ⅵ)的反应活性降低。这可能是由于,绿原酸等多酚类物质很不稳定,延长烟叶振荡提取时间到6 h,反而会导致多酚类物质氧化[15]。因此,可以采用振荡提取2 h代替超声30 min制备烟叶提取液来合成酵母菌载纳米铁。
2.3 纳米铁合成条件优化
2.3.1 烟叶提取液用量的确定
称取10.0 g烟叶,按固液比1∶20制备烟叶乙醇提取液并浓缩到100 mL。在50 mg吸附有10 mg 亚铁盐的酵母菌中分别加入2.0 mL、3.0 mL、4.0 mL和10.0 mL烟叶提取液合成酵母菌载纳米铁,烟叶提取液用量对纳米铁去除Cr(Ⅵ)反应活性的影响如图4所示。

图4 烟叶提取液用量对纳米铁去除Cr(Ⅵ)反应活性的影响Fig.4 Effect of tobacco leaf extract dosage on Cr(Ⅵ) removalactivity of iron nanoparticles
从图4可以看出,当烟叶提取液用量在3.0 mL以上时,所合成的纳米铁对Cr(Ⅵ)去除率相近,并可达到最大恒定值。因此,选择3.0 mL烟叶提取液合成酵母菌载纳米铁。
2.3.2 亚铁盐与酵母菌质量比的确定
分别在20 mg、50 mg、100 mg、200 mg和300 mg酵母菌中加入含有10 mg亚铁盐的溶液吸附30 min后,再加入3.0 mL烟叶乙醇提取液合成酵母菌载纳米铁。在所得纳米铁中分别加入100 mg·L-1Cr(Ⅵ)溶液5.00~20.00 mL,测定Cr(Ⅵ)去除量,亚铁盐与酵母菌质量比对纳米铁去除Cr(Ⅵ)反应活性的影响如表3所示。
表3 亚铁盐与酵母菌质量比对纳米铁去除Cr(Ⅵ)反应活性的影响

Tab.3 Effect of mass ratio of ferrous salt to yeast on Cr(Ⅵ)removal activity of iron nanoparticles
纳米铁的表面效应和小尺寸效应是其反应活性高的主要原因。从表3可以看出,酵母菌载纳米铁的Cr(Ⅵ)去除量与其铁含量间无线性关系,当亚铁盐与酵母菌质量比从1∶2增加到1∶10时,Cr(Ⅵ)去除量增加了2.29倍,由于此时纳米铁中铁含量仅增加了15.8%,因此,酵母菌用量增大4倍后,酵母菌的分散作用有效地降低了纳米铁的团聚,从而显著提高了酵母菌载纳米铁的Cr(Ⅵ)去除活性;而当质量比从1∶10增加到1∶30时,虽然纳米铁中铁含量增加了54.4%,Cr(Ⅵ)去除量却只增加了9.8%。这可能是因为,随着酵母菌用量的继续增大,一方面进一步降低了纳米铁的团聚性,但同时也使纳米铁暴露在空气中的机会迅速增大而导致纳米铁氧化失活,因而酵母菌载纳米铁去除Cr(Ⅵ)的活性增加不显著。可见,酵母菌载纳米铁去除Cr(Ⅵ)不仅与其铁含量有关,还与酵母菌及纳米铁的组成和结构密切相关。综合考虑,选择亚铁盐与酵母菌的质量比为1∶10合成酵母菌载纳米铁。
2.3.3 合成反应时间的确定
固定亚铁盐与酵母菌的质量比为1∶10,加入3.0 mL烟叶提取液,在室温下分别反应1 h、3 h、5 h和8.5 h合成酵母菌载纳米铁,合成反应时间对纳米铁去除Cr(Ⅵ)反应活性的影响如图5所示。
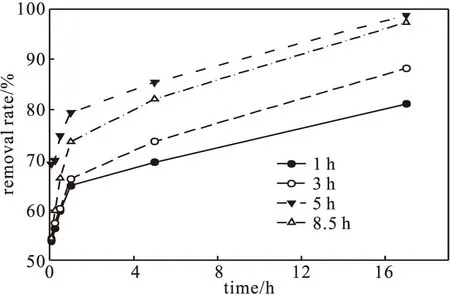
图5 合成反应时间对纳米铁去除Cr(Ⅵ)反应活性的影响Fig.5 Effect of synthesis reaction time on Cr(Ⅵ) removal activity of iron nanoparticles
从图5可以看出,酵母菌载纳米铁去除Cr(Ⅵ)的反应活性随着烟叶提取液与亚铁盐合成反应时间的延长而增强,反应5 h合成的纳米铁去除Cr(Ⅵ)的活性最强;延长合成反应时间至8.5 h,纳米铁的反应活性降低。这可能是由于,随着合成反应时间的延长,生成的纳米铁在酸性反应介质中的腐蚀作用加剧[17]。因此,选择酵母菌载纳米铁的合成反应时间为5 h。
3 结论
以酵母菌为载体和分散剂,烟叶乙醇提取液为还原剂和稳定剂,原位还原FeSO4合成酵母菌载纳米铁。结果表明,以固液比为1∶20(g∶mL)的烟叶乙醇提取液还原亚铁盐的能力最强,而室温振荡提取2 h与超声提取30 min的乙醇提取液还原性能相当;当亚铁盐与酵母菌质量比为1∶10时,以固液比为1∶20的烟叶乙醇提取液在室温下反应5 h合成的酵母菌纳米铁最适于去除Cr(Ⅵ)。

