牛黄上清丸(大蜜丸)微生物限度检查法方法适用性试验研究
王 瑛,王丽霞,买买提·艾买提
(1.黑龙江省药品检验研究中心,黑龙江 哈尔滨 150001;2.哈尔滨市食品药品行政执法局,黑龙江 哈尔滨 150001;3.新疆哈密市食品药品检验所,新疆 哈密 839000)
对牛黄上清丸(大蜜丸)的处方及其制造工艺进行研究,检验牛黄上清丸(大蜜丸)之中生药原粉含量,应用《药典四部附录通则(2015版)》--1107相关标准进行判断,牛黄上清丸(大蜜丸)之中需氧菌总数≤3×104cfu/g,霉菌和酵母菌总数应≤102 cfu,沙门菌每10 g不得检出,大肠埃希菌每克不得检出,耐胆盐革兰阴性菌每克应<102cfu[1]。
1 仪器与材料
1.1 仪器
超净台生产厂家:AIRTECH,仪器型号:SW-CJ-2FD;电子天平生产厂家:METTLER,仪器型号:PL202-S;匀浆仪生产厂家:泰林生物技术设备有限公司,仪器型号:HTY-761;生物安全柜生产厂家:HealForce,仪器型号:Hfsafe-1200A2;电热恒温培养箱生产厂家:天津市泰斯特仪器有限公司,仪器型号:DH5000A;生化培养箱生产厂家:上海博迅实业有限公司医疗设备厂,仪器型号:SPX-250B-Z型;高压蒸汽灭菌器生产厂家:Panasonic,仪器型号:MLS-3781L-PC;培养箱生产厂家:上海精宏实验设备有限公司,仪器型号:MJPS-250;涡旋混合器生产厂家:IKA,仪器型号:VORTEX3。
1.2 培养基
培养基符合《中国药典》2015年版四部附录通则的相关规定[2],包括胰酪大豆胨琼脂培养基、胰酪大豆胨液体培养基、沙氏葡萄糖肉汤、沙氏葡萄糖琼脂培养基、麦康凯液体培养基、麦康凯琼脂培养基、RV沙门增菌液体培养基、木糖赖氨酸脱氧胆酸盐琼脂培养基、肠道菌增菌肉汤培养基、紫红胆盐葡萄糖琼脂培养基等。
1.3 菌株
全部所应用的菌株均为中国食品药品检定研究院提供的5代内菌种,包括金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌、黑曲霉、乙型副伤寒沙门菌、大肠埃希氏菌等。
2 方法和结果
2.1 微生物计数法适用性试验
采用胰酪大豆胨液体培养基实施铜绿假单胞菌、金黄色葡萄球菌及枯草芽孢杆菌接种,培养后应用氯化钠溶液10倍递增稀释,菌悬液制成每含菌量≤104 cfu/mL;黑曲霉斜面混合5 mL聚山梨酯及无菌氯化钠溶液,后吸出孢子悬液10倍稀释,孢子悬液制成含菌量≤104 cfu/mL。采用沙氏葡萄糖液体培养基实施白色念珠菌接种,培养后应用氯化钠溶液10倍递增稀释,菌悬液制成含菌量≤104 cfu/mL。
取5份9.9 mL供试液,分别加入铜绿假单胞菌、金黄色葡萄球菌、枯草芽孢杆菌、黑曲霉、白色念珠菌,分别为0.1 mL混匀,抽取1 mL置入到无菌平皿中,置于胰酪大豆胨琼脂培养基中,温度≤45℃,平行制备2个平皿。
取2份9.9 mL供试液,分别加入黑曲霉菌、白色念珠菌试验菌菌液,分别为0.1 mL,取1 mL置入到无菌平皿中,置于沙氏葡萄糖琼脂培养基中,温度≤45℃,平行制备2个平皿。
对照组应用供试液与稀释液混合后实施各项操作。
试验组平均菌落数与供试品对照组平均菌落数之差,同菌液对照组平均菌落数的比值为菌回收率,见表1。
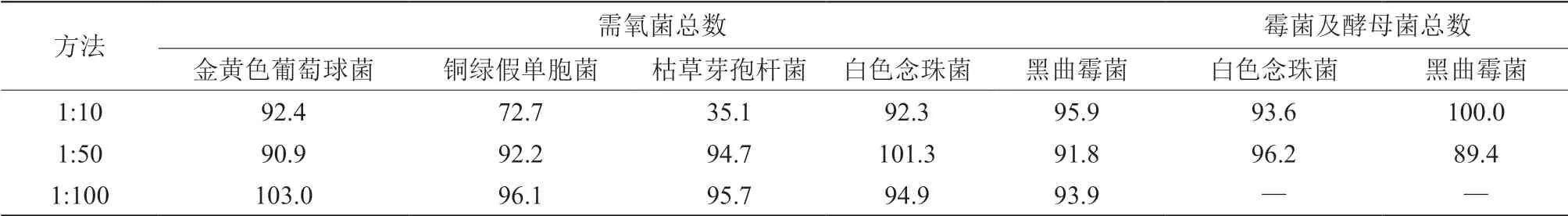
表1 计数方法适用性试验回收率
2.2 控制菌检查法适用性试验
取供试液(供试品)与100 mL胰酪大豆胨液体培养基实施接种,分别放置1 mL大肠埃希菌菌液、乙型副伤寒沙门菌菌液;取供试液(供试品)与100 mL10 mL肠道菌增菌液体培养基实施接种,分别放置1 mL大肠埃希菌菌液、铜绿假单胞菌菌液。阴性对照试验通过稀释液予以检验,见表2。
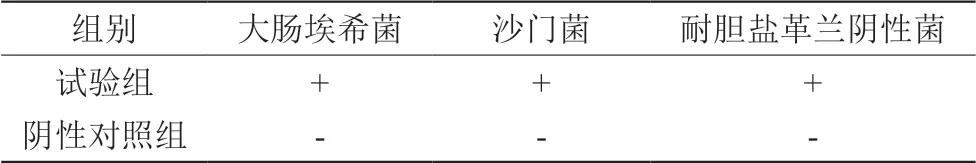
表2 控制菌检查法适用性试验情况
3 讨 论
企业提供的牛黄上清丸经过检验可知,牛黄上清丸(大蜜丸)抑菌性欠佳,在培养基稀释法检验方式,能够降低其抗菌活性、药渣对菌落计数结果所产生的影响。对比《中国药典》2015版与2010版试验方法,可知2010版方法并不会因为2015版方法改变而完全废弃,它可作为探索新方法的参考,虽然2010版方法不能真实的反映药品对菌液的抑制能力,但是它也客观的体现出药品是否具有抑菌性、抑菌能力的强弱。

