邻苯二甲酸二丁酯的GC检测及其合成动力学研究
刘晴晴 ,叶晓洁 ,齐然 ,张志昆 ,刘玉敏 *
(1.河北科技大学化学与制药工程学院,河北石家庄050018;2.河北省药用分子化学重点实验室,河北石家庄050018)
邻苯二甲酸二丁酯(DBP)为一种果香味的无色、无毒的透明液体,不溶于水,易溶于大多数有机溶剂[1]。DBP用途广泛,需求量较大,主要应用于增塑剂方面。另外,也被用于有机合成和日用化工产品中[2]。由于其相对廉价,且加工性好,其产量占我国增塑剂总量的20%以上[3]。目前工业上DBP的合成主要采用苯酐和正丁醇为原料,以浓硫酸作为催化剂合成DBP。鉴于工业上对该法DBP合成的广泛应用,本论文首先建立了DBP的分析方法,然后对该合成过程的动力学进行跟踪测定和分析,以达到更好地控制DBP的合成。
1 实验部分
1.1 试剂与仪器
苯酐(分析纯,山东旭晨化工科技有限公司);正丁醇(分析纯,天津市永大化学试剂有限公司);氢氧化钠(优级纯,北京化工厂);浓硫酸(分析纯,北京志盛威华科技发展有限公司)。
安捷伦气相色谱仪SP-7820A。
1.2 DBP气相色谱检测条件
毛细管色谱柱dlhws PEG-20M:250℃,50 m×320μ m× 0.4μ m;载气为高纯氮(纯度 99.99%),流量2 mL/min;尾吹气流量60 mL/min;空气流量400 mL/min;氢气流量40 mL/min;进样口温度240℃;前检测器温度300℃;进样量0.2μL。
柱温采用程序升温:初始温度100℃,保持5min;以25℃/min的升温速率升至240℃,保持5 min,共运行17 min。分流比100∶1。
1.3 DBP标准样品配置及其合成
标准溶液配置,分别取一定量的DBP标准储备液于10 mL的容量瓶中,用无水乙醇定容。分别配置不同百分比含量的DBP乙醇溶液。
DBP合成,其工艺流程图如图1所示。在装有磁转子、温度计和醇水分离器的三口烧瓶中,按一定配比加入一定量的苯酐和正丁醇,升温反应,温度达到140℃时,缓慢滴加一定量的浓硫酸,反应温度控制在140~150℃,反应直到温度不变时,停止反应,冷却。取出一定量的溶液用氢氧化钠中和,静置分层,再用水洗涤2~3遍。用气相色谱法测定产品的纯度,再通过外标法计算产率。
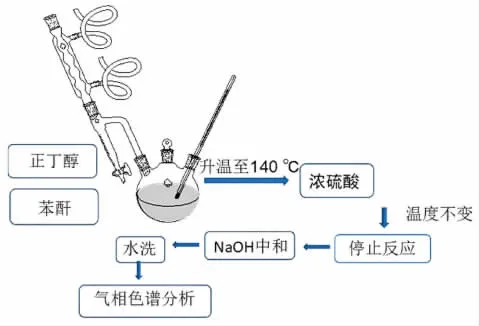
图1 DBP合成工艺流程图
2 结果与讨论
2.1 DBP合成机理
DBP的合成是一个连串反应,其反应机理如图2所示[4]。目前工业生产企业主要以苯酐和正丁醇为原料,以浓硫酸为催化剂酯化合成DBP。a)步为酯化反应,苯酐与正丁醇首先生成邻苯二甲酸单酯,该步反应不需催化剂,是放热反应,且反应速率快。b)步反应为邻苯二甲酸单酯与正丁醇反应脱去1分子水生成DBP。该酯化反应是可逆吸热反应,反应速率很慢,需要在催化剂的作用下才能反应。该反应主反应是b)可逆的吸热反应,反应速率很慢,是整个反应的速率控制步骤。
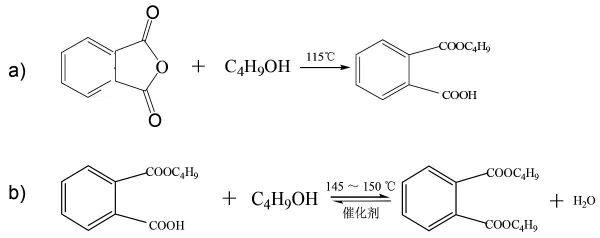
图2 DBP合成机理图
2.2 DBP气相色谱检测方法建立
DBP合成过程中反应物及其产物包含正丁醇、丁醚和DBP。为有效跟踪DBP合成过程,本文首先建立正丁醇、丁醚和DBP的气相色谱分析方法。气相色谱检测采用毛细管色谱柱,结果如图3所示。该方法能够有效地分析检测DBP反应中的各个物质。正丁醇、丁醚以及DBP的保留时间分别为1.707,1.193和14.000 min,三种物质出峰保留时间不重合。

图3 正丁醇、丁醚和DBP的气相色谱图
为实现DBP合成过程的定量分析[5,6],我们配置不同含量的DBP的乙醇溶液,建立其气相色谱外标法,并绘制出标准曲线。结果如图4-图6所示。
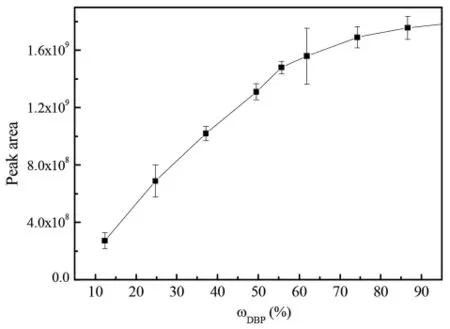
图4 气相色谱峰面积(Peak area)随DBP(w)百分含量的变化
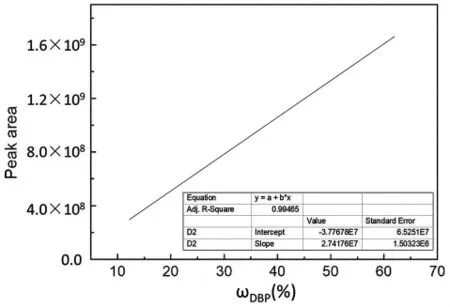
图5 DBP质量分数为10%~60%的气相色谱标准曲线拟合图
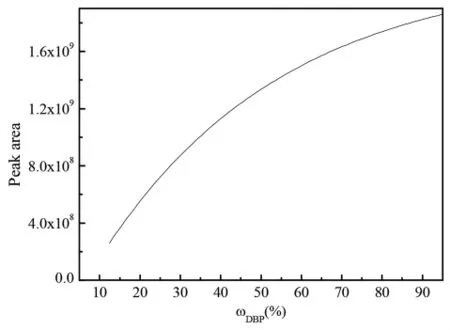
图6 DBP气相色谱标准曲线拟合图
由图5标准曲线所得方程
y=-3.7768× 107+2.7418× 107x
由图6标准曲线所得方程
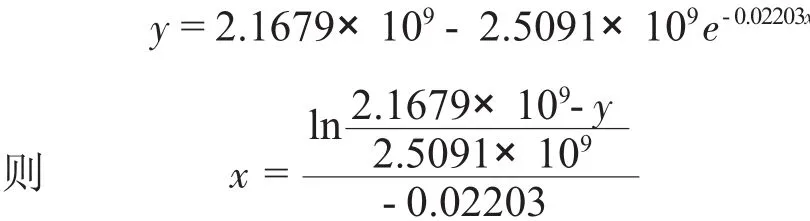
采用苯酐和正丁醇为原料,以浓硫酸作为催化剂合成DBP,基于标准曲线,考察了4次该反应的反应收率。
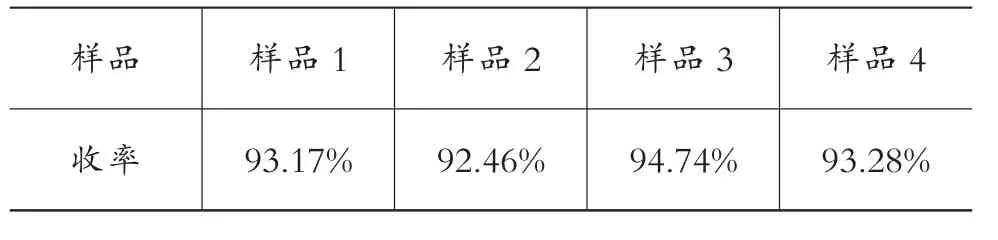
表1 DBP合成反应收率
2.2 邻苯二甲酸二丁酯的反应动力学研究
动力学研究必须对该反应随时间的变化、反应体系中的产品分布进行跟踪测定,因此采用气相色谱对苯酐与正丁醇在催化剂作用下合成DBP的反应进行了跟踪测定[8]。
在酯化过程中由于产物水不断蒸出,烧瓶中水的含量极低,因此DBP酯化反应可以看作是不可逆的二级反应,同时假设对于单酯酸、正丁醇反应均是一级反应,其动力学方程式可以表示为[9]:

其中,CA=CA0-x,CB=CB0-x,CA0和 CA分别为单酯酸的起始浓度和t时刻的浓度,mol/L;CB0,CB分别是正丁醇的起始和t时刻的浓度,mol/L;x为经t时刻后转化掉的浓度也是DBP的浓度,mol/L;r为反应速率,mol/(L·min);k2为反应速率常数,L/(mol·min)。
若另 Y=CB0-CA0,则 CB-CA=Y,CB=CA+Y,代入方程(1)得:

对t和1/Y ln(Y/CA+1)作线性关系,可得到反应速率常数。
苯酐的起始浓度为3.57 mol/L,则第二步反应单酯酸的起始浓度也是3.57 mol/L,即CA0=3.57 mol/L;对于第二步反应正丁醇的起始浓度为4.42 mol/L,即CB0=4.42 mol/L,所以 Y=CB0-CA0=0.85 mol/L,即 CA=CA0-x=(3.57-x)mol/L。以时间/min为横坐标,以1/Y ln(Y/CA+1)(L/mol)为纵坐标,得线性回归方程为:y=4× 10-5x+0.2506,R2=0.9123,其结果如表 2所示。
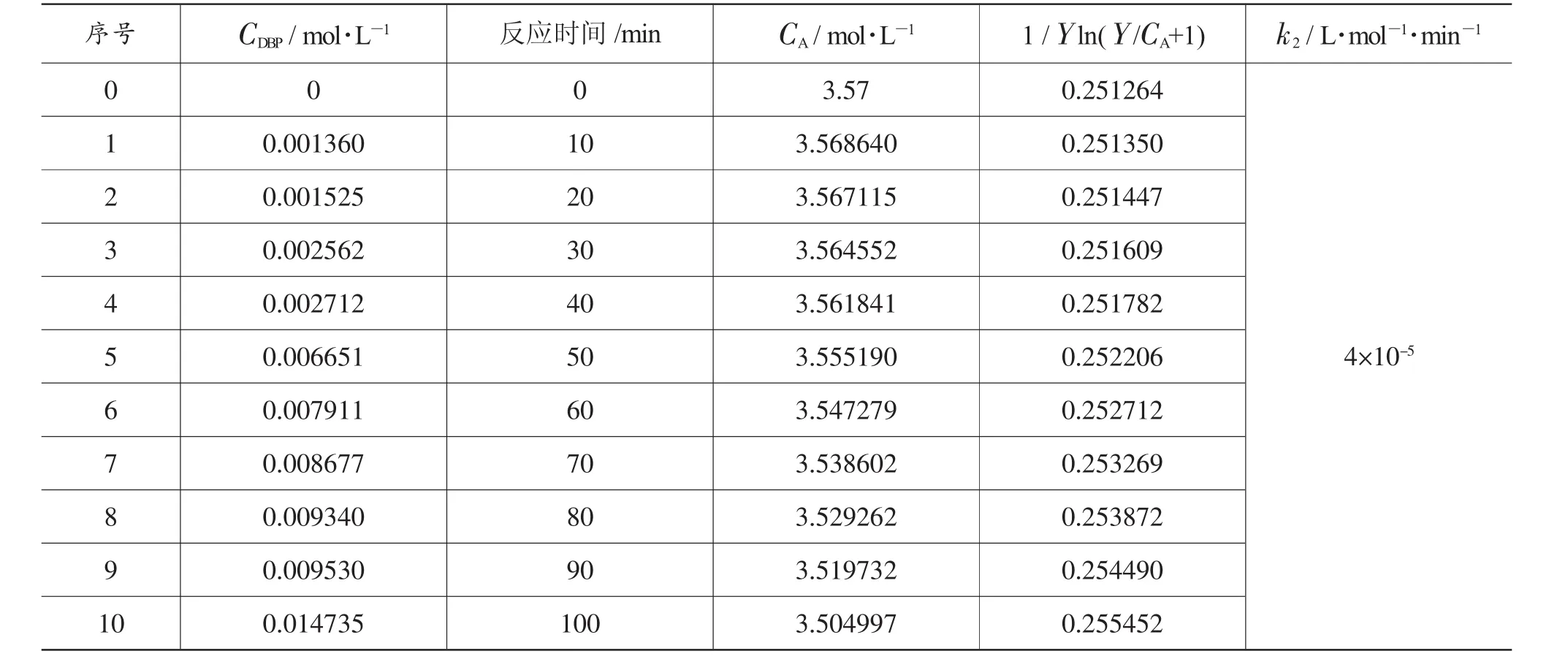
表2 DBP合成第二步反应的反应速率常数
用表2数据绘图,可以看出t对1/Y ln(Y/CA+1)是良好的线性关系,且该直线斜率就是第二步反应的速率常数,即 k2=4× 10-5L/(mol·min),因此上述假设成立,即第二步反应为二级反应,对单酯酸、正丁醇反应均是一级反应。
因此,DBP合成的第二步反应的反应动力学方程为:
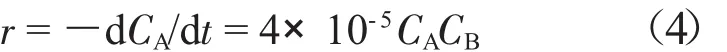
3 结论
1)本文建立了气相色谱法测定DBP,该方法简单,快速,精确;
2)以浓硫酸为催化剂合成的邻苯二甲酸二丁酯,收率达到93.41%。
3)使用气相色谱测定了DBP反应中产品的浓度随时间的变化,发现该变化符合连串反应的规律[10]。苯酐与丁醇生成单酯酸的反应是快反应,单酯酸与丁醇生成DBP的反应是慢反应,且反应速率常数为4× 10-5L/(mol·min)。

